Аккумулятор это устройство для – устройство, виды и принцип работы АКБ, а также срок службы и характеристики батареи
- 17.04.2019
|
Типовые характеристики разряда Li-ion и Li-polymer элементов
Конструкция Li-ion элемента (не аккумулятора).
| |||
Литий-ионный аккумулятор — Википедия
 Литий-ионный аккумулятор цилиндрический, типоразмера 18650
Литий-ионный аккумулятор сотового телефона Siemens, призматический[1]
Литий-ионный аккумулятор цилиндрический, типоразмера 18650
Литий-ионный аккумулятор сотового телефона Siemens, призматический[1]Литий-ионный аккумулятор (Li-ion) — тип электрического аккумулятора, который широко распространён в современной бытовой электронной технике и находит своё применение в качестве источника энергии в электромобилях и накопителях энергии в энергетических системах. Это самый популярный тип аккумуляторов в таких устройствах как сотовые телефоны, ноутбуки, цифровые фотоаппараты, видеокамеры и электромобили.
Основной источник: [2]Впервые принципиальная возможность создания литиевых аккумуляторов на основе способности дисульфид титана или дисульфид молибдена включать в себя ионы лития при разряде аккумулятора и экстрагировать их при зарядке была показана в 1970 году Майклом Стэнли Уиттингемом. Существенным недостатком таких аккумуляторов являлось низкое напряжение — 2,3 В и высокая пожароопасность вследствие образования дендритов металлического лития, замыкающих электроды.
Позднее Дж. Гуденафом были синтезированы другие материалы для катода литиевого аккумулятора — кобальтит лития LixCoO2(1980 год), феррофосфат лития LiFePO4 (1996 год). Преимуществом таких аккумуляторов является более высокое напряжение — около 4 В.
Современный вариант литий-ионного аккумулятора с анодом из графита и катодом из кобальтита лития изобрёл в 1991 году Акира Ёсино. Первый литий-ионный аккумулятор по его патенту выпустила корпорация Sony в 1991 году.
В настоящее время ведутся исследования по поиску материалов на основе кремния и фосфора, обеспечивающих повышенную емкость интеркалирования ионов лития и по замене ионов лития на ионы натрия.
Нобелевская премия по химии 2019 года была вручена троим перечисленным выше учёным «За создание литий-ионных батарей».
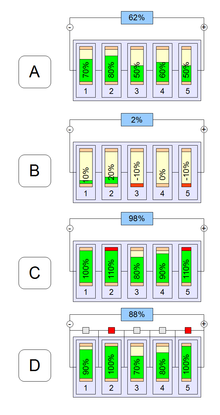 При использовании литий-ионных аккумуляторов в составе батарей без балансирующего устройства, часть из них окажется переразряженной (B) при работе батареи или перезаряженной (C) либо не дозаряженной (D) до номинальной ёмкости во время зарядки батареи
При использовании литий-ионных аккумуляторов в составе батарей без балансирующего устройства, часть из них окажется переразряженной (B) при работе батареи или перезаряженной (C) либо не дозаряженной (D) до номинальной ёмкости во время зарядки батареиХарактеристики литий-ионных аккумуляторов зависят от химического состава составляющих компонентов и варьируются в следующих пределах:
Контроллер заряда/разряда (плата защиты) цилиндрического литий-ионного аккумулятора, конструкционно припаянный к отрицательному контакту аккумулятора и обратной фольгированной стороной выполняющий его функции. На снимке частично демонтирован и отсоединён от проводника, идущего к положительному контакту аккумулятораЧасто в корпус аккумулятора встраивают контроллер защиты (или PCB-плата (англ. Protection Circuit Module)), который отключает аккумулятор, предотвращая превышение напряжения заряда, чрезмерный разряд и превышение температуры, приводящие его к преждевременной деградации или разрушению. Также этот контроллер может опционально ограничивать ток потребления. Тем не менее, надо учитывать, что не все аккумуляторы снабжаются защитой. В целях снижения стоимости производители могут не устанавливать её. Кроме того, в устройствах в которых встроен контроллер защиты, а также в аккумуляторных батареях (к примеру ноутбуков) используются только аккумуляторы без встроенной платы защиты[6].
Литиевые аккумуляторы имеют специальные требования при подключении нескольких ячеек последовательно. Зарядные устройства для таких многосоставных аккумуляторов с ячейками или сами аккумуляторные батареи снабжаются схемой балансировки ячеек. Смысл балансировки в том, что электрические свойства ячеек могут немного отличаться, и какая-то ячейка достигнет полного заряда/разряда раньше других. При этом необходимо прекратить заряд этой ячейки, продолжая заряжать остальные, так как переразряд или перезаряд литий-ионных аккумуляторов выводит их из строя. Эту функцию выполняет специальный узел — балансир[en] (или BMS-плата (англ. Battery Management System)[7]). Он шунтирует заряженную ячейку так, чтобы ток заряда шёл мимо неё. Балансиры одновременно выполняют функцию платы защиты в отношении каждого из аккумуляторов, так и батареи в целом[8][9].
Зарядные устройства могут поддерживать конечное напряжение заряда в диапазоне 4,15—4,25В.
Кроме контроллера защиты, литий-ионные, а также литий-полимерные аккумуляторы выпускаемые в формфакторах АА и ААА с напряжением 1,5 В (не следует путать с аналогичного размера формфакторами 14500 и 10440 напряжением 3,7 В, а также с незаряжаемыми одноразовыми литиевыми элементами питания напряжением тоже 1,5 В) оборудуются встроенными электронными преобразователями напряжения. Отличие таких аккумуляторов — стабилизированное напряжение на выходе на контактах в 1,5 В независимо от рабочего напряжения самой ячейки аккумулятора и его моментальное обнуление, когда напряжение самой литиевой ячейки становится ниже допустимого (срабатывает плата защиты).
Литий-ионный аккумулятор. Схема работыЛитий-ионный аккумулятор состоит из электродов (катодного материала на алюминиевой фольге и анодного материала на медной фольге), разделённых пористым сепаратором, пропитанным электролитом. Пакет электродов помещён в герметичный корпус, катоды и аноды подсоединены к клеммам-токосъёмникам. Корпус иногда оснащают предохранительным клапаном, сбрасывающим внутреннее давление при аварийных ситуациях или нарушениях условий эксплуатации. Литий-ионные аккумуляторы различаются по типу используемого катодного материала. Переносчиком заряда в литий-ионном аккумуляторе является положительно заряженный ион лития, который имеет способность внедряться (интеркалироваться) в кристаллическую решётку других материалов (например, в графит, оксиды и соли металлов) с образованием химической связи, например: в графит с образованием LiC6, оксиды (LiMnO2) и соли (LiMnRON) металлов.
Первоначально в качестве отрицательных пластин применялся металлический литий, затем — каменноугольный кокс. В дальнейшем стал применяться графит. Применение оксидов кобальта позволяет аккумуляторам работать при значительно более низких температурах, повышает количество циклов разряда/заряда одного аккумулятора. Распространение литий-железо-фосфатных аккумуляторов обусловлено их относительно низкой стоимостью. Литий-ионные аккумуляторы применяются в комплекте с системой контроля и управления — СКУ или BMS (battery management system), — и специальным устройством заряда/разряда.
В настоящее время в массовом производстве литий-ионных аккумуляторов используются три класса катодных материалов:
- кобальтат лития LiCoO2 и твёрдые растворы на основе изоструктурного ему никелата лития
- литий-марганцевая шпинель LiMn2O4
- литий-феррофосфат LiFePO4.
Электрохимические схемы литий-ионных аккумуляторов:
- литий-кобальтовые LiCoO2 + 6C → Li1-xCoO2 + LiC6
- литий-ферро-фосфатные LiFePO4 + 6C → Li1-xFePO4 + LiC6
Благодаря низкому саморазряду и большому количеству циклов заряда/разряда, Li-ion-аккумуляторы наиболее предпочтительны для применения в альтернативной энергетике. При этом, помимо системы СКУ они укомплектовываются инверторами (преобразователи напряжения).
- Высокая энергетическая плотность (ёмкость).[источник не указан 660 дней]
- Низкий саморазряд.
- Высокий ток работы
- Не требуют обслуживания.
Широко применяемые литий-ионные аккумуляторы при перезаряде, несоблюдении условий заряда или при механическом повреждении часто бывают чрезвычайно огнеопасными.
- Огнеопасны
- Теряют работоспособность при переразряде
- Теряют ёмкость на холоде
- От 200 до 500 циклов зарядки
Взрывоопасность[править | править код]
 | Статья или раздел содержит противоречия и не может быть понята однозначно. Следует разрешить эти противоречия, используя более точные авторитетные источники или корректнее их цитируя. На странице обсуждения должны быть подробности. |

Аккумуляторы Li-ion первого поколения были подвержены взрывному эффекту. Это объяснялось тем, что в них использовался анод из металлического лития, на котором в процессе многократных циклов зарядки/разрядки возникали пространственные образования (дендриты), приводящие к замыканию электродов и, как следствие, возгоранию или взрыву. Этот недостаток удалось окончательно устранить заменой материала анода на графит. Подобные процессы происходили и на катодах литий-ионных аккумуляторов на основе оксида кобальта при нарушении условий эксплуатации (перезарядке). Литий-ферро-фосфатные аккумуляторы полностью лишены этих недостатков. Кроме того, все современные зарядные устройства для литий-ионных аккумуляторов предотвращают перезаряд и перегрев вследствие слишком интенсивного заряда.[источник не указан 539 дней]
Литиевые аккумуляторы изредка проявляют склонность к взрывному самовозгоранию.[17][18][19] Интенсивность горения даже от миниатюрных аккумуляторов такова, что может приводить к тяжким последствиям.[20] Авиакомпании и международные организации принимают меры к ограничению перевозок литиевых аккумуляторов и устройств с ними на авиатранспорте.[21][22]
Самовозгорание литиевого аккумулятора очень плохо поддается тушению традиционными средствами. В процессе термического разгона неисправного или поврежденного аккумулятора происходит не только выделение запасенной электрической энергии, но и ряд химических реакций, выделяющих вещества для поддержания горения, горючие газы от электролита[23], а также в случае не LiFePO4 электродов[24], выделяется кислород. Потому вспыхнувший аккумулятор способен гореть без доступа воздуха и для его тушения непригодны средства изоляции от атмосферного кислорода. Более того, металлический литий активно реагирует с водой с образованием горючего газа водорода, потому тушение литиевых аккумуляторов водой эффективно только для тех видов аккумуляторов, где масса литиевого электрода невелика. В целом тушение загоревшегося литиевого аккумулятора неэффективно. Целью тушения может быть лишь снижение температуры аккумулятора и предотвращение распространения пламени[25][26][27].
Эффект памяти[править | править код]
Традиционно считается, что, в отличие от Ni-Cd и Ni-MH аккумуляторов, Li-Ion аккумуляторы полностью избавлены от эффекта памяти. По результатам исследований учёных Института Пауля Шерера (Швейцария) в 2013 году этот эффект был таки обнаружен, но оказался ничтожен.[28]
Причиной его является то, что основой работы батареи являются процессы высвобождения и обратного захвата ионов лития, динамика которых ухудшается в случае неполной зарядки.[29] Во время зарядки ионы лития один за другим покидают частицы литий-феррофосфата, размер которых составляет десятки микрометров. Катодный материал начинает разделяться на частицы с разным содержанием лития. Заряжание батареи происходит на фоне возрастания электрохимического потенциала. В определённый момент он достигает предельного значения. Это приводит к ускорению высвобождения оставшихся ионов лития из катодного материала, но они уже не меняют суммарного напряжения батареи. Если батарея не будет полностью заряжена, то на катоде останется некоторое число частиц, близких к пограничному состоянию. Они практически достигли барьера высвобождения ионов лития, но не успели его преодолеть. При разряде свободные ионы лития стремятся вернуться на место и рекомбинировать с ионами феррофосфата. Однако на поверхности катода их также встречают частицы в пограничном состоянии, уже содержащие литий. Обратный захват затрудняется, и нарушается микроструктура электрода.
В настоящее время просматриваются два пути решения проблемы: внесение изменений в алгоритмы работы системы управления батареями и разработка катодов с увеличенной площадью поверхности.
Требования к режимам заряда/разряда[править | править код]
Глубокий разряд полностью выводит из строя литий-ионный аккумулятор. Также на жизненный цикл аккумуляторов влияет глубина его разряда перед очередной зарядкой и зарядка токами выше установленных производителем. Крайне чувствительны они и к напряжению зарядки. Если его повысить всего на 4 %, то аккумуляторы будут вдвое быстрее терять ёмкость от цикла к циклу. Ток зарядки зависит от разницы напряжений между аккумулятором и зарядным устройством и от сопротивления как самого аккумулятора, так и подводимых к нему проводов. Поэтому увеличение напряжения зарядки на 4 % может приводить к увеличению тока зарядки в 10 раз. Это отрицательно сказывается на аккумуляторе. Он может перегреваться и деградировать[30].
Старение[править | править код]
Литиевые аккумуляторы стареют, даже если не используются. Соответственно, нет смысла покупать аккумулятор «про запас» или чрезмерно увлекаться «экономией» его ресурса.
Оптимальные условия хранения Li-ion-аккумуляторов достигаются при 40-процентном заряде от ёмкости аккумулятора и температуре 0…10 °C:[31]
| Температура, ⁰C | С 40%-м зарядом, % за год | Со 100%-м зарядом, % за год |
|---|---|---|
| 0 | 2 | 6 |
| 25 | 4 | 20 |
| 40 | 15 | 35 |
| 60 | 25 | 40 % за три месяца |
Снижение ёмкости при низких температурах[править | править код]
Как и в других типах аккумуляторов, разрядка в условиях низких температур приводит к снижению отдаваемой энергии, в особенности при температурах ниже 0 ⁰C. Так, снижение запаса отдаваемой энергии при понижении температуры от +20 ⁰C до +4 ⁰C приводит к уменьшению отдаваемой энергии на ~5-7 %, дальнейшее понижение температуры разрядки ниже 0 ⁰C приводит к потере отдаваемой энергии на десятки процентов. Разряд аккумулятора при температуре не ниже, указанной производителем аккумуляторов, не приводит к их деградации (преждевременному исчерпанию ресурса). Химия литий-ионных аккумуляторов более чувствительна к температурам при зарядке АКБ, и оно оптимально при температурах ~ +20 ⁰C, а при температурах ниже +5 ⁰C не рекомендовано.[32]
Как и для других типов аккумуляторов, одним из вариантов решения проблемы являются аккумуляторы с внутренним подогревом.[33]
- ↑ А.М. Скундин, О.А. Брылев. Наноматериалы в современных химических источниках тока (неопр.). МГУ (2011).
- ↑ Татьяна Кулова. Аккумуляторы, изменившие жизнь // Наука и жизнь. — 2019. — № 12. — С. 2-7.
- ↑ Li-ion 4.35V vs 4.20V сколько теряем? Тест SANYO UR18650ZTA. / Зарядки, пауэрбанки, провода и переходники / iXBT Live (рус.). iXBT Live (26 августа 2018). Дата обращения 18 октября 2019.
- ↑ Топовые аккумуляторы 21700: LG M50 5000мАч vs Samsung 48G 4800мАч / Зарядки, пауэрбанки, провода и переходники / iXBT Live (рус.). iXBT Live (30 июня 2018). Дата обращения 18 октября 2019.
- ↑ Sony VTC6A и VTC6 с одинаковыми Matrix-кодами — результаты тестов (неопр.). www.ecigtalk.ru. Дата обращения 18 октября 2019.
- ↑ Н. Бровка, О. Янченков Применение специализированных микропроцессоров для построения схем контроля и защиты литий-ионных и литий-полимерных аккумуляторных батарей // Журнал «Компоненты и Технологии». — № 3, 2007 г. С. 132—135. ISSN 2079-6811.
- ↑ Обзор BMS контроллера заряда литий-ионных аккумуляторов 18650 3.7В на YouTube
- ↑ Сердечный Д. В., Томашевский Ю. Б. Управление процессом заряда многоэлементных литий-ионных аккумуляторных батарей / Научная статья // Журнал «Измерение. Мониторинг. Управление. Контроль». — № 3 (21), 2017 г. С. 115—123. УДК 621.314. DOI 10.21685/2307-5538-2017-3-16. ISSN 1999-5458.
- ↑ Сазонов И. Е., Лукьяненко М. В. Выравнивание заряда в литий-ионных аккумуляторных батареях / Научная статья // Сборник материалов IX Междунарародной научно-практической конференции, посвящённой Дню космонавтики]]. «Актуальные проблемы авиации и космонавтики» [Электронныйресурс]. Красноярск: СибГУ им. М. Ф. Решетнева — № 9, т. 1, 2013 г. С. 204. УДК 537.22. ISSN 1999-5458.
- ↑ [1].
- ↑ [2].
- ↑ [3].
- ↑ [4]
- ↑ [5]
- ↑ [6].
- ↑ [7].
- ↑ Возгорания на Dreamliner связаны с аккумуляторами
- ↑ Samsung отзывает Galaxy Note 7 из-за возможности возгорания
- ↑ Находившийся за рулем Tesla бывший агент ФБР погиб в ДТП
- ↑ Should You Be Worried About Your E-Cigarette Exploding?
- ↑ Лайнер экстренно сел из-за загоревшегося планшета Samsung
- ↑ Lithium Batteries as Cargo in 2016 Update III
- ↑ Bandhauer Todd M., Garimella Srinivas, Fuller Thomas F. A Critical Review of Thermal Issues in Lithium-Ion Batteries (англ.) // Journal of The Electrochemical Society. — 2011. — Vol. 158, no. 3. — P. R1. — ISSN 0013-4651. — DOI:10.1149/1.3515880. [исправить]
- ↑ Zaghib K., Dubé J., Dallaire A., Galoustov K., Guerfi A., Ramanathan M., Benmayza A., Prakash J., Mauger A., Julien C.M. Enhanced thermal safety and high power performance of carbon-coated LiFePO4 olivine cathode for Li-ion batteries (англ.) // Journal of Power Sources. — 2012. — December (vol. 219). — P. 36—44. — ISSN 0378-7753. — DOI:10.1016/j.jpowsour.2012.05.018. [исправить]
- ↑ http://www.powerinfo.ru/accumulator-liion.php
- ↑ Гореть, а не тлеть! Что на самом деле случилось с электроседаном Tesla Motors?
- ↑ Аспекты безопасности литий-ионных аккумуляторов
- ↑ Paul Scherrer Institut (PSI) :: Memory effect now also found in lithium-ion batteries (неопр.). Дата обращения 2 мая 2013. Архивировано 11 мая 2013 года.
- ↑ Экономия батареи на Андроид: советы и мифы | AndroidLime (неопр.). androidlime.ru. Дата обращения 29 февраля 2016.
- ↑ Мельничук О. В., Фетисов В. С. Особенности заряда и разряда литиевых аккумуляторных батарей и современные технические средства управления этими процессами / Научная статья // Журнал «Электротехнические и информационные комплексы и системы». — № 2, т. 12, 2016 г. С. 41-48. УДК 621.355.9. ISSN 1999-5458.
- ↑ 5 практических советов по эксплуатации литий-ионных аккумуляторов (рус.)
- ↑ Эксплуатация и хранение литий-ионных аккумуляторов (рус.)
- ↑ Независимая интернет-газета «Новый взгляд». 22.01.2016.Созданы литий-ионные аккумуляторы с подогревом
Электрический аккумулятор — это… Что такое Электрический аккумулятор?
{б{redirect|Аккумулятор|Аккумулятор (значения)}}

Электри́ческий аккумуля́тор — химический источник тока многоразового действия, основная специфика которого заключается в обратимости внутренних химических процессов, что обеспечивает его многократное циклическое использование (через заряд-разряд[1]) для накопления энергии и автономного электропитания различных электротехнических устройств и оборудования[2].
Принцип действия
 Замена аккумуляторной батареи на электропогрузчике
Замена аккумуляторной батареи на электропогрузчикеПринцип действия аккумулятора основан на обратимости химической реакции. Работоспособность аккумулятора может быть восстановлена путём заряда, то есть пропусканием электрического тока в направлении, обратном направлению тока при разряде.
Несколько аккумуляторов, объединённых в одну электрическую цепь, составляют аккумуля́торную батаре́ю.
Характеристики
Максимально возможный полезный заряд аккумулятора называется зарядной ёмкостью, или просто ёмкостью. Ёмкость аккумулятора — это заряд, отдаваемый полностью заряженным аккумулятором при разряде до наименьшего допустимого напряжения. В системе СИ ёмкость аккумуляторов измеряют в кулонах, на практике часто используется внесистемная единица — ампер-час. 1 А⋅ч = 3600 Кл.
Реже на аккумуляторах указывается энергетическая ёмкость — энергия, отдаваемая полностью заряженным аккумулятором при разряде до наименьшего допустимого напряжения. В системе СИ она измеряется в джоулях, на практике иногда используется внесистемная единица — ватт-час. 1 Вт⋅ч = 3600 Дж.
Электрические и эксплуатационные характеристики аккумулятора зависят от материала электродов и состава электролита. Сейчас наиболее распространены следующие аккумуляторы:
| Тип | ЭДС (В) | Область применения |
|---|---|---|
| свинцово-кислотные (Lead Acid) | 2,1 | троллейбусы, трамваи, воздушные суда, автомобили, мотоциклы, электропогрузчики, штабелеры, электротягачи, аварийное электроснабжение, источники бесперебойного питания |
| никель-кадмиевые (NiCd) | 1,2 | замена стандартного гальванического элемента, строительные электроинструменты, троллейбусы, воздушные суда |
| никель-металл-гидридные (NiMH) | 1,2 | замена стандартного гальванического элемента, электромобили |
| литий-ионные (Li‑ion) | 3,7 | мобильные устройства, строительные электроинструменты, электромобили |
| литий-полимерные (Li‑pol) | 3,7 | мобильные устройства, электромобили |
| никель-цинковые (NiZn) | 1,6 | замена стандартного гальванического элемента |
По мере исчерпания химической энергии напряжение и ток падают, аккумулятор перестаёт действовать. Зарядить аккумулятор (батарею аккумуляторов) можно от любого источника постоянного тока с бо́льшим напряжением при ограничении тока. Стандартным считается зарядный ток (в амперах) в 1/10 номинальной ёмкости аккумулятора (в ампер⋅часах). Многие типы аккумуляторов имеют различные ограничения, которые необходимо учитывать при зарядке и последующей эксплуатации, например NiMH-аккумуляторы чувствительны к перезаряду, литиевые — к переразряду, напряжению и температуре. NiCd- и NiMH-аккумуляторы имеют так называемый эффект памяти, заключающийся в снижении ёмкости, в случае когда зарядка осуществляется при не полностью разряженном аккумуляторе. Также эти типы аккумуляторов обладают заметным саморазрядом, то есть они постепенно теряют заряд, даже не будучи подключенными к нагрузке. Для борьбы с этим эффектом может применяться капельная подзарядка.
Типы аккумуляторов
См. также
Примечания
Ссылки
Зарядное устройство — Википедия
Материал из Википедии — свободной энциклопедии
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 7 июня 2015; проверки требуют 72 правки. Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 7 июня 2015; проверки требуют 72 правки. Бытовые внешние зарядные устройства и электробритва с встроенным зарядным устройствомЗарядное устройство (ЗУ; разг. зарядка) — электронное устройство для заряда электрических аккумуляторов и аккумуляторных батарей энергией внешнего источника; как правило, — от сети переменного тока.
Включает в себя преобразователь напряжения (трансформатор или импульсный блок питания), выпрямитель, стабилизатор напряжения, и по необходимости устройство контроля процесса заряда, средства индикации (стрелочный или светодиодный амперметр/вольтметр).
Характеристики зарядных устройств зависят от типа аккумуляторов, рабочего напряжения, номинальной ёмкости.
Зарядные устройства могут быть встроенными и внешними.
Зарядные и пуско-зарядные устройства аккумуляторов автомобиля[править | править код]
Зарядные устройства автомобильных аккумуляторных батарей являются внешними, запитываются от сети 220—230 В переменного тока штепсельным разъёмом и снабжены зажимами-крокодилами для присоединения к клеммам аккумуляторной батареи.
Пуско-зарядное устройство (ПЗУ) для автомобильных аккумуляторных батарей используется не только для зарядки автомобильных аккумуляторных батарей, но также и для запуска автомобильного двигателя электрическим стартером при севшем батарее (без предварительной полной зарядки самой батареи). При этом может использоваться как методика пуска двигателя с предварительной частичной подзарядкой штатной аккумуляторной батареи в течение нескольких минут, так и запуск двигателя при полном разряде штатной батареи с немедленным запуском. Запуск достигается за счёт возможности ПЗУ выдавать в несколько раз бо́льший ток, чем просто зарядное устройство (ЗУ — предназначенное только для зарядки аккумуляторной батареи). Как следствие, ПЗУ обладает существенно бо́льшей массой и габаритами, нежели простое зарядное устройство.
Необходимый ток для запуска двигателя внутреннего сгорания должен в моменте достигать значений 100—1000 А[1][неавторитетный источник?]. Поэтому первые советские пуско-зарядные устройства обладали способностью давать ток только в нижнем пределе потребностей[источник не указан 2255 дней]. С появлением электрических приборов и сетей, способных использовать токи не 6 А, а 16 А, выходной ток пуско-зарядных устройств мог быть увеличен со 100 А до 290 А.
Маркировка зарядных устройств для зарядки автомобильных аккумуляторов[править | править код]
А В/С, где А — название зарядного устройства, В — максимальная ёмкость аккумуляторной батареи в А⋅ч, который целесообразно заряжать этим зарядным устройством, С — максимальное значение напряжения аккумуляторной батареи, который целесообразно заряжать этим зарядным устройством.
При превышении параметра В значения 170 А зарядное устройство может быть использовано не только для зарядки, но и для помощи при запуске двигателя.
Автоматическое зарядное устройство позволяющее проводить десульфатацию автомобильных аккумуляторных батарей
Зарядно-пусковое устройство позволяющее заводить автомобиль «прикуриванием»
Автоматическое зарядное устройство для автомобильных аккумуляторных батарей со светодиодной индикацией
-

Зарядное устройство с возможностью автоматического режима зарядки и ручного управления зарядкой
Зарядные устройства литиевых аккумуляторов[править | править код]
Зарядные устройства для литий-ионных и литий-полимерных аккумуляторов имеют свои особенности, поскольку перезаряд и глубокий разряд может привести к выходу аккумулятора из строя. Основной способ заряда литий-ионных и литий-полимерных аккумуляторов, рекомендуемый производителями, это заряд постоянным током с контролем тока заряда и напряжения на выводах аккумулятора. Для этого предназначены специализированные, зачастую встроенные в аппаратуру зарядные устройства с использованием специализированных контроллеров[2].
-

Зарядное устройство для заряжания 7,2 В литий-ионной аккумуляторной батареи видеокамеры
Зарядное устройство для заряжания 3,7 В литий-ионного аккумулятора типоразмера 18650 от 5 В USB-порта вмонтировано в фонарик в котором он используется
Беспроводное зарядное устройство / Индукционное зарядное устройство[3][4] применяется, с конца 2000-х годов, во многих мобильных устройствах.
Также применяется на электротранспорте.
Промышленные зарядные устройства представляют собой блоки с электронной аппаратурой, размещаемые в цехе зарядной станции (или специализированном помещении). Такая аппаратура предназначена для одновременного обслуживания нескольких аккумуляторных батарей и позволяет выполнять различные долговременные операции (заряд-разряд, заряд импульсными токами), в том числе и в автоматическом режиме.
-

Зарядная станция свинцово-кислотных аккумуляторных батарей
Зарядное устройство электробуса для подзарядки аккумуляторных батарей на остановке
Зарядные станции аккумуляторов портативных радиостанций
Зарядный автомат для мобильных устройств
Общественное зарядное устройство с USB-разъёмами вмонтированное в панель с картой на станции метрополитена
-

Зарядное устройство с USB-разъёмами вмонтированное в поручень автобуса
- Зарядные устройства портативных и мобильных устройств
-

Зарядное устройство (блок питания) сотового телефона ограниченное разъёмом подключаемого устройства для зарядки, выдаваемым напряжением и силой тока на которую рассчитано
-

Зарядное устройство для плоских 3,7 В литий-ионных аккумуляторов телефонов и других устройств ограниченное производителем расположением контактных площадок и размерами аккумулятора для заряжания которых рассчитан
-

На переднем плане 2 аккумуляторные батареи фотоаппарата и зарядное устройство к ним
-

Устройство платы зарядного устройства «Canon CB2LTE»
Устройство зарядного устройства «Bosch AL1105CV»
- Зарядные устройства типовых аккумуляторов
Зарядное устройство со светодиодной индикацией, для заряжания аккумуляторов типоразмеров AA, AAA и аккумуляторных батарей типа «Крона»
-

Автоматическое цифровое «интеллектуальное» 4-х канальное зарядное устройство для зарядки разных типоразмеров цилиндрических аккумуляторов с возможностью корректировки процесса заряда
-

Портативное зарядное устройство для 2-х аккумуляторов типоразмера АА с питанием от USB-порта
Аккумуляторы типоразмера АА со встроенной платой обеспечивающей зарядку от USB-порта
- Универсальные и USB зарядные устройства
Универсальное зарядное устройство для заряжания малогабаритных аккумуляторов и аккумуляторных батарей разного типа и формфактора с автоматической и ручной предустановкой режимов заряда
-

Универсальное зарядное устройство типа «лягушка» для заряжания плоских с разными размерами и расположением контактных площадок литий-ионных аккумуляторов телефонов, фотоаппаратов и других устройств
-

USB-зарядное устройство (блок питания) встроенное в электророзетку выдающее стандартное для USB 5 В напряжение питания
-

Универсальное зарядное устройство (блок питания) с USB-выходом подключаемое к сети 220 В, непосредственно управление зарядки осуществляет само мобильное устройство в котором установлен аккумулятор
Пример устройства зарядного устройства (блока питания) с USB-выходом
Пример автомобильного зарядного устройства (блока питания) с 2 USB-выходами подключаемого в гнездо прикуривателя
- Внешние аккумуляторы (портативные автономные блоки питания)
Устройство простейшего повер-банка с USB-гнездом, платой-преобразователем и литий-ионным аккумулятором типоразмера 18650
-

Повер-банк с 2-мя никель-металл-гидридными аккумуляторами типоразмера АА с возможностью их подзарядки встроенной солнечной батареей
-

Переносная солнечная батарея для зарядки мобильных устройств и встроенного аккумулятора
-

Универсальный повер банк с 5 USB-портами и несколькими напряжениями питания устройств
Накопление энергии — Википедия

Накопление энергии — аккумуляция энергии для её использования в дальнейшем. Устройство, хранящее энергию, обычно называют аккумулятором или батареей. Типичным примером устройства накопления энергии (энергонакопителя) является аккумуляторная батарея, в которой хранится химическая энергия, легко преобразуемая в электричество для работы мобильного телефона. Менее очевидный пример — гидроэлектростанция: вода в резервуаре выступает в качестве источника потенциальной энергии гравитации. Ископаемые виды топлива, такие как уголь, нефть и газ, также являются накопителями энергии, полученной в свое время от солнечного света живыми организмами, которые со временем и превратились в эти виды топлива.
Новейшая история[править | править код]
В двадцатом веке электричество вырабатывалось, прежде всего, за счет сжигания ископаемого топлива. Проблемы с транспортировкой энергии, загрязнением воздуха и глобальным потеплением к росту использования возобновляемых источников энергии — таких, как солнечная энергия и энергия ветра. Энергия ветра зависит от климатических условий и погоды. Солнечная энергия зависит от географического положения, облачного покрова. Она доступна только в дневное время, в то время, как спрос зачастую достигает пика после захода солнца. Интерес к накоплению энергии из этих источников растет, поскольку именно они в последнее время генерируют всё большую часть мирового энергопроизводства.
Использование электричества вне электросетей в XX веке было нишевым рынком, но в XXI веке оно значительно расширилось. Портативные устройства используются во всем мире. Солнечные батареи получают все более широкое распространение в сельской местности. Доступ к электричеству теперь является вопросом экономики, а не местоположения. Однако в энергоснабжении транспорта сжигание топлива по-прежнему преобладает.
Схема[править | править код]
См. также: Схема аккумулирования энергии
Следующий список включает виды аккумулирования энергии:
- Хранение ископаемого топлива
- Механическое
- Электрический, электромагнитный
- Биологический
- Электрохимический (Система накопления энергии Батареи, BESS)
- Тепловой
- Тепловой аккумулятор
- Криогенные системы хранения, Аккумулирование энергии жидкого воздуха (LAES)
- Криогенный двигатель Дэрмана
- Эвтектическая система
- Кондиционер хранения льда
- Соль в качестве накопителя энергии
- Фазовый переход вещества
- Сезонное хранение тепловой энергии
- Солнечный водоем
- Паровой аккумулятор
- Хранение тепловой энергии (Общее)
Механическое накопление[править | править код]
Энергия может сохраняться в воде, перекачиваемой на большую высоту с использованием накачки или путем перемещения твердого вещества в более высокие места (гравитационные батареи). Другие механические методы предполагают сжатие воздуха и маховиков, которые преобразуют электрическую энергию в кинетическую, а возвращая её, когда потребность в электричестве достигает пика.
Гидроэлектричество[править | править код]
Основная статья: Гидроэлектростанция
Гидроэлектростанции с водохранилищами могут эксплуатироваться для обеспечения электроэнергией в периоды пикового спроса. Вода хранится в резервуаре в периоды низкой потребности и высвобождается при высокой потребности. Эффект аналогичен накоплению с перекачкой, но без сопутствующих потерь. Хотя гидроэлектростанция напрямую не накапливает энергию из других источников, она ведет себя эквивалентно, снижая выработку в период избытка электроэнергии, полученной из других источников. В этом режиме плотины являются одной из наиболее эффективных форм аккумулирования энергии, поскольку меняются только сроки её генерации. Гидроэлектрические турбины имеют время запуска порядка нескольких минут[1].
Гидроаккумулирующая электростанция[править | править код]
Основная статья: Гидроаккумулирующая электростанция
Во всем мире гидроаккумулирующая электростанция (ГАЭС) является наиболее крупной формой накопления энергии в больших масштабах. Энергетическая эффективность ГАЭС варьируется, на практике, от 70 % до 80 %[2][3][4][5].
В периоды низкой потребности в электроэнергии, избыточная генерирующая мощность используется для перекачки воды из более низкого резервуара в более высокий. Когда спрос растет, вода поступает обратно в нижний резервуар (или водный путь/водоем) через турбину, вырабатывающую электричество. Реверсивные турбогенераторные узлы действуют как насос и турбина (обычно это турбина Фрэнсиса). Почти все подобные сооружения используют перепад высот между двумя водоемами. Насосно-накопительные установки «в чистом виде» перемещают воду между резервуарами, в то время как подход с «откачкой» представляет собой комбинацию насосных хранилищ и обычных гидроэлектростанций, использующих естественное течение воды.
Технология накопления энергии сжатого воздуха[править | править код]
Пневматический аккумулятор использует избыточную энергию для сжатия воздуха для последующего производства электроэнергии. Сжатый воздух хранится в подземном резервуаре[6].
Пневматический аккумулятор может преодолеть разрыв между волатильностью производства и нагрузкой. Пневматический аккумулятор удовлетворяет потребности потребителей в энергии, эффективно обеспечивая доступную энергию для удовлетворения спроса. Возобновляемые источники энергии, такие как энергия ветра и солнца, имеют переменные ресурсы. В результате, добавление других видов энергии необходимо для удовлетворения спроса на энергию в периоды снижения доступности возобновляемых ресурсов. Установки для хранения энергии на сжатом воздухе способны аккумулировать избыточную энергию от возобновляемых источников энергии во время перепроизводства энергии. Эта накопленная энергия может быть использована, когда спрос на электроэнергию увеличивается или доступность энергетических ресурсов уменьшается.
Сжатие воздуха создает тепло: при сжатии воздух теплеет. Расширение, со своей стороны требует тепловой энергии. Если не добавлять дополнительной энергии, воздух после расширения будет намного холоднее. Если тепло, выделяемое во время сжатия, может аккумулироваться и использоваться во время расширения, эффективность значительно повышается[7].
Технология накопления энергии маховиком[править | править код]
см. также: супермаховик, маховик
Накопитель энергии маховика (FES) работает за счет ускорения ротора (маховика) до очень высокой скорости, аккумулируя энергию вращения. Когда энергия извлекается, скорость вращения маховика уменьшается; добавление энергии соответственно приводит к увеличению скорости маховика.
Большинство систем FES используют электричество для ускорения и замедления маховика, но рассматриваются и устройства, которые непосредственно используют механическую энергию[8].
Системы FES имеют роторы, изготовленные из высокопрочных углеродно-волокнистых композитов, подвешенных на магнитных подшипниках и вращающихся со скоростью от 20000 до более 50000 об/мин в вакуумном корпусе. Такие маховики могут достигать максимальной скорости («заряда») за считанные минуты. Система маховика соединена с комбинированным электродвигателем / генератором.
Системы FES имеют относительно долгий срок службы (длятся десятилетия, практически не требуя технического обслуживания[9]; срок службы полного цикла, указанный для маховиков, варьируется от 10 5 до 10 7 циклов использования), высокая удельная энергия (100—130 Вт · ч/кг или 360—500 кДж/кг) и удельная мощность[10].
Накопление гравитационной потенциальной энергии твердых масс[править | править код]
Изменение высоты твердых масс может накапливать или выделять энергию через подъемную систему, приводимую в движение электродвигателем / генератором.
Методы включают использование рельсов[11][12] и кранов[13] для перемещения бетонных грузов вверх и вниз, использование высотных плавучих платформ на солнечных батареях, поддерживающих лебедки для подъёма и опускания твердых масс.
Накопление тепловой энергии[править | править код]
Аккумулирование тепловой энергии (TES) — это временное хранение или отвод тепла.
Аккумулированная тепловая энергия[править | править код]
Аккумулирование тепла использует преимущества нагрева материала для накопления энергии.
Технологии сезонного накопления тепловой энергии (СНТЭ) позволяют использовать тепло или холод спустя месяцы после того, как оно было получено из природных источников или отходов. Аккумуляция может происходить в водоносных слоях, скоплениях скважин в геологических субстратах, таких как песок или кристаллические породы, в выстланных ямах, заполненных гравием и водой, или в заполненных водой шахтах. Технологии СНТЭ часто имеют срок окупаемости в диапазоне от четырёх до шести лет. Примером является сообщество солнечных батарей Drake Landing в Канаде, для которого 97 % круглогодичного тепла обеспечивается солнечно-тепловыми коллекторами на крышах гаражей, а скважинный накопитель тепловой энергии (СНТЭ) является поддерживающей технологией[14]. В Браструпе (Дания) система коммунального солнечного теплоснабжения, также использует СНТЭ при температуре хранения 65° C (149° F). Тепловой насос, который работает только при наличии избыточной энергии ветра в единой энергосети, используется для повышения температуры до 80° C (176° F) для распределения. Когда избыточного электричества, генерируемого ветром, нет, используется газовый котел. 20 % процентов тепла Браструпа имеют солнечное происхождение.[15]
Скрытое накопление тепловой энергии[править | править код]
Скрытые тепловые системы накопления тепловой энергии работают с материалами с высокой скрытой теплоемкостью, известными как материалы с фазовым переходом (PCM). Основным преимуществом этих материалов является то, что их скрытая теплоемкость гораздо больше, чем ощутимое тепло. В определённом температурном диапазоне фазовый переход от твердого к жидкому поглощает большое количество тепловой энергии для последующего использования.
Скрытое накопление тепловой энергии представляет собой процесс, посредством которого энергия в форме тепла либо поглощается, либо выделяется во время фазового перехода материала (PCM). Изменение фазы — это плавление или затвердевание материала. Во время изменения фазы PCM обладает способностью поглощать большое количество энергии из-за высокой температуры плавления.
Электрохимический[править | править код]
Аккумуляторная батарея[править | править код]
Аккумуляторная батарея содержит один или несколько электрохимических элементов. Аккумуляторы бывают разных форм и размеров, от кнопок до мегаваттных энергосистем.
Аккумуляторные батареи имеют более низкие общую стоимость использования и уровень воздействия на окружающую среду, чем неперезаряжаемые (одноразовые) батареи. Некоторые типы аккумуляторных батареек доступны в тех же форматах, что и одноразовые. Аккумуляторные имеют более высокую начальную стоимость, но их можно очень дёшево перезаряжать и использовать много раз.
Общие химические составы аккумуляторной батареи:
- Свинцово-кислотные аккумуляторы: свинцово-кислотные аккумуляторы занимают самую большую долю рынка аккумуляторов. В заряженном состоянии отрицательный электрод из металлического свинца и положительный электрод из сульфата свинца погружают в электролит с разбавленной серной кислотой (H 2 SO 4). В процессе разряда электроны выталкиваются из ячейки, так как на отрицательном электроде образуется сульфат свинца, а электролит восстанавливается до воды.
- Технология свинцово-кислотных аккумуляторов получила широкое развитие. Эксплуатация требует минимального труда, его стоимость низкая. Доступная энергетическая ёмкость батареи подвержена быстрой разрядке, что приводит к малому сроку службы и низкой плотности энергии[16].
Проточная батарея[править | править код]
Проточная батарея работает, пропуская раствор через мембрану, где происходит обмен ионов для зарядки / разрядки элемента. Напряжение тока химически определено уравнением Нернста, и на практике составляет от 1,0 до 2,2 В. Ёмкость накопителя зависит от объёма ёмкостей, в которых находится раствор.
Проточная батарея технически близка как топливному элементу, так и элементу электрохимического аккумулятора. Коммерческие приложения предназначены для длительного полупериода хранения, например, для резервного энергоснабжения.
Суперконденсатор[править | править код]
Основная статья: Суперконденсатор
Суперконденсаторы, также называемые электрическими двухслойными конденсаторами (EDLC) или ультраконденсаторами, являются общими терминами для семейства электрохимических конденсаторов, которые не имеют обычных твердых диэлектриков. Ёмкость определяется двумя параметрами аккумуляции: двухслойная емкость и псевдоёмкость[17][18].
Суперконденсаторы ликвидируют разрыв между обычными конденсаторами и аккумуляторными батареями. Они хранят наибольшее количество энергии на единицу объёма или массы (плотности энергии) среди конденсаторов. Они поддерживают до 10 000 фарад / 1,2 В[19], до 10 000 раз больше, чем у электролитических конденсаторов, но выдают или принимают менее половины мощности в единицу времени (плотность мощности)[20].
В то время, как суперконденсаторы имеют удельную энергию и удельные плотности энергии примерно 10 % в сравнении с батареями, их плотность мощности обычно в 10-100 раз больше. Это приводит к гораздо более коротким циклам зарядки / разрядки. Кроме того, они будут выдерживать гораздо больше циклов зарядки и разрядки, чем батареи.
Суперконденсаторы поддерживают широкий спектр применений, включая:
- Низкий ток питания для резервного копирования памяти в статической оперативной памяти (SRAM)
- Питание для автомобилей, автобусов, поездов, кранов и лифтов, в том числе рекуперация энергии при торможении, кратковременное накопление энергии и подача питания в импульсном режиме
Другие химические вещества[править | править код]
Технология Power-to-Gas (P2G)[править | править код]
Технология Power-to-Gas — это технология, которая преобразует электричество в газообразное топливо, к примеру, водород или метан. Известны три метода использования электричества для превращения воды в водород и кислород посредством электролиза.
При первом методе водород впрыскивается в сеть природного газа. Второй метод заключается в реакции водорода с диоксидом углерода для получения метана, с использованием реакции метанирования (такой, как реакция Сабатье) или биологического метанирования, что приводит к дополнительной потере преобразования энергии на 8 %. Затем метан можно подавать в природную газовую сеть. Третий метод использует выходной газ из генератора древесного газа или биогазовой установки после того, как модификатор биогаза смешан с водородом из электролизера, чтобы улучшить качество биогаза.
Водород[править | править код]
Основная статья: Хранение водорода
Водород тоже можно рассматривать как накопитель энергии: электричество в этом случае производится посредством водородного топливного элемента.
Для синтеза килограмма водорода требуется около 50 кВт⋅ч (180 МДж) солнечной энергии, поэтому стоимость электроэнергии является критически важной.
Подземное хранение водорода производится в подземных пещерах, соляных куполах и истощенных нефтяных и газовых месторождениях.[21]Imperial Chemical Industries в течение многих лет хранит в подземных пещерах большие количества газообразного водорода без каких-либо проблем. Европейский проект Hyunder указал в 2013 году, что для аккумуляции энергии ветра и солнца с использованием подземного водорода потребует 85 пещер.
Метан[править | править код]
Основная статья: Синтетический природный газ
Метан — простейший углеводород с молекулярной формулой СН 4. Метан легче хранить и транспортировать, чем водород. Имеется полноценная инфраструктура его хранения и сжигания (трубопроводы, газометры, электростанции).
Синтетический природный газ (синтез-газ или SNG) может быть создан в многоступенчатом процессе, начиная с водорода и кислорода. Водород реагирует с диоксидом углерода в реакции Сабатье, производя метан и воду. Метан может храниться, а затем использоваться для производства электроэнергии. Полученная вода рециркулируется, уменьшая потребность во внешних её источниках. На стадии электролиза, кислород сохраняется для сжигания метана в чистой кислородной среде на соседней электростанции.
При сгорании метана образуются углекислый газ (CO2) и вода. Диоксид углерода может быть переработан для ускорения процесса Сабатье, а вода может быть переработана для дальнейшего электролиза. Производство метана, хранение и сгорание перерабатывают продукты реакции.
Биотопливо[править | править код]
Основная статья: Биотопливо
Ископаемое топливо могут заменять различные виды биотоплива, такие как биодизельное топливо, растительное масло, спиртовое топливо или биомасса. Химические процессы могут превращать углерод и водород (в составе угля, природного газа, растительной и животной биомассы и органических отходов), в простые углеводороды, подходящие в качестве замены для традиционных углеводородных видов топлива. Примерами являются дизельное топливо Фишера-Тропша, метанол, диметиловый эфир и синтез-газ. Этот источник дизельного топлива широко использовался во время Второй мировой войны в Германии, которая столкнулась с ограниченным доступом к поставкам сырой нефти. По тем же причинам Южная Африка производит большую часть дизельного топлива из угля.
Алюминий[править | править код]
Рядом исследователей в качестве энергонакопителя был предложен алюминий. Электрохимический эквивалент алюминия почти в четыре раза больше, чем у лития. Энергия может извлекаться из алюминия путем его взаимодействия с водой с образованием водорода. Однако для реакции с водой алюминий должен быть отделен от его естественного оксидного слоя. Это процесс, который требует измельчения, а также химических реакций с едкими веществами или сплавами. Побочным продуктом реакции с образованием водорода является оксид алюминия, который может быть переработан обратно в алюминий в рамках процесса Холла-Херулта, делая реакцию теоретически возобновляемой. Если процесс Холла-Херулта запускается с использованием солнечной или ветровой энергии, алюминий может использоваться для хранения энергии, причем у такого процесса эффективность более высока, чем при прямом солнечном электролизе[22].
Бор, кремний и цинк[править | править код]
В качестве альтернативных накопителей энергии рассматриваются также бор[23], кремний и цинк[24].
Другие химические вещества[править | править код]
Органическое соединение норборнадиен, в реакции превращения в квадрицикл, при воздействии света, сохраняет солнечную энергию, в форме энергии химических связей. Функционирующий образец был разработана в Швеции и позиционируется как молекулярная солнечная тепловая система[25].
Электрические методы[править | править код]
Конденсатор[править | править код]
Основная статья: Электрический конденсатор
Конденсатор — это пассивный двухполюсный электрический компонент, используемый для электростатического накопления энергии. На практике конденсаторы сильно различаются, но все они содержат, по меньшей мере, два электрических проводника (пластины), разделенных диэлектриком (изолятором). Конденсатор может накапливать электрическую энергию, когда он отключен от своей зарядной цепи, поэтому его можно использовать как временную батарею или как другие виды перезаряжаемой системы накопления энергии. Конденсаторы обычно используются в электронных устройствах для поддержания питания при замене батарей (это предотвращает потерю информации в энергозависимой памяти). В среднем конденсаторы имеют плотность менее 360 джоулей на килограмм, в то время как у обычной щелочной батареи этот параметр составляет порядка 590 кДж / кг.
Конденсаторы накапливают энергию в электростатическом поле между пластинами. Благодаря разности потенциалов на проводниках (например, когда конденсатор присоединен к батарее), электрическое поле проходит через диэлектрик, заставляя положительный заряд (+Q) собираться на одной пластине и отрицательном заряде (-Q) на другой пластине. Если аккумулятор подключен к конденсатору в течение достаточного времени, через конденсатор не может протекать ток. Однако если через выводы конденсатора подается напряжение, может возникать ток смещения.
На практике диэлектрик между пластинами пропускает небольшое количество тока в виде утечки и имеет предел напряженности электрического поля, известный как напряжение пробоя. Однако эффект восстановления диэлектрика после пробоя высокого напряжения может привести к созданию нового поколения самовосстанавливающихся конденсаторов[26][27].
Сверхпроводящие индуктивные накопители[править | править код]
Система хранения сверхпроводящей магнитной энергии — сверхпроводящий индуктивный накопитель (СПИН) хранит энергию в магнитном поле, создаваемом потоком постоянного тока в сверхпроводящей катушке, которая была охлаждена до температуры ниже её сверхпроводящей критической температуры. Типичная система СПИН включает в себя сверхпроводящую катушку, систему кондиционирования и холодильник. Как только сверхпроводящая катушка заряжена, ток не распадается, и магнитная энергия может храниться бесконечно долго.
Накопленная энергия может быть передана в сеть путем разрядки катушки. Соответствующий инвертор / выпрямитель обеспечивает примерно 2-3 % потерь энергии в каждом направлении. СПИН теряет наименьшее количество электроэнергии в процессе накопления энергии, по сравнению с другими методами хранения энергии.
Из-за энергетических требований охлаждения и стоимости сверхпроводящего провода, СПИН используется для кратковременного хранения, например, для улучшения качества электроэнергии Эта система хранения применяется так же в балансировке сетки.
Мельницы[править | править код]
Классическим применением накопления энергии до промышленной революции было управление водными путями для приведения в действие водяных мельниц для обработки зерна или приводной техники. Сложные системы водохранилищ и плотин были построены, чтобы хранить и выпускать воду (и потенциальную энергию, которую она содержит), когда требуется.
Домашнее накопление энергии[править | править код]
Ожидается, что накопление энергии в домашних условиях станет все более распространенным явлением, учитывая растущую важность распределенного производства возобновляемых источников энергии (особенно фотоэлектрических) и значительную долю потребления энергии в жилых зданиях[28]. Чтобы повысить самообеспеченность (самостоятельность) на 40 % в доме, оборудованном фотоэлектрическими приборами, необходимо накопление энергии[28]. некоторые производители производят аккумуляторные батареи для хранения энергии, как правило, для удержания избыточной энергии солнечной/ветровой генерации. Сегодня для хранения энергии в домашних условиях литий-ионные аккумуляторы предпочтительнее свинцово-кислотных, учитывая их аналогичную стоимость, но гораздо более высокую производительность[29].
Tesla Motors выпускает две модели Tesla Powerwall. Одна из них представляет собой версию на 10 кВт⋅ч в неделю, а другая — версию на 7 кВт⋅ч для применения с ежедневным циклом[30]. В 2016 году ограниченная версия, Telsa Powerpack 2, стоила 398 долларов США / кВт⋅ч для хранения электроэнергии, стоимостью 12,5 цента / кВт⋅ч (средняя цена на энергосистему США), что положительно сказывалось на рентабельности инвестиций, если цены на электроэнергию не превышали 30 центов / кВт⋅ч[31].
Компания Enphase Energy анонсировала интегрированную систему, которая позволяет домашним пользователям хранить, контролировать и управлять электроэнергией. Система сохраняет 1,2 кВт⋅ч энергии и 275 Вт / 500 Вт выходной мощности[32].
Аккумуляция энергии ветра или солнца с использованием накопителя тепловой энергии, хотя и менее гибкое, значительно дешевле, чем батареи. Простой 52-галлонный электрический водонагреватель может хранить примерно 12 кВт⋅ч энергии для добавления горячей воды или отопления помещения[33].
Электросеть и электростанции[править | править код]
Накопление возобновляемой энергии[править | править код]
Самый большой запас возобновляемой энергии предоставляется сейчас гидроэлектростанциями. Большое водохранилище около гидроэлектростанции может хранить достаточно воды, чтобы усреднить годовой сток реки между сухим и влажным сезонами. Хотя гидроэлектростанция не накапливает напрямую энергию от прерывистых источников, она уравновешивает энергосистему, удерживая воду, когда энергия генерируется солнечным или ветровым излучением.
Важнейшее направление накопления энергии — гидроаккумулирующие электростанции. Такие регионы, как Норвегия, Уэльс, Япония и США эксплуатируют географические особенности, используя электрические насосы для заполнения резервуаров. При надобности вода проходит через генераторы и преобразует гравитационный потенциал падающей воды в электричество[34].
Среди видов энергонакопителей, используемых при производстве электроэнергии, следует отметить гидроэлектростанции с насосным накопителем, аккумуляторные батареи, тепловые энергонакопители (включая расплавленные соли), которые могут эффективно хранить и высвобождать очень большое количество тепловой энергии[35], и хранилища энергии сжатого воздуха, маховики, криогенные системы и сверхпроводящие магнитные катушки.
Избыточная мощность также может быть преобразована в метан (реакция Сабатье) с запасом в сети природного газа[36][37].
В 2011 году Администрация энергетики Бонневилля (северо-запад США) разработала экспериментальную программу по поглощению избыточного ветра и гидроэнергии, генерируемых ночью или во время штормовых периодов, сопровождаемых сильными ветрами. При наличии центрального управления бытовые приборы поглощают избыточную энергию, нагревая керамический кирпич в специальных обогревателях до сотен градусов и повышая температуру в резервуарах с подогревом горячей воды. После зарядки приборы обеспечивают отопление дома и подачу горячей воды по мере надобности. Экспериментальная система была создана с учётом последствий сильного шторма 2010 года, который довел ситуация до перепроизводства возобновляемой энергии а такой степени, что все обычные источники энергии были закрыты, или в случае АЭС — редуцированы до минимально возможного рабочего уровня, оставляя большую область почти полностью на возобновляемых источниках энергии.
Ещё один продвинутый метод, который использовался в бывшем проекте Solar Two в Соединенных Штатах и Solar Tres Power Tower в Испании, использует расплавленную соль для хранения тепловой энергии, получаемой от солнца, а затем преобразует её и отправляет в виде электрической энергии. Система перекачивает расплавленную соль через башню или другие специальные трубопроводы, которые нагреваются солнцем. Изолированные резервуары хранят раствор. Электричество производится путем превращения воды в пар, который подается в турбины.
- ↑ Robert A. Huggins. Energy Storage. — Springer Science & Business Media, 2010-09-01. — 424 с. — ISBN 9781441910233.
- ↑ Packing some power // The Economist. — 2012-03-03. — ISSN 0013-0613.
- ↑ Packing some power // The Economist. — 2012-03-03. — ISSN 0013-0613.
- ↑ Wayback Machine (неопр.). web.archive.org (1 августа 2014). Дата обращения 16 марта 2019.
- ↑ Wayback Machine (неопр.). web.archive.org (5 сентября 2012). Дата обращения 16 марта 2019.
- ↑ Wald, Matthew L.. Pushed Along by Wind, Power Storage Grows (англ.), The New York Times (27 июля 2010). Дата обращения 16 марта 2019.
- ↑ Gies, Erica. A Storage Solution Is in the Air (англ.), The New York Times (1 октября 2012). Дата обращения 16 марта 2019.
- ↑ Wayback Machine (неопр.). web.archive.org (16 мая 2011). Дата обращения 16 марта 2019.
- ↑ Flywheels: Spinning into Control (англ.). sciencewriter.org (22 August 2010). Дата обращения 16 марта 2019.
- ↑ Next-gen Of Flywheel Energy Storage | Product Design and Development (неопр.). web.archive.org (10 июля 2010). Дата обращения 16 марта 2019.
- ↑ Nathanael Massey,ClimateWire. Energy Storage Hits the Rails Out West (англ.). Scientific American. Дата обращения 16 марта 2019.
- ↑ Energy-Storing Train Gets Nevada Approval (англ.). Fortune. Дата обращения 16 марта 2019.
- ↑ Akshat Rathi, Akshat Rathi. Stacking concrete blocks is a surprisingly efficient way to store energy (англ.). Quartz. Дата обращения 16 марта 2019.
- ↑ Wayback Machine (неопр.). web.archive.org (4 марта 2016). Дата обращения 16 марта 2019.
- ↑ Braedstrup Solar Park in Denmark is now a reality! (неопр.). web.archive.org (26 января 2013). Дата обращения 16 марта 2019.
- ↑ Liangzhong YAO, Bo YANG, Hongfen CUI, Jun ZHUANG, Jilei YE. Challenges and progresses of energy storage technology and its application in power systems (англ.) // Journal of Modern Power Systems and Clean Energy. — 2016-10-01. — Vol. 4, iss. 4. — P. 519–528. — ISSN 2196-5420. — DOI:10.1007/s40565-016-0248-x.
- ↑ ScienceDirect (неопр.). www.sciencedirect.com. Дата обращения 16 марта 2019.
- ↑ Сосенкин В.е, Михалин А.а, Вольфкович Ю.м, Бограчев Д.а. УГЛЕРОДНЫЕ ЭЛЕКТРОДЫ С БОЛЬШОЙ ПСЕВДОЕМКОСТЬЮ ДЛЯ СУПЕРКОНДЕНСАТОРОВ // Электрохимия. — 2012. — Т. 48, вып. 4. — ISSN 0424-8570.
- ↑ Capacitor cells — ELTON (неопр.). web.archive.org (23 июня 2013). Дата обращения 16 марта 2019.
- ↑ B. E. Conway. Electrochemical Supercapacitors: Scientific Fundamentals and Technological Applications. — Springer US, 1999-04-30. — 734 с. — ISBN 9780306457364.
- ↑ (PDF) Sustainable transportation based on electric vehicle concepts: A brief overview (англ.). ResearchGate. Дата обращения 16 марта 2019.
- ↑ Current Efficiency, Specific Energy Consumption, Net Carbon Consumption — The Aluminum Smelting Process (неопр.). www.aluminum-production.com. Дата обращения 16 марта 2019.
- ↑ Boron: A Better Energy Carrier than Hydrogen? (28 February 2009) (неопр.). www.eagle.ca. Дата обращения 16 марта 2019.
- ↑ The Ergosphere: Zinc: Miracle metal? (неопр.). Дата обращения 16 марта 2019.
- ↑ Liquid storage of solar energy: More effective than ever before (англ.). ScienceDaily. Дата обращения 16 марта 2019.
- ↑ A. Belkin, A. Bezryadin, L. Hendren, A. Hubler. Recovery of Alumina Nanocapacitors after High Voltage Breakdown // Scientific Reports. — 04 20, 2017. — Т. 7, вып. 1. — С. 932. — ISSN 2045-2322. — DOI:10.1038/s41598-017-01007-9.
- ↑ Y. Chen, H. Li, F. Lin, F. Lv, M. Zhang. Study on Self-Healing and Lifetime Characteristics of Metallized-Film Capacitor Under High Electric Field // IEEE Transactions on Plasma Science. — 2012-8. — Т. 40, вып. 8. — С. 2014–2019. — ISSN 0093-3813. — DOI:10.1109/TPS.2012.2200699.
Основные типы аккумуляторов
Наиболее распространенные типы аккумуляторов – для бытовой техники, радиотелефонов, фотоаппаратов, фонариков, ИБП, их особенности и лучшие производители. |
Электрический аккумулятор – специальное устройство, накапливающее электроэнергию и обеспечивающее автономное питание оборудования. При его эксплуатации происходит переход одного вида энергии в другой, а также обратимость описанного процесса.
В большинстве случаев используется электрохимический метод. Среди названий электрического аккумулятора – вторичный химический источник тока, так как перед эксплуатацией требуется его зарядка.
Типы аккумуляторов
По типу аккумуляторы разделяют в зависимости от их химсостава, который влияет на их эксплуатационные свойства.
- никель-кадмиевые (Ni-Cd) – наиболее старый тип аккумуляторных батареек, отличается необходимостью соблюдения цикла «полный разряд» – «полный заряд» (имеют эффект памяти) и чувствительны к холоду (плохо отдают энергию на морозе), но могут хранится разраженными и отличаются низким саморазрядом, сейчас используются в основном в электроинструменте
- никель-металл-гидридные (Ni-MH) – очень распространенный тип простых и дешевых компактных аккумуляторных батареек, эффект памяти и чувствительность к холоду несколько ниже, чем у никель-кадмиевых аккумуляторов, но их нужно хранить заряженными и у них выше саморазряд, сейчас они используются в основном в радиотелефонах
- литий-ионные (Li-Ion) – более современный тип аккумуляторов, почти не подвержены эффекту памяти (снижению емкости), что позволяет заряжать их в любое время и необязательно разряжать до конца, чувствительность к холоду есть, но не критична, нужно поддерживать заряд при хранении, они часто используются в фотоаппаратах
- литий-полимерные (Li-Pol) – облегченный вариант литий-ионных аккумуляторов, обладающий теми же свойствами, но со значительно меньшим весом, что нашло применение в компактных мобильных устройствах и дронах
- свинцово-кислотные (SLA) – большие мощные аккумуляторы, способные быстро отдавать огромную энергию (силу тока), что используется в пусковых установках двигателей (стартерах) и источниках бесперебойного питания, требуют периодической подзарядки во время хранения
Также аккумуляторы отличаются напряжением в вольтах (В), емкостью в ампер-часах (Ач) или миллиампер-часах (мАч) и физическим размером (типоразмером).
Классификация аккумуляторов
Все аккумуляторы можно условно разделить по назначению на несколько основных групп:
- бытовые (аккумуляторные батарейки)
- для радиотелефонов
- для фонариков
- автомобильные
- для ИБП
- промышленные
Теперь рассмотрим их немного подробней, включая типоразмеры и лучших производителей.
Аккумуляторные батарейки
Для обеспечения нормального функционирования техники применяются аккумуляторы разных типоразмеров. Основная сфера их использования – питание мелких устройств бытового назначения.
Аккумуляторные батарейки используются для самых различных устройств – радио мышек, клавиатур, фотоаппаратов, простых фонариков, часов, другой мелкой электроники.
Они имеют различные типоразмеры:
- AA (пальчик) – наиболее распространенный формат круглых батареек длиной 5 см, напряжением 1.2 В и емкостью 1000-3000 мАч
- AAA (мини-пальчик) – также широко распространены, имеют длину 4.4 см, такое же напряжение 1.2 В, но меньшую емкость 500-1500 мАч
- крона – более редкая прямоугольная батарейка с напряжением 9 В, используется в некоторых электроприборах (например, мультиметрах)
Существуют и другие, более редкие форматы аккумуляторных батареек:
- CS (Sub C) – короткая круглая батарейка
- C (R14) – средняя круглая батарейка
- D (R20) – большая круглая батарейка
Они мало распространены и используются в некоторых специфических устройствах и старых фотоаппаратах.
К лучшим популярным производителям аккумуляторных батареек можно отнести Panasonic, Varta, Ansmann, Sanyo. Есть также много других именитых брендов, но их чаще подделывают.
Аккумуляторы для радиотелефонов
Это может быть монолитная аккумуляторная батарея либо отдельные элементы. Подобные устройства отличаются небольшим размером и незначительным весом. Аккумуляторы для радиотелефонов часто представляют собой удобные готовые сборки обычных Ni-MH аккумуляторных батареек.
Также в некоторых телефонах используются нестандартные фирменные аккумуляторы. Из производителей можно порекомендовать Panasonic и Robiton.
Аккумуляторы для фонариков
Аккумуляторы для фонарика представлены на рынке в широком ассортименте и выбор зависит от конкретной модели.
Наибольшей популярностью пользуются:
- АА (14500) – аккумуляторы для больших фонариков (длина 5 см, диаметр 1.4 см)
- ААА – обычные Ni-MH элементы с номинальным напряжением 1.2 В и емкостью 500-1100 мАч
- CR123A 16340– созданы для компактных фонариков (длина 3.4 см)
Есть также специальные аккумуляторы для мощных фонариков и электрошокеров.
Они имеют свои уникальные типоразмеры, которые нужно подбирать в зависимости от модели фонарика:
Эти аккумуляторы отличаются физическими размерами и емкостью. В основном они являются литий-полимерными, что делает их очень легкими. Из производителей хорошо зарекомендовали себя Panasonic, Robiton, Fenix.
Автомобильные аккумуляторы
Об автомобильных аккумуляторах мы особо рассказывать не будем, коснемся только отличий от всех других, которые нужно знать.
Это большие обслуживаемые кислотно-свинцовые батареи с жидким электролитом. Они способны быстро отдавать огромный ток, но необходимо следить за их зарядом и уровнем электролита (доливать по необходимости). Хранить свинцовый аккумулятор разряженным нельзя, так как где-то через полгода он выйдет из строя.
Аккумуляторы для ИБП
Аккумуляторы для компьютерных ИБП призваны обеспечить недлительное питание техники в случае временного отключения электричества. Они также являются свинцово-кислотными, но в отличие от автомобильных необслуживаемыми, а электролит в них загущенный в виде геля, что предотвращает утечки.
В остальном эти аккумуляторы подобны автомобильным, они могут быстро отдать большой ток и требуют периодической подзарядки. В разных ИБП используются аккумуляторы с разным напряжением (12 или 24 В), разной емкости (7, 9, 12 Ач) и разного физического размера. Также есть модели, в которые устанавливается несколько соединенных вместе батарей.
Выбирайте аккумулятор такого же напряжения и размера как в вашем ИБП, емкость при желании можно чуть больше (например, 9 Ач вместо 7 Ач) – это продлит работу ПК от ИБП. Из производителей можно порекомендовать SCB, Yuasa и Delta.
Аккумуляторы в ИБП для газового котла и другой ответственной техники, отличаются большей емкостью по сравнению с моделями, применяемыми при работе компьютерного оборудования. Ведь они рассчитаны на поддержание функционирования отопительных приборов на протяжении суток и более.
Такие аккумуляторы часто являются внешними и подключаются к ИБП с помощью специальных клемм, а сами ИБП должны выдавать напряжение в форме чистой синусоиды, что важно для электронасосов, используемых в системах отопления и другой чувствительной к форме напряжения техники.
Промышленные аккумуляторы
Обычно огромные батареи большой емкости. Могут быть разного напряжения, в том числе высоковольтные. Больше мы о них ничего говорить не будем, так как это не тематика нашего сайта.
Заключение
Для того, чтобы аккумулятор хорошо держал заряд и прослужил достаточно долго, он должен быть от надежного проверенного производителя и само собой оригинальным, а не дешевой подделкой. Также важно в каких условиях и как долго хранятся аккумуляторы.
Поэтому лучше всего приобретать аккумуляторы в специализированных магазинах, которые уделяют особое внимание их качеству. Качественные аккумуляторы для самых различных целей от лучших производителей можно приобрести на сайте https://voltacom.ru/catalog/power/akkum.
Зарядное устройство Xiaomi Mi Power Bank 2C 20000mAh
Зарядное устройство Xiaomi Mi Power Bank 2 10000mAh
Зарядное устройство Xiaomi Mi Power Bank 5000mAh
Аккумуляторные батареи. Виды и устройство. Применение
АКБ или аккумуляторные батареи – это оборудование, которое состоит из нескольких аккумуляторов. Оно может накапливать, хранить и расходовать энергию. Благодаря обратимости химических процессов, происходящих внутри аккумулятора, такие устройства могут заряжаться и разряжаться многократно.
Сфера применения аккумуляторов весьма обширна. Они применяются в автомобилях и различной бытовой технике, например, в пультах ДУ и ноутбуках. Но также и в качестве резервных источников питания в медицинской сфере, производстве, космической отрасли, дата-центрах.
Виды и типы АКБ
Сегодня производят около 30 типов аккумуляторов. Такое большое количество обуславливается возможностью применять в качестве электродов и электролитов различные химические элементы. Именно от материала электрода и состава электролита зависят все характеристики аккумулятора.
Мы не будем приводить все типы, а лишь дадим небольшую таблицу с описанием наиболее распространенных:
Устройство
1 — Отрицательный электрод
2 — Разделительный слой
3 — Положительные электроды
4 — Отрицательный контакт
5 — Предохранительный клапан
6 — Положительные электроды
7 — Положительный контакт
Аккумуляторные батареи состоят из нескольких банок аккумуляторов, соединенных либо параллельно, либо последовательно. Последовательное соединение применяют в целях увеличения напряжения, а параллельное для увеличения силы тока.
Каждый из отдельно взятого аккумулятора в АКБ состоит из двух электродов и электролита, помещенных в корпус из специального материала.
Электрод с отрицательным зарядом – анод, с положительным зарядом – катод. Анод содержит восстановитель, катод – окислитель. Внутри корпуса аккумулятора стоит разделительная пластина, которая не позволяет электродам замыкаться.
Электролит – водный раствор, в который погружены оба электрода.
При разрядке аккумулятора восстановитель анода начинает окисляться и выделяются электроны. Электроны затем попадают в электролит и оттуда движутся к катоду, при этом создавая разрядный ток. Попадая в катод электроны восстанавливают его окислитель. Простыми словами можно описать процесс так: электроны идут от отрицательного электрода к положительному и создают разрядный ток.
При зарядке аккумулятора электроды меняются своим химическим составом и происходит обратная реакция. Электроны здесь двигаются от положительного анода к отрицательному катоду.
Особенности разных типов АКБ
Свинцово-кислотные аккумуляторы
Разработан Гастоном Планте в 19 веке. Эти аккумуляторные батареи сегодня наиболее актуальны благодаря дешевизне и универсальности. Сфера их применения обширна ввиду большого количества разновидностей этого типа. В качестве отрицательно заряженных электродов здесь используется оксид свинца. Положительные электроды выполняются из свинца. Электролит – серная кислота.
У свинцовых-кислотных батарей есть следующие разновидности:
- LA – аккумуляторы с напряжением 6 или 12 Вольт. Традиционное устройство для осуществления запуска двигателей автомобилей. Требуют постоянного обслуживания и вентиляции.
- VRLA – напряжением 2, 4, 6 или 12 Вольт. Клапанно-регулируемая свинцово-кислотная аккумуляторная батарея. Как видно из названия этот АКБ укомплектован разгрузочным клапаном. Его роль – минимизировать выделение газа и расход воды. Такие батареи можно устанавливать в жилых помещениях.
- AGM VRLA – как и предыдущий тип оснащен клапаном, но имеет совсем другие свойства. В аккумуляторах, сделанных по технологии AGM роль сепаратора играет стекловолокно. Его микропоры пропитаны жидким электролитом. Такие АКБ не требуют обслуживания и устойчивы к вибрациям.
- GEL VRLA – подвид свинцово-кислотных аккумуляторов с гелеобразным электролитом. Благодаря этому увеличен их ресурс заряда/разряда. Не требуют обслуживания.
- OPzV – герметичные аккумуляторы используемые в области телекоммуникации и для аварийного освещения. Электролит, как и в предыдущем случае гелевый. В электродах содержится кальций, благодаря которому срок службы такого типа батарей – 20 лет.
- OPzS – катод таких аккумуляторов имеет трубчатую структуру. Это существенно повышает циклический ресурс этого типа батарей. Служит также около 20 лет. Выпускается в виде АКБ с напряжением от 2 до 125 В.
Литий-ионные аккумуляторы
Был впервые выпущен Sony в 1991 году и с тех пор активно применяется в бытовой технике, электронных устройствах. Практически все мобильные телефоны, ноутбуки, фотоаппараты и видеокамеры оснащены таким видом батарей. Роль катода здесь играет литий-ферро-фосфатная пластина. Отрицательный анод – каменноугольный кокс. Положительный ион лития переносит заряд в таких батареях. Он может проникать в кристаллическую решетку других материй и образовывать с ними химическую связь. Преимуществом этого типа является высокая энергоемкость, низкий саморазряд и отсутствие нужды в обслуживании.
Литий-ионные аккумуляторные батареи также, как и их свинцовые аналоги имеют большое количество подтипов. В данном случае подтипы отличаются между собой составом катода и анода. Напряжение литий-ионных аккумуляторов варьируется в пределах от 2,4 до 3,7 В.
Одним из самых известных подтипов является литий-полимерные аккумуляторные батареи. Они появились сравнительно недавно и быстро завоевал популярность. Она обусловлена тем, что в литий-полимерных батареях используется твердый полимерный электролит. Это позволяет создавать батареи любой формы. При этом стоимость этих батарей всего лишь на 15% выше обычных литий-ионных.
















