Аккумулятор принцип работы: Что такое АКБ — принцип работы, термины, история изобретения
- 11.12.2018
Как устроен автомобильный аккумулятор — типы современных АКБ, принцип их работы, конструктивные особенности
- Все статьи
- Как устроен автомобильный аккумулятор — типы современных АКБ, принцип их работы, конструктивные особенности
Автомобильный аккумулятор выполняет три функции. Основанная функция АКБ – это запуск двигателя. Также, батарея питает бортовые электрические устройства – при неработающем двигателе. Вторая важная функция – возможность аварийного питания, источником которого аккумулятор выступает в случае поломки генератора. Третья функция – это достижение баланса напряжения, которое поступает от генератора. Эта функция характерна для инжекторных двигателей.
Устройство аккумулятора автомобиля существенно не меняется уже много десятилетий.
Основу работы аккумулятора составляет принцип возникновения разности потенциалов – то есть, напряжения. Оно возникает между пластинами, которые погружены в раствор электролита.
АКБ – устройство, которое, в зависимости от типа и производителя, имеет определенные конструктивно-технологические различия. Но общий принцип – одинаков: все аккумуляторные батареи содержат электроды, разделенные сепараторами, и помещенные в пространство, заполненное электролитом.
Корпус
Корпус аккумулятора состоит из двух частей: основной глубокой емкости и закрывающей крышки. Она может быть оснащена горловинами с пробками или системой, при помощи которой стабилизируется давление внутри батареи, и отводится образующийся газ. Конструкция корпуса зависит от типа АКБ.
Сам корпус изготовлен из материала, к которому предъявляются большие требования прочности и безопасности. Он должен быть устойчив к воздействию агрессивных химических реагентов, переносить колебания температуры и сильную вибрацию. В большинстве современных аккумуляторов корпус сделан из полипропилена.
Он должен быть устойчив к воздействию агрессивных химических реагентов, переносить колебания температуры и сильную вибрацию. В большинстве современных аккумуляторов корпус сделан из полипропилена.
Внутренние отсеки
Стандартное устройство аккумуляторной батареи представляет собой контейнер, состоящий из шести секций (или, как их называют, «банок»). Каждая секция – это отдельный источник питания. Она вырабатывает порядка 2 – 2,1 В. Стандартная АКБ рассчитана на 12 В.
В каждой из ячеек находится набор (или пакет) из отдельных пластин с чередующейся полярностью. То есть, одна пластина положительная, другая отрицательная. Причем, пластины отделены друг от друга. Пластины сделаны из свинца и имеют решетчатую структуру в виде прямоугольных сот. Это облегчает нанесение них активной массы – основного рабочего реагента.
Пластины
Для увеличения прочности пластин в них добавляют сурьму. У этой технологии есть и свои недостатки: присутствие сурьмы способствует выкипанию воды из электролита. Это – основная причина, по которой практически во все типы АКБ необходимо доливать воду. Но технологии не стоят на месте. Устройство автомобильных аккумуляторов совершенствуется. Количество сурьмы в свинцовых пластинах значительно уменьшилось, благодаря чему появились малообслуживаемые и гибридные аккумуляторы.
Это – основная причина, по которой практически во все типы АКБ необходимо доливать воду. Но технологии не стоят на месте. Устройство автомобильных аккумуляторов совершенствуется. Количество сурьмы в свинцовых пластинах значительно уменьшилось, благодаря чему появились малообслуживаемые и гибридные аккумуляторы.
На положительный электрод наносится двуокись свинца, на отрицательный – губчатый свинец. Внутрь заливается электролит, который является водным раствором серной кислоты.
Каждая чередующаяся пластина является электродом, имеющим противоположную полярность. Таким образом, с целью предотвращения замыкания, между каждой парой пластин располагается сепаратор. Он изготовлен из пористого пластика и не создает препятствий для циркуляции электролита внутри ячейки.
Пластин с отрицательной полярностью больше на 1 единицу, так как каждая пластина с положительным зарядом помещена между двумя отрицательными (минусовыми).
Пакет с пластинами надежно фиксируется, чтобы предотвратить смещение и деформацию. Фиксация осуществляется при помощи специального бандажа. Токовыводы пластин (плюсовые и минусовые) объединены в пары. Концентрация энергии происходит при помощи токосборников – на выводные борны аккумулятора. К ним токоприемные клеммы.
Фиксация осуществляется при помощи специального бандажа. Токовыводы пластин (плюсовые и минусовые) объединены в пары. Концентрация энергии происходит при помощи токосборников – на выводные борны аккумулятора. К ним токоприемные клеммы.
Устройство АКБ обеспечивает максимальную надежность. Современные аккумуляторы – это качественные устройства, выступающие источниками питания даже для самых мощных автомобилей.
Виды современных аккумуляторов
Современные АКБ подразделяются на два основных вида: классические и необслуживаемые. Классические существуют уже больше ста лет и описаны выше. Необслуживаемые аккумуляторные батареи были созданы всего несколько десятилетий назад. Они эффективно работают в любом, даже перевернутом, положении. Вместо жидкого электролита в них применяется гелиевый, или адсорбированный сепараторами. Устройство автомобильного аккумулятора, который является необслуживаемым, подразумевает максимальную герметичность. Для отвода газов, которые выделяются при заряде и разряде, предусмотрен специальный клапан.
Главное различие необслуживаемых АКБ от классических – в более низких разрядных и зарядных токах. Причина – в конструкции необслуживаемых батарей. При больших токах классическая АКБ активно выделяет газ и «закипает». У необслуживаемых и герметизированных батарей этого нет.
Устройство и схема автомобильного аккумулятора
Устройство и схема автомобильного аккумулятора
Мы вспоминаем об аккумуляторе тогда, когда он сам напоминает о себе низким зарядом или неисправностью. Но посмотрите на этот тяжелый параллелепипед — что происходит за его пластмассовыми стенками? Откуда вообще в АКБ берется электричество? Понять это не сложно.
Полтора века истории
Трудно поверить, но свинцово-кислотный аккумулятор был изобретен свыше полутора века назад — это произошло во Франции в 1859-1860 годах. Создателем первого аккумулятора стал Гастон Планте, который занимался поиском надежных источников тока для физических опытов.
Свинцово-кислотный аккумулятор появился на свет после долгих раздумий и сотен экспериментов, а первый работоспособный образец был невероятно простым по сути и конструкции. Это была банка, наполненная разбавленной серной кислотой, в которую опущен «рулет» из двух сложенных свинцовых полос, разделенных куском сукна.
Аккумулятор показал очень хорошие результаты, хотя, конечно, и имел некоторые недостатки, главный из которых — низкая емкость. Решить эту проблему смог Камилл Фор — в 1878 году ученый покрыл пластины свинцовым суриком, и с тех пор свинцово-кислотный аккумулятор, в общем, приобрел современные черты.
Устройство и схема автомобильного аккумулятора

Устроен аккумулятор довольно-таки просто. Основу всего составляет прочный корпус, выполненный из кислотоупорной пластмассы — моноблок. Внутри корпус разделен перегородками на шесть банок. Собственно, каждая банка — это и есть аккумулятор, а АКБ — это батарея аккумуляторов. Зачем так сделано? Не проще ли было сделать один большой аккумулятор?
Нет, не проще. Независимо от конструкции, размеров и принципа работы, все типы аккумуляторов дают напряжение около 2 вольт, в случае со свинцово-кислотными аккумуляторами напряжение составляет около 2,1 В. Понятно, что 12 В можно получить, если последовательно соединить сразу шесть таких аккумуляторов — это и делается в АКБ.
В нижней части каждой банки есть опорные призмы высотой несколько миллиметров, на которые опираются самые главные элементы АКБ — электродные блоки. Каждый блок состоит из ряда свинцовых пластин, разделенных тонкими прочными пластмассовыми пластинками — сепараторами.
Блок содержит четное количество пластин, одна их половина — отрицательные, другая — положительные.
Положительные и отрицательные пластины хотя и находятся рядом, но несколько отличаются друг от друга. В основе обеих пластин — свинцовая решетка, но ячейки положительных пластин заполнены двуокисью свинца (имеет темно-коричневый цвет), а ячейки отрицательных — губчатым свинцом (имеет серый цвет).
Электродные блоки жестко устанавливаются в банках, а банки, в свою очередь, закрываются герметичными крышками, в которые впаяны выводы электродов, и выполнены пробки для контроля электролита. Банки соединяются друг с другом посредством массивных свинцовых перемычек — борнов, расположенных на верхней крышке АКБ.
Сверху же монтируются и полюсные клеммы, к которым, собственно, и подключается бортовая электросеть автомобиля.
Так устроены аккумуляторы классической конструкции, а многие виды современных АКБ имеют несколько иные решения. В частности, распространены батареи с общей крышкой моноблока, обладающие меньшей габаритной высотой и лучшим соотношением массы к емкости.
В частности, распространены батареи с общей крышкой моноблока, обладающие меньшей габаритной высотой и лучшим соотношением массы к емкости.
Как аккумулятор запасает энергию
В корне неверно утверждение, что аккумулятор вырабатывает электричество — он его запасает во время заряда, и отдает во время разряда. А достигается эта цель с помощью ряда электрохимических реакций.
Наиболее просто описать процессы, происходящие внутри свинцово-кислотного аккумулятора, можно одной формулой:
Pb + PbO2 + H2SO4 ↔ PbSO4 + H2O
Эта реакция, как можно увидеть, обратимая, и во время разряда она протекает справа налево, а в время заряда — слева направо.
То есть, полностью заряженный аккумулятор представляет собой набор трех химических элементов — свинца, двуокиси свинца и серной кислоты (вода, которой разбавлена кислота, в реакции не принимает участия). При разряде и пористый свинец на отрицательных пластинах, и двуокись свинца на положительных реагирует с кислотой — в результате образуется сульфат свинца, который осаждается на отрицательных пластинах. Нетрудно понять, что во время разряда плотность электролита падает, ведь количество кислоты уменьшается, а количество воды — растет!
Нетрудно понять, что во время разряда плотность электролита падает, ведь количество кислоты уменьшается, а количество воды — растет!
Во время заряда реакция протекает в обратном направлении: из сульфата восстанавливается металлический свинец, а сернокислый остаток вступает в реакцию с водой, образуя серную кислоту. Так что при заряде кислоты становится больше, воды — меньше, а все это ведет к увеличению плотности электролита.
А чтобы эти реакции протекали с наибольшей интенсивностью, в конструкции АКБ имеется ряд особенностей. Главная из них — использование губчатого свинца — он пронизан тончайшими порами, и действительно похож на губку. Поры в десятки раз повышают площадь поверхности отрицательных электродов, что увеличивает интенсивность и эффективность течения реакций.
«Болезни» АКБ и попытки их «лечения»
В аккумуляторах используется свинец, но сам по себе этот металл обладает малой прочностью, поэтому на практике применяется легированный свинец повышенной прочности. Традиционно в качестве легирующей добавки выступает сурьма — ее содержание не превышает 5 — 7%. Однако применение сурьмы имеет не только положительный, но и отрицательный эффект.
Традиционно в качестве легирующей добавки выступает сурьма — ее содержание не превышает 5 — 7%. Однако применение сурьмы имеет не только положительный, но и отрицательный эффект.
Сурьма служит катализатором электрохимического разложения воды, и этот процесс запускается при меньшем напряжении, чем в отсутствии сурьмы. Ситуация усугубляется тем, что со временем сурьма осаждается на отрицательных электродах, и в какой-то момент из-за разложения воды электролит начинает «кипеть» не при полном заряде, а при гораздо более низких напряжениях. От такого АКБ уже не приходится ожидать нормальной работы. Кроме того, обильно выделяющийся газ делает батарею просто небезопасной в пожарном отношении — имели место случаи не просто пожаров, а взрывов таких аккумуляторов.
Данную проблему решают необслуживаемые аккумуляторы, в составе электродов которых нет или очень мало сурьмы (она заменена на другие металлы, в основном — на кальций). В этих АКБ электролит «закипает» только при полном заряде, и за короткое время не успевает выделиться большого количества газа. Нет электрохимического разложения воды — нет и истощения электролита, и именно это является главным преимуществом необслуживаемых АКБ.
Нет электрохимического разложения воды — нет и истощения электролита, и именно это является главным преимуществом необслуживаемых АКБ.
В данном виде аккумуляторов не предусмотрены пробки для контроля электролита — в них просто нет необходимости! Зачем следить за электролитом, если он не «кипит», и его плотность со временем остается постоянной? В остальном необслуживаемые АКБ устроены точно так же, как и АКБ классической конструкции.
Как видите, автомобильный аккумулятор устроен не слишком сложно, но это лишний раз подтверждает, что все гениальное — просто.
что это, значение, принцип работы
В автомобилях и мотоциклах аккумулятор используется для запуска двигателя электростартером. Он служит вспомогательным источником электроэнергии при заглушенном двигателе или в случаях, когда генератор на малых оборотах не справляется с нагрузкой.
Что такое аккумуляторная батарея
Аккумулятор — это перезаряжаемый источник электроэнергии, используемый в машинах и мотоциклах. В автомобилях используются свинцово-кислотные аккумуляторные батареи. Этот выбор обоснован тремя качествами:
В автомобилях используются свинцово-кислотные аккумуляторные батареи. Этот выбор обоснован тремя качествами:
- доступная цена;
- высокая удельная энергоемкость;
- низкое внутреннее сопротивление (большой пусковой ток).
Принцип действия АКБ (автомобильной кислотной батареи) основан на реакции свинца и его диоксида. При разряде электроэнергия вырабатывается за счет взаимодействия свинца с серной кислотой (образование сульфата). Во время заряда окисляется свинец анода и восстанавливается диоксид свинца на катоде.
Устройства состоят из последовательно соединенных секций («банок») напряжением 2 вольта. Напряжение зависит от сферы применения:
- 6-вольтовые АКБ применяются на легкой моторной технике;
- 12-вольтовые — на большинстве мотоциклов, автомобилей, грузовиков и автобусов с бензиновыми моторами;
- 24-вольтовые — на тяжелых дизельных грузовиках и автобусах, на специальной и армейской технике.
Какие бывают аккумуляторы.
 Виды аккумуляторов
Виды аккумуляторовАккумуляторные батареи делятся на два типа:
- Пусковые, главное назначение первых — питание стартера двигателя. Они отличаются большим пусковым током, однако разрушаются при глубоком разряде и не могут долгое время выдавать большой ток. Такие АКБ устанавливаются на технику с двигателями внутреннего сгорания.
- Тяговые, предназначенные для обеспечения ходовых двигателей электроэнергией. Они не могут выдать ток в сотни ампер, зато могут без вреда разряжаться «в ноль» — пластины не разрушаются при глубоком разряде. Более толстые прочные пластины кислотных тяговых АКБ увеличивают вес и стоимость устройств. Такие аккумы используются на электромобилях, погрузчиках и прочей технике с электродвигателями.
В зависимости от сплава состава пластин и электролита, автомобильные пусковые АКБ делятся на следующие типы:
- Сурьмянистые. Самая старая разновидность «аккумов», отличающаяся высоким содержанием сурьмы в свинцовых электродах (более 5%).
 Сурьма увеличивает прочность пластин, однако усиливает процесс электролиза — вода разлагается на кислород и водород. Такие аккумуляторы требуют постоянного контроля уровня содержимого банок и доливки дистиллированной воды.
Сурьма увеличивает прочность пластин, однако усиливает процесс электролиза — вода разлагается на кислород и водород. Такие аккумуляторы требуют постоянного контроля уровня содержимого банок и доливки дистиллированной воды. - Малосурьмянистые. АКБ с небольшим содержанием сурьмы (до 5%) медленнее выкипают и не требуют частых проверок уровня электролита. Это позволило создать необслуживаемые батареи, которые практически не требуют вмешательства. В отличие от кальциевых и гелиевых батарей, малосурьмянистые менее требовательны к показателям напряжения бортовой сети. Если напряжение на генераторе превышает норму, АКБ не разрушаются и не теряет емкость.
- Кальциевые. Более современные модели, в которых свинец пластин содержит кальций вместо сурьмы. Это позволило еще больше снизить интенсивность газовыделения и уменьшить саморазряд. Они хранятся дольше, однако теряют емкость при систематическом перезаряде и резких скачках напряжения бортовой сети. Поэтому для старых отечественных авто с ненадежным электрооборудованием актуальны малосурьмянистые аккумы.

- Гибридные. Малосурьмянистые аноды и кальциевые катоды таких устройств позволяют совместить положительные качества двух типов батарей. Они имеют средние характеристики: расход воды ниже, чем у сурьмянистых, устойчивость к перезаряду выше, чем у кальциевых.
- Гелевые и AGM. Электролит в них находится в связанном гелеобразном состоянии. Это исключает возможность утечки кислоты при повреждении или опрокидывании аккума. AGM-устройства заполнены пористым материалом, предотвращающим осыпание пластин. Высокая цена, резкое падение емкости при низкой температуре и уязвимость к большому току заряда делает их востребованными лишь на дорогих иномарках, оборудованных системами «стоп-старт».
Отдельно стоит отметить два вида батарей, используемых на технике с электроприводом:
- Щелочные. Никель-железные и никель-кадмиевые аккумы со щелочью вместо кислоты отличаются устойчивостью к глубокому разряду и долговечностью. Однако они обладают высоким внутренним сопротивлением и не могут выдать ток, достаточный для работы стартера.

- Литий-ионные. Изделия отличаются высокой энергоемкостью и быстрым зарядом. Однако они дорого стоят, чувствительны к температуре и быстро теряют емкость. Их используют на электромобилях типа Tesla, Nissan Leaf.
Щелочные и литиевые батареи не применяются в качестве пусковых.
Из чего состоит аккумулятор автомобиля (конструкция аккумулятора)
12-вольтовая аккумуляторная батарея состоит из корпуса с отделениями для 6 ячеек. В ячейки помещены сборки из положительных и отрицательных электродов, разделенных сепараторами. Перемычки обеспечивают электрический контакт между анодами и катодами соседних банок. К крайнему катоду и аноду подключена отрицательная и положительная клеммы. Банки заполнены электролитом — водным раствором серной кислоты. Для его заливки и контроля уровня в крышке корпуса имеются пробки.
Основные характеристики автомобильного аккумулятора
При выборе аккума для машины следует обратить внимание на такие показатели:
- Емкость — количество электроэнергии, которую может отдать аккумулятор до момента полного разряда.
- Напряжение, которое должно соответствовать напряжению бортовой сети.
- Пусковой ток, определяющий эффективность работы аккумулятора.
- Полярность — расположение положительной и отрицательной клеммы. Если расположить АКБ лицевой частью к себе (стороной с клеммами), при прямой полярности плюс находится слева, при обратной — справа. В отечественных авто и большинстве иномарок предусмотрены аккумы с прямой полярностью.
- Габариты. Слишком большую или маленькую батарею не получится закрепить на штатном месте.
Следует учитывать тип АКБ. Для машин с системами «старт-стоп» нужно покупать гелевые и AGM-системы, а на более простые авто следует ставить кальциевые и гибридные.
Аккумуляторные батареи: виды, принцип действия, характеристики
Данная статья посвящена описанию технических характеристик и принципа действия аккумуляторных батарей различных типов.
Содержание:
- Принцип действия
- Технические характеристики
- Виды аккумуляторов
- Правила эксплуатации
Аккумуляторные батареи являются источником постоянного тока, предназначенным для хранения и накопления электроэнергии. Большинство моделей современных аккумуляторов действуют по принципу циклического преобразования химической энергии в электрическую, что обеспечивает возможность многократной зарядки и разрядки. В настоящее время такие устройства используются во многих электротехнических приборах.
Принцип действия
Работа аккумуляторных батарей основана на взаимодействии жидкости и металлов. Данный процесс является обратимым и возникает в случае замыкания контактов отрицательных и положительных пластин. При разряде, который происходит при подключении к потребителям, активная масса электродов вступает в реакцию с электролитом. Для зарядки аккумуляторов применяется специальное устройство.
Заряд аккумуляторной батареи должен осуществляться при оптимальном уровне напряжения. Работа АКБ зависит от температуры окружающей среды. При ее повышении увеличивается отдаваемая мощность, но в то же время увеличивается коррозия электродов и саморазряд. Понижение температурного режима сопровождается снижением емкости, уменьшением плотности электролита и замедлением химических процессов.
Срок службы аккумуляторных батарей зависит от интенсивности эксплуатации и в среднем составляет 4-5 лет. Производители постоянно предлагают новые решения, целью которых является повышение эффективности. Среди наиболее перспективных направлений можно выделить:
- Совершенствование конструкции (передовая AGM-технология).
- Использование двух батарей, при этом одна из них предназначена только для запуска, а вторая — для всех остальных процессов и операций.
- Система управления энергетическим балансом, регулирующая подключение потребителей.
Технические характеристики
При выборе аккумуляторов необходимо учитывать следующие параметры:
- Емкость — показывает количество отдаваемого электролита в случае разрядки до минимально допустимого значения.
- Ток холодной прокрутки — обеспечивает возможность запуска батареи при низких температурах.
- Срок хранения — максимальный период, на протяжении которого аккумулятор может храниться при определенных условиях без необходимости дополнительной зарядки.
- Саморазряд — потеря емкости в случае отсутствия потребителя.
- Электродвижущая сила — показывает уровень напряжения на клеммах без внешней нагрузки. Для измерения данной величины используется вольтметр или мультиметр.
- Полярность — влияет на расположение батареи под капотом авто или в корпусе другого устройства.
Виды аккумуляторов
Все многообразие моделей аккумуляторов можно разделить на несколько больших групп:
- Свинцово-кислотные — наиболее распространенный вид АКБ, который применяется как источник бесперебойного питания и устанавливается автомобилях.
- Никель-кадмиевые — в настоящее время они используются в качестве замены стандартным гальваническим элементам, а также в троллейбусах, трамваях и электрокарах.
- Никель-металлогидридные — предназначены для использования в осветительной технике, радиоаппаратуре и электромобилях.
- Литий-ионные — получили широкое распространение в современных строительных и бытовых приборах и мобильных устройствах.
Правила эксплуатации
С целью обеспечения безопасности и продления срока службы аккумуляторных батарей рекомендуется придерживаться следующих правил:
- Не хранить аккумуляторы в разряженном состоянии, поскольку это ведет к сульфатации электродов и снижению емкости.
- Не допускать создания цепей короткого замыкания между клеммами, так как электрический ток может расплавить контакты и нанести термический ожог.
- Подключать батарею к устройству необходимо в соответствии с ее полярностью. При неправильном подсоединении приборы могут выйти из строя.
- Запрещается вскрывать корпус аккумулятора. Воздействие расположенного внутри гелеобразного электролита на кожу может вызвать химический ожог.
- Утилизация отслужившей свой срок аккумуляторной батареи должна осуществляться в соответствии с установленными правилами для устройств, содержащих тяжелые металлы.
Как работает аккумулятор
Как работает автомобильный аккумулятор? Автомобильный аккумулятор обеспечивает всю электросистему машины необходимым количеством электроэнергии для питания всех электрических компонентов в Вашем автомобиле. И речь здесь идёт о довольно огромной ответственности. Без аккумулятора автомобиль, как Вы, наверное, уже поняли, никуда не поедет. Давайте взглянем на то, как работает этот мощный маленький ящик! Химическая реакция — это главный принцип работы аккумулятора: он попросту преобразует химическую энергию в электрическую, необходимую для питания Вашего автомобиля, обеспечения напряжением стартера и множества других электрических узлов машины, а также электрическую — обратно в химическую. Ещё одна важная функция аккумулятора — он обеспечивает постоянство силы тока — он также стабилизирует напряжение для того, чтобы двигатель работал
По-простому принцип работы аккумулятора можно охарактеризовать так: химические процессы в нём приводят в появлению электрического тока, которым питается автомобиль — особенно полезен такой ток, и больше всего его потребляется, когда Вы стартером раскручиваете двигатель, заводя его; когда же автомобиль заведён, то двигатель крутит генератор — и здесь мы видим процесс превращения механической энергии (кручение генератора) в электрическую — в свою очередь генератор передаёт произведённый им ток аккумулятору, и тот превращает уже электроэнергию в химическую — аккумулирует её, сохраняет, чтобы затем опять «накормить» ей тот стартер или любые иные электрические системы автомобиля, когда генератор не работает или же когда электроэнергии, производимой генератором недостаточно для обеспечения всех систем автомобиля. Автомобильный аккумулятор имеет два полюса: один положительный и второй — отрицательный, и Вы, наверное, уже знаете это, если хотя бы раз видели или отсоединяли/крепили клеммы аккумулятора. Эти полюсы подключаются к машине и отвечают за питание ряда очень важных механизмов автомобиля, в том числе: Запуск двигателя Кондиционер Воспроизведение аудиосистемы Все световые механизмы (фары, задние фонари, разного рода подсветки и т.п.) Стеклоочистители Многое-многое другое. В подавляющем большинстве случаев аккумулятор состоит из шести ячеек. В каждую ячейку помещаются два электрода, представляющих собой и изготовленных из восьми перекрывающихся металлических пластин. Эти восемь перекрывающихся металлических пластин образуют то, что известно как «гальванический элемент». Таким образом, в общей сложности каждая ячейка включает 2 электрода и 16 пластин. Именно через эти пластина производится питание электричеством автомобиля. Но как это работает? На самом деле, всё достаточно просто — давайте резюмируем вышеописанное: Батарея состоит из шести ячеек Каждая ячейка состоит из двух наборов пластин Каждый набор пластин включает в себя восемь перекрывающихся металлических пластин
А теперь немного химии… Первый набор пластин в ячейке является положительным, а второй — отрицательным. Положительное сетка покрыта оксидом свинца и приносит электроны в ячейку. Отрицательный набор покрыт непосредственно свинцом, и он, наоборот, освобождает электроны. Металлические пластины — помните, восемь из них в каждой сетке, 16 в каждой ячейке — находятся в смеси воды и серной кислоты (на самом деле в этой концентрации только около 35 процентов серной кислоты, но этого более чем достаточно, чтобы, например, прожечь одежду и сильно обжечь кожу. Эта смесь действует как электролит — вещество, которое хорошо проводит электричество. Когда аккумулятор заряжается (от генератора или другими способами), то происходит химическая реакция окисления свинца на положительном заряде, в результате чего электролит насыщается серной кислотой и удельный вес электролита повышается. Когда же аккумулятор, наоборот, разряжается, питая какие-либо электросистемы автомобиля (мы помним, что основной потребитель — это стартер), то за счёт восстановления свинца на другом — отрицательном наборе пластин, в результате которого образуется больше воды, и, следовательно, удельный вес электролита уменьшается. При этом, химический процесс в каждой из пластин настолько ничтожен, что выделяется очень мало энергии, но на выходе из аккумулятора легкового автомобиля, когда все эти реакции проходят по всем 6 ячейкам, мы и получаем уже сокровенные 12 Вольт. Возможные неполадки аккумулятора Аккумулятор со временем приходит в негодность — это естественный его износ и, кроме того, разного рода вредные процессы в нём и воздействия на него могут значительно укоротить срок его жизни. И первыми симптомами того, что в аккумуляторе есть неполадки, являются неспособность завести автомобиль (особенно, в морозную погоду).
Итак, какие же могут быть проблемы с аккумулятором? Низкий уровень жидкости в аккумуляторе: автомобильные аккумуляторы обычно имеют небольшую часть корпуса в виде полупрозрачной полосы — чтобы Вы всегда могли следить за уровнем жидкости Вашего аккумулятора. Если уровень жидкости ниже свинцовых пластин (проводник электричества) внутри аккумулятора, то это самое время, чтобы либо долить её, либо заменить аккумулятор. «Отёк» аккумулятора — это когда корпус Вашего аккумулятора выглядит так, как-будто он съел очень много и вздулся. Это может указывать на срочную замену аккумулятора. Можно обвинить избыточное количества тепла в качестве причины вздутия аккумулятор и, как следствие, уменьшения срока службы аккумулятора. Запах тухлых яиц от аккумулятора: Вы можете заметить острый запах тухлого яйца (на самом деле, это запах серы) вокруг своей батареи. Причина: протечка аккумулятора. Протечка эта, кроме запаха, также вызывает коррозию вокруг клемм.
Как работает аккумулятор — принцип работы АКБ простыми словами
Аккумулятор или сокращённо (АКБ), это основное и необходимое устройство в любом автомобиле. Каждый водитель знает, что серце его машины — это конечно же аккумулятор, и нет таких машин с двигателем внутреннего сгорания, где бы его не было. Как бы это устройство не менялось за 150 лет с момента его изобретения, принцип работы аккумуляторной батареи остался низменным. Однако, современность внесла серьёзные коррективы в технологические процессы их изготовления. В этой статье вы ознакомитесь с и используемыми материалами, из чего состоит аккумулятор и как он работает. Итак, как работает аккумулятор (АКБ)?
Как работает аккумулятор (АКБ)Понятие аккумулятор и его устройство
В общем понимании этого слова в технике под термином «Аккумулятор» подразумевается устройство, позволяющие при разных условиях эксплуатации накапливать определенный вид энергии, либо же — расходовать ее для человеческих нужд.
Хотите узнать, как построить энергосберегающий дом? Смотрите секреты строительства дома , который сам экономит
Применимы в тех ситуациях, когда необходимо собрать энергию за определенное время, после чего использовать ее для совершения больших трудоемких процессов. Так — гидравлические аккумуляторы, используемые в шлюзах, позволяют поднимать корабли на новый уровень русла реки.
Электрические аккумуляторы работают с электроэнергией по такому же принципу: когда вначале накапливают (аккумулируют) электричество от внешнего источника заряда, а после отдают его подключенным приборам для совершения дальнейшей работы. По своей природе они относятся к химическим источникам тока, способным совершать много раз периодические циклы разряда и заряда.
В процессе работы постоянно происходят химические реакции между компонентами электродных пластин с заполняющим их веществом — электролитом.
Узнайте больше о самовозобновляемой и бесплатной энергии будущего. Солнечные батареи в действии.
На рисунке ниже изображена схема устройства аккумулятора. Изображен тот вид, когда в корпус сосуда вставлены две пластины из разнородных металлов с выводами для обеспечения электрических контактов. Между пластинами залит электролит.
Устройство аккумулятораКак работает аккумулятор (АКБ) при разряде
В момент, когда к электродам подключена нагрузка в виде лампочки, создается замкнутая электрическая цепь, через которую протекает ток разряда. Его формированию способствует движение электронов в металлических частях и анионов с катионами в электролите.
Этот процесс условно показан на схеме с никель-кадмиевой конструкцией электродов.
Заряд и разряд аккумулятораВ данном примере в качестве материала положительного электрода используют окислы никеля с добавками графита, которые повышают электрическую проводимость. Металлом отрицательного электрода работает губчатый кадмий.
Во время разряда частицы активного кислорода из окислов никеля выделяются в электролит и направляются на отрицательные пластины, где окисляют кадмий.
Общее устройство и маркировка аккумуляторных батарейРабота аккумулятора при зарядеБеря за основу отключенную нагрузку на клеммы пластин, подаем постоянное (в определенных ситуациях пульсирующее) напряжение большей величины, чем у заряжаемого аккумулятора с той же полярностью, когда плюсовые и минусовые клеммы источника и потребителя совпадают.
Таким образом мощность зарядного устройства всегда больше, чем та, которая «подавляет» оставшуюся в аккумуляторе энергию и создает электрический ток с направлением, противоположным разряду. Это приводит к изменениям внутренних химических процессов между электродами и электролитом. К примеру на банке с никель кадмиевыми пластинами положительный электрод обогащается кислородом, а отрицательный — восстанавливается до состояния чистого кадмия.
При разряде и заряде аккумулятора происходит изменение химического состава материала пластин (электродов), а электролита не меняется.
Способы соединения аккумуляторов (как работает аккумулятор)Параллельное соединение (как работает аккумулятор)
Величина разряда тока, зависит от многих факторов, хотя в первую очередь от конструкции, примененных материалов и их габаритов. Чем значительнее площадь пластин у электродов, тем больший ток они могут выдерживать.
Этот принцип используется для параллельного подключения однотипных банок у аккумуляторов при необходимости увеличения тока на нагрузку. Чтобы зарядить такую конструкцию потребуется поднять мощность источника. Этот способ используется редко для готовых конструкций, в настоящее время куда проще сразу приобрести необходимый аккумулятор. Но им пользуются производители кислотных АКБ, соединяя различные пластины в единые блоки.
Последовательное соединение (как работает аккумулятор)
В зависимости от применяемых материалов, между двумя электродными пластинами распространенных в быту аккумуляторов может быть выработано напряжение 1,2/1,5 или 2,0 вольта. На самом деле этот диапазон гораздо шире. И многим электрическим приборов его явно недостаточно. Поэтому однотипные аккумуляторы подключают последовательно, делают это зачастую в едином корпусе.
Примером подобной конструкции служит широко распространенная автомобильная разработка на основе серной кислоты и свинцовых пластин-электродов.
Часто среди водителей транспорта, под понятием «аккумулятор» принято понимать любое устройство, независящее от количества его составных элементов — банок. Это не является правильным. Собранная из нескольких последовательно подключенных банок конструкция считается уже батареей, за которой закрепилось сокращенное название «АКБ». Ее внутреннее устройство показано на рисунке.
Устройство кислотной аккумуляторной батареи (АКБ)Любая банка состоит из двух блоков с набором пластин для положительного и отрицательного электродов. Блоки входят друг в друга без металлического контакта с возможностью надежной гальванической связи через электролит.
При этом контактные пластины имеют дополнительную решетку и отдалены между собой разделительной пластиной — сепаратором.
Благодаря соединению пластин в блоки увеличивается их рабочая площадь. Это снижает общее удельное сопротивление всей конструкции, позволяет повышать мощность подключаемой нагрузки.
Компоновка АКБ
С внешней стороны корпуса такая АКБ имеет элементы, показанные на рисунке ниже.
Компоновка кислотной аккумуляторной батареи (АКБ)Из него видно, что прочный пластмассовый корпус закрыт герметично крышкой и сверху оборудован двумя клеммами. Они обычно имеют конусную форму, для подключения к электрической схеме автомобиля. На их выводах выбита маркировка полярности: «+» и «-». При этом есть одно правило: во избежании ошибок при подключении, диаметр положительной клеммы немного больше, чем у отрицательной.
У обслуживаемых аккумуляторных батарей сверху каждой банки помещена заливная горловина, чтобы контролировать уровень электролита либо доливки дистиллированной воды при эксплуатации. В нее вворачиваются пробка, предохраняющая внутренние полости банки от попадания загрязнений и одновременно не дает выливаться электролиту при наклонах АКБ.
Для того, чтобы предотвратить бурное выделение газов из электролита, который возможен при интенсивной езде, в пробках делаются отверстия для предотвращения повышения давления внутри банки. И через эти отверстия выходят кислород и водород, а также пары электролита. Такие ситуации, связанные с чрезмерными токами заряда, желательно избегать.
На том же рисунке выше показано соединение элементов между банками и расположение пластин-электродов.
Стартерные автомобильные АКБ (свинцово-кислотные) работают по принципу двойной сульфатации. На них во время разряда/заряда происходит электрохимический процесс, что сопровождается изменением химического состава активной массы электродов с выделением или поглощением в электролит (серную кислоту) воды.
Этим явлением можно объяснить повышение удельной плотности электролита при заряде, а так же снижение при разряде батареи. Иными словами, величина плотности дает возможность оценивать электрическое состояние АКБ. Для ее замера используют специальный прибор — автомобильный ареометр.
В состав электролита кислотных батарей входит дистиллированная вода. Она же при отрицательной температуре переходит в твердое состояние — лед. Поэтому, чтобы автомобильные аккумуляторы не замерзали в холодное время, необходимо применять специальные меры, предусмотренные правилами эксплуатации.
Виды аккумуляторов
Классификация АКБ по составу активного вещества
Свинцовые пластины, используемые в старых аккумуляторах перестали устраивать потребителей. Таким образом, возникала необходимость по улучшению качества работы АКБ. Сначала добавили сурьму к свинцу, что позволило заметно продлить срок эксплуатации батареи. На следующем этапе – уменьшили процентное содержания сурьмы до оптимальной концентрации. Такой подход привел к созданию малообслуживаемых аккумуляторов, характерной чертой которых является более редкий процесс долива воды.
При использовании металлического кальция для покрытия пластин появились кальциевые энергосберегающие источники. В предыдущих моделях потери воды из-за электролиза на 12 вольт нуждались в постоянном доливе, а кальций позволил повысить этот порог до 16 вольт. Так появилась возможность в производстве необслуживаемых аккумуляторов и использовать герметичный, неразборной корпус.
Виды АКБ
- Сурьмянистые батареи. Этот вид относится к классике из-за повышенного состава сурьмы, которая ускоряет процесс электролиза.
- АКБ со свинцом. В малосурьмянистых АКБ материалом для пластин служит свинец с небольшой примесью сурьмы. В них степень саморазряда значительно меньше, чем в сурьмянистых АКБ.
- Калициевые источники. При производстве кальциевых источников свинцовые пластины легированы до 0,1% кальцием. Они могут иметь различные заряды, как отрицательный, так и положительный.
- Гибридные источники энергии вытесняют кальциевые. При их производстве, две объединенные основные технологии имеют конструктивные отличия: одна, когда пластины формируются из сплава свинца и сурьмы, положительные электроды, а другая – когда пластины формируются из сплава свинца и кальция, отрицательные электроды.
- EFB является улучшенной жидкозаполненной батареей. Свинцовые пластины в ЕФБ аккумуляторах в два раза толще, чем у обычных, вследствие чего увеличивается их ёмкость. Каждая платина закрыта в пакет из специальной ткани, который наполнен жидким сернокислотным электролитом.
- В гелевых аккумуляторах применяется гелеобразный электролит. Суть такой технологии в том, что она позволяет снизить текучесть электролита, который содержит агрессивную серную кислоту.
- В литиевых АКБ используется жидкий электролит, представляющий собой раствор фторсодержащих солей лития в смеси эфиров угольной кислоты.
- AGM имеет отличительную особенность в электролите, где с помощью специальной технологии между пластинами вставляются стекловолоконные микропористые прокладки.
- Во всех щелочных батареях применяется растворенная в воде щёлочь.
Классификация батарей по типу электролита
Электролиты бывают кислотными и щелочными.
Щелочные растворы применяются в заправке аккумуляторных батарей. Щелочные аккумуляторные жидкости этот такие жидкости, которые проявляют большую активность по отношению к металлам и кислотам. При реакциях с кислотами образуются соль и вода. Растворы щелочей подвергаются гидролизу. Химические свойства позволяют использовать этот тип электропроводящей жидкости для накопления электрической энергии в аккумуляторе.
Кислотные смеси с дистиллированной водой применяются в основном в автомобильных аккумуляторах. Составы этого типа легко можно приобрести в специализированных магазинах либо, при желании, приготовить самостоятельно на дому. На заводе процесс изготовления таких смесей осуществляется в масштабном производстве по ГОСТу. В домашней обстановке его приготовление так же возможно при соблюдении обязательных пропорций и правил техники безопасности. Для этого нужно смешать кислоту с дистиллированной водой.
Как работает аккумулятор — АКБ
Как работает аккумулятор (АКБ)Принцип работы аккумулятора основан на электрохимической реакции окисления свинца в растворе серной кислоты и воды.
При разрядке батареи на положительной пластине происходит окисление металлического свинца, в то время, как на отрицательной пластине восстанавливается уже диоксид свинца.
При зарядке происходит обратный процесс, количество диоксида свинца на отрицательной пластине уменьшается, а на положительной пластине увеличивается количество металла.
Так же при разрядке АКБ уменьшается количество серной кислоты в электролите и увеличивается количество воды. А при зарядке происходит обратный процесс.
Материалы АКБ
Пластины
На данный момент наиболее качественные батареи потерпели небольшие изменения. И связаны эти изменения с материалом пластин. Теперь пластины делают не из чистого свинца, а из его сплава с серебром. При этом удалось снизить массу батареи на треть, а срок её службы увеличить на 20 %.
Кроме этого, изменилась сама технология их изготовления. Если первые пластины производились путём их литья, то сегодня их делают из тонкого свинцового листа, путём штамповки. Такой метод дешевле и при этом пластины получаются прочнее и тоньше.
Сепараторы
Одной из причин выхода АКБ из строя является короткое замыкание положительных и отрицательных пластин.
Когда из пластин осыпается активная зона внизу банок происходит замыкание. Чтобы этого не случилось на помощь приходят сепараторы, которые делают в виде конвертов, запаянных снизу, под пластинами. Таким образом, когда активная зона осыпается она остаётся внутри конверта и не замыкает.
Литий-ионные аккумуляторы
Эти батареи получили широкое распостранение благодаря мобильным телефонам и иным гаджетам. Сегодня же, существуют разработки и для автомобилей. Однако, невзирая на все свои достоинства, в автотехнике данный вид АКБ не прижился из-за ряда принципиальных недостатков.
Литий-ионные аккумуляторы- Они резко теряют свою мощность из-за низкой температуры.
- Для зарядки таких батарей требуется строгое соответствие зарядному току, а это требует переделки электронной части генераторов.
- И самое главное, данные АКБ имеют стоимость в 15 раз дороже обычного кислотного аккумулятора.
Как было указано выше, электролит представляет собой раствор серной кислоты и воды. Под действием низких температур, известно, что вода замерзает, однако с электролитом этого не происходит.
Но тем не менее она заметно загустевает и теряет свои свойства, из-за чего ёмкость батареи заметно снижается. Что бы избежать этого, сегодня, в электролит добавляют разнообразные присадки.
Гелевые электролиты
Их по праву можно считать вершиной эволюции кислотных батарей. Такие АКБ называются попросту, гелевыми. В этих устройствах электролит модифицирован настолько, что представляет собой нечто наподобие желе.
Такая модификация, в комплексе с другими вышеописанными инновациями дала поистине волшебные результаты. В итоге батареи стали практически вечными, невосприимчивыми к переворачиванию, практически не теряющими свои свойства зимой и при этом на много легче по массе.
Графен-полимерные аккумуляторы
Это, пожалуй, самые перспективные батареи для использования, как в автомобилях, оснащённых ДВС, так и электрической силовой установкой. В производстве этих АКБ использованы нанотехнологии.
Графен-полимерные аккумуляторыПринцип работы этих поистине чудесных аккумуляторов заключается в следующем: их ёмкость, практически в три раза больше литий-ионных и при этом имеет меньшую стоимость, поскольку в их производстве не используется дорогостоящий литий. Кроме этого они не теряют своих свойств под действием низких температур.
Основные технические характеристики аккумуляторов
Технические характеристики аккумуляторовНоминальная емкость аккумулятора
Номинальная емкость элемента – способность накапливать и отдавать электроэнергию постоянного тока, определяет время автономной работы ИБП. Емкость электрического аккумулятора показывает время питания подключенной к нему нагрузки.
Важно! Полностью емкость не характеризует энергию аккумулятора, то есть энергию, которая может быть накоплена в полностью заряженном аккумуляторе. Чем больше напряжение аккумулятора, тем больше накопленная в нем энергия.
Емкость всегда указывается на корпусе АКБ, а также на упаковке. Именно по этому критерию, большинство пользователей выбирают нужную модель.
Пусковой ток
Это величину, характеризующая параметр тока, который протекает в стартере автомобиля в момент пуска силового узла. Пусковой или стартерный ток возникает в тот момент, когда в замке зажигания поворачивается ключ и начинает проворачиваться стартер. Единица измерения величины – Ампер. Тот же ток холодной прокрутки является показателем поведения аккумулятора в морозную погоду и сможет запускать двигатель при минусовых показателях. Определяется мощностью тока, которую батарея может выдать в течение первых 30 секунд при температуре -18°С. При высоких показателях пускового тока увеличиваются шансы завести машину при минусовой температуре.
Полярность
Порядок расположения на крышке аккумулятора присоединительных клемм, которые являются токовыводящими соединительными элементами, называется полярностью. Имеет два полюса – положительный и отрицательный и варианты расположения – прямое и обратное.
Прямая полярность – отечественная разработка. Дла ее определения нужно повернуть аккумулятор таким образом, чтобы этикетка была перед глазами. При расположении плюсовой клеммы слева, а минусовой справа, можно утверждать, что АКБ с прямой полярностью. На иномарках устанавливаются аккумуляторные батареи обратной полярности.
Прямая и обратная полярность АКБУстройство корпуса
У большинства аккумуляторов корпус состоит из ударопрочного полипропилена. Он характеризуется как легкий материал, не вступающий в химическую реакцию с агрессивным электролитом АКБ. Полипропилен имеет весьма хорошую стойкость к перепадам температур, возникающих под капотом автомобиля, где нагрев может достигать до +60 ̊С, а при морозах до -30°С. Корпус большинства АКБ состоит из ручки для переноса, пробок, индикатора заряда, клемм для подключения к электросети. Вес АКБ емкостью 55Ач около 16,5 кг. Известными типами аккумуляторов, обладающих спросом являются: американский, европейский, азиатский и российский типы корпусов.
Европейский тип корпуса характерен тем, что АКБ клеммы находятся в углублении, их верхний край не выступает над плоскостью крышки. В некоторых случаях клеммы дополнительно защищаются от внешнего воздействия специальными крышечками. Азиатский тип корпуса – это коробка, на которой клеммы расположились на верхней крышке. Верхний край клемм является самой высокой точкой аккумулятора.
Российский стандарт АКБ
| Обозначение | Описание букв |
| А | АКБ имеет общую крышку для всего корпуса |
| З | Корпус батареи залит и она является полностью заряженной изначально |
| Э | Корпус-моноблок АКБ выполнен из эбонита |
| Т | Корпус-моноблок АБК выполнен из термопластика |
| М | В корпусе использованы сепараторы типа минпласта из ПВХ |
| П | В конструкции использованы полиэтиленовые сепараторы-конверты |
Тип крепления аккумулятора
Особое внимание при выборе АКБ следует уделять типу крепления АКБ, при котором батарея может крепиться снизу или сверху. С помощью специальной монтажной рамки, которая охватывает аккумулятор, элемент крепится вверху. Крепление аккумулятора происходит с помощью планки и двух шпилек. Чаще всего такой вид установки и фиксации аккумуляторной батареи встречается на автомобилях китайского или корейского производства.
Тип крепления на АКБНижнее крепление применимо на европейских автомобилях. На нижней части корпуса АКБ находится выступ. За этот выступ аккумулятор прижимается к платформе с помощью пластины и винта.
Выступ для фиксации АКБЗаключение
Теперь вы знаете, как работает аккумулятор. Его роль в работе приборов трудно оспорить. Данный источник энергии применяться почти во всех отраслях. Что доказывает его значимость и необходимость знаний о принципе работы АКБ. А также ее внутреннем содержимом. Аккумуляторы широко используются в автомобилях, разнообразных электроприборах, кондиционерах, мультимедийных центрах. Там, где, генераторы не всегда справляются с обеспечением их энергией. И тогда в «игру» вступает АКБ, которая кроме подпитки энергией еще и выполняет основную функцию, обеспечивая электроэнергией стартер двигателя. Водителю необходимо знать, как устроен аккумулятор. Ведь в нужное время придется устранять сбои в работе источника энергии. К тому же, важно иметь представление о назначении и видах аккумулятора, чтобы правильно использовать ресурс, подобрать батарею к условиям эксплуатации и автомобилю.
Как работает аккумулятор (АКБ)Принципы работы свинцового аккумулятора! | Статьи компании ООО «KRONVUZ» г Москва
Свинцовые аккумуляторы являются вторичными химическими источниками тока, которые могут использоваться многократно. Активные материалы, израсходованные в процессе разряда, восстанавливаются при последующем заряде. Химический источник тока представляет собой совокупность реагентов (окислителя и восстановителя) и электролита. Восстановитель (отрицательный электрод) электрохимической системы в процессе токообразующей реакции отдает электроны и окисляется, а окислитель (положительный электрод) восстанавливается. Электролитом, как правило, является жидкое химическое соединение, обладающее хорошей ионной и малой электронной проводимостью. В свинцовом аккумуляторе в токообразующих процессах участвуют двуокись свинца (диоксид свинца) РЬО 2 (окислитель) положительного электрода, губчатый свинец РЬ (восстановитель) отрицательного электрода и электролит (водный раствор серной кислоты H2S04). Активные вещества электродов представляют собой относительно жесткую пористую электронопроводящую массу с диаметром пор 1,5 мкм у РЬО2 и 5-10 мкм у губчатого свинца. Объемная пористость активных веществ в заряженном состоянии — около 50%. Часть серной кислоты в электролите диссоциирована на положительные ионы водорода Н+ и отрицательные ионы кислотного остатка (SO4)2-. Губчатый свинец при разряде аккумулятора выделяет в электролит положительные ионы двухвалентного свинца РЬ2+. Избыточные электроны отрицательного электрода по внешнему участку замкнутой электрической цепи перемещаются к положительному электроду, где восстанавливают четырехвалентные ионы свинца РЬ4+ до двухвалентного свинца РЬ2+. Положительные ионы свинца РЬ2+ соединяются с отрицательными ионами кислотного остатка (SO2)2-, образуя на обоих электродах сернокислый свинец РЬSО4 (сульфат свинца). При подключении аккумулятора к зарядному устройству электроны движутся к отрицательному электроду, нейтрализуя двухвалентные ионы свинца РЬ2+. На электроде выделяется губчатый свинец РЬ. Отдавая под влиянием напряжения внешнего источника тока по два электрона, двухвалентные ионы свинца РЬ2+ у положительного электрода окисляются в четырехвалентные ионы РЬ4+. Через промежуточные реакции ионы РЬ4+ соединяются с двумя ионами кислорода и образуют двуокись свинца РЬO2. Химические реакции в свинцовом аккумуляторе описываются уравнением: содержание в электролите серной кислоты и плотность электролита уменьшаются при разряде и увеличиваются при заряде. По плотности электролита судят о степени разряженности свинцового аккумулятора: где ΔCp — степень разряженности аккумулятора, %;РЗ и Рр — плотность электролита соответственно полностью заряженного и полностью разряженного аккумулятора при температуре 25°С, г/см2;Р25 — измеренная плотность электролита, приведенная к температуре 25°С, г/см3. Расход кислоты у положительных электродов больше, чем у отрицательных. Если учитывать количество воды, образующейся у положительных электродов, то количество кислоты, необходимое для них в течение разряда, в 1,6 раза больше, чем для отрицательных. При разряде происходит незначительное увеличение объема электролита, а при заряде — уменьшение (около 1 см3 на 1 А·ч). На 1 А·ч электрической емкости расходуется: при разряде — свинца 3,86 г, диоксида свинца 4,44 г, серной кислоты 3,67 г, а при заряде — воды 0,672 г, сульфата свинца 11,6 г.
ЩЕЛОЧНЫЕ АККУМУЛЯТОРЫ.
Щелочными аккумуляторами называют такие аккумуляторы, в которых в качестве электролита используется щелочь, например раствор едкого натрия или едкого калия. Электроды (пластины) в щелочных аккумуляторах выполнены из никелированного железа, в которые запрессовывается активная масса. Корпус щелочных аккумуляторов выполняют из никелированного стального листа. В качестве активной массы в щелочных аккумуляторах, к примеру — в кадмиево-никелевых, для положительных пластин используется гидрат закиси никеля в смеси с графитом, а в отрицательных пластинах — кадмий и окись железа. Электролит в щелочных аккумуляторах в процессе работы не расходуется и не меняет своей плотности. Это замечательное свойство позволяет корпус аккумулятора выполнить герметичным. Такая конструкция не требует никакого дополнительного обслуживания, кроме циклических зарядов после разряда. В зависимости от типа применяемой активной массы щелочные аккумуляторы называют: железо-никелевые (окись никеля и железо), кадмиево-никелевые (окись никеля и кадмий), серебряно-цинковые (положительные электроды из чистого серебра, а отрицательные пластины из спрессованной смеси окиси цинка и цинкового порошка, электролит из едкого калия). Основные характеристики аккумуляторов. Основные характеристики у аккумуляторов такие же, как и у гальванических элементов, дополнительные — это зарядная емкость, коэффициент отдачи, срок службы и годности. Зарядная емкость аккумулятора — количество электричества, преобразованного в химическую энергию, накопленную при полном заряде аккумулятора. Коэффициент отдачи, определяется соотношением разрядной емкости к зарядной емкости. Коэффициент отдачи по энергии — отношение энергии, полученной аккумулятором, к энергии, отданной при разряде. Срок службы — наработка по времени, при которой его разрядная емкость сделается меньше определенной нормативной величины. Срок годности аккумулятора — сумма срока хранения и времени эксплуатации, в течение которого наработка аккумулятора достигает срока его службы.
Рекомендуем ознакомиться со следующими материалами:
Как работает аккумулятор — Любопытно
Представьте себе мир без батарей. Все портативные устройства, от которых мы так зависим, были бы настолько ограничены! Мы сможем доставить наши ноутбуки и телефоны настолько далеко, насколько это досягаемо для их кабелей, что сделает это новое работающее приложение, которое вы только что загрузили на свой телефон, практически бесполезным.
К счастью, батарейки у нас есть. Еще в 150 г. до н.э. в Месопотамии парфянская культура использовала устройство, известное как багдадская батарея, сделанное из медных и железных электродов с уксусом или лимонной кислотой.Археологи считают, что на самом деле это не батареи, а в основном они использовались для религиозных церемоний.
Изобретение батареи в том виде, в котором мы ее знаем, приписывают итальянскому ученому Алессандро Вольта, который собрал первую батарею, чтобы доказать свою точку зрения другому итальянскому ученому Луиджи Гальвани. В 1780 году Гальвани показал, что лапы лягушек, подвешенных на железных или латунных крючках, подергиваются при прикосновении к зонду из другого металла. Он считал, что это было вызвано электричеством из тканей лягушек, и называл это «животным электричеством».
Луиджи Гальвани обнаружил, что лапы лягушек, подвешенных на латунных крючках, дергались, когда их ткнули зондом из другого металла. Он думал, что эта реакция была вызвана «животным электричеством» внутри лягушки. Источник изображения: Луиджи Гальвани / Wikimedia Commons.Вольта, первоначально впечатленный открытиями Гальвани, пришел к выводу, что электрический ток исходит от двух разных типов металла (крючки, на которых висели лягушки, и другой металл зонда) и просто передается через них, а не через них. из тканей лягушек.Он экспериментировал со стопками слоев серебра и цинка, перемежаемых слоями ткани или бумаги, пропитанной соленой водой, и обнаружил, что электрический ток действительно протекает через провод, приложенный к обоим концам стопки.
Батарея Алессандро Вольта: куча цинковых и серебряных листов, перемежаемых тканью или бумагой, пропитанной соленой водой. Представьте, что вы используете это для питания вашего телефона. Источник изображения: Луиджи Кьеза / Wikimedia Commons.Volta также обнаружил, что, используя различные металлы в свае, можно увеличить количество напряжения.Он описал свои открытия в письме Джозефу Бэнксу, тогдашнему президенту Лондонского королевского общества, в 1800 году. Это было довольно большое дело (Наполеон был весьма впечатлен!), И его изобретение принесло ему устойчивое признание в честь «вольта». ‘(мера электрического потенциала), названная в его честь.
Я сам, шутя в сторону, поражен тем, как мои старые и новые открытия … чистого и простого электричества, вызванного контактом металлов, могли вызвать такое волнение.Алессандро Вольта
Так что же именно происходило с этими слоями цинка и серебра и с дрожащими лягушачьими лапами?
Химия батареи
Батарея — это устройство, которое накапливает химическую энергию и преобразует ее в электричество.Это известно как электрохимия, а система, лежащая в основе батареи, называется электрохимическим элементом. Батарея может состоять из одной или нескольких (как в оригинальной кучке Вольты) электрохимических ячеек. Каждая электрохимическая ячейка состоит из двух электродов, разделенных электролитом.
Итак, откуда электрохимический элемент получает электричество? Чтобы ответить на этот вопрос, нам нужно знать, что такое электричество. Проще говоря, электричество — это тип энергии, производимый потоком электронов.В электрохимической ячейке электроны образуются в результате химической реакции, которая происходит на одном электроде (подробнее об электродах ниже!), А затем они перетекают на другой электрод, где расходуются. Чтобы понять это правильно, нам нужно внимательнее изучить компоненты клетки и то, как они устроены вместе.
Электроды
Чтобы создать поток электронов, вам нужно где-то, чтобы электроны текли с из , а где-то электроны текли с по .Это электроды ячейки. Электроны текут от одного электрода, называемого анодом (или отрицательным электродом), к другому электроду, называемому катодом (положительный электрод). Как правило, это разные типы металлов или другие химические соединения.
В котле Вольта анодом служил цинк, от которого электроны текли по проволоке (при соединении) с серебром, которое было катодом батареи. Он сложил много этих ячеек вместе, чтобы получилась общая куча, и поднял напряжение.
Но откуда анод вообще берет все эти электроны? И почему они так счастливы, что их отправили в веселый путь к катоду? Все сводится к химии, происходящей внутри клетки.
Нам нужно понять пару химических реакций. На аноде электрод вступает в реакцию с электролитом, образуя электроны. Эти электроны накапливаются на аноде. Между тем, на катоде одновременно происходит другая химическая реакция, которая позволяет этому электроду принимать электроны.
Технический химический термин, обозначающий реакцию, которая включает обмен электронами, — это реакция окисления-восстановления, обычно называемая окислительно-восстановительной реакцией. Вся реакция может быть разделена на две половинные реакции, и в случае электрохимической ячейки одна полуреакция происходит на аноде, а другая — на катоде. Уменьшение — это усиление электронов, и это то, что происходит на катоде; мы говорим, что катод восстанавливается во время реакции. Окисление — это потеря электронов, поэтому мы говорим, что анод окисляется.
Каждая из этих реакций имеет определенный стандартный потенциал. Думайте об этой характеристике как о способности / эффективности реакции либо производить, либо поглощать электроны — ее силу в электронном перетягивании каната.
- Стандартные потенциалы для полуреакций
Ниже приведен список половинных реакций, которые включают высвобождение электронов из чистого элемента или химического соединения. Рядом с реакцией указано число (E 0 ), которое сравнивает силу электрохимического потенциала реакции с силой готовности водорода расстаться со своим электроном (если вы посмотрите вниз по списку, вы увидите, что водородная полуреакция имеет нулевое значение E 0 ).E 0 измеряется в вольтах.
Причина, по которой этот список настолько интересен, заключается в том, что если вы выберете две реакции из списка и объедините их в электрохимическую ячейку, значения E 0 скажут вам, в каком направлении будет протекать общая реакция: реакция с более отрицательной реакцией. Значение E 0 отдает свои электроны другой реакции, и это определяет анод и катод вашей ячейки. Разница между двумя значениями E 0 говорит вам об электрохимическом потенциале вашей ячейки, который в основном представляет собой напряжение ячейки.
Итак, если вы возьмете литий и фторид и сумеете объединить их, чтобы сделать элемент батареи, у вас будет самое высокое напряжение, теоретически достижимое для электрохимического элемента. Этот список также объясняет, почему в котле Вольта цинк был анодом, а серебро — катодом: полуреакция цинка имеет более низкое (более отрицательное) значение E 0 (-0,7618), чем полуреакция серебра (0,7996). .
Источник: UC Davis ChemWiki
Любые два проводящих материала, которые вступают в реакцию с разными стандартными потенциалами, могут образовывать электрохимическую ячейку, потому что более сильный из них сможет забирать электроны у более слабого.Но идеальным выбором для анода был бы материал, который вызывает реакцию со значительно более низким (более отрицательным) стандартным потенциалом, чем материал, который вы выбираете для своего катода. В итоге мы получаем электроны, притягивающиеся к катоду от анода (и анод не очень сильно пытается бороться), и, когда у нас есть легкий путь, чтобы добраться туда — проводящий провод, мы можем использовать их энергию для обеспечения электрического питание нашего фонарика, телефона или чего-то еще.
Разница в стандартном потенциале между электродами как бы равна силе, с которой электроны перемещаются между двумя электродами.Это известно как общий электрохимический потенциал ячейки, и он определяет напряжение ячейки. Чем больше разница, тем больше электрохимический потенциал и выше напряжение.
Чтобы увеличить напряжение аккумулятора, у нас есть два варианта. Мы могли бы выбрать для наших электродов другие материалы, которые придадут ячейке больший электрохимический потенциал. Или мы можем сложить несколько ячеек вместе. Когда элементы объединяются определенным образом (последовательно), это оказывает аддитивное влияние на напряжение батареи.По сути, силу, с которой электроны движутся через батарею, можно рассматривать как общую силу, когда они движутся от анода первого элемента на всем пути, сколько бы ячеек ни содержала батарея, к катоду последнего элемента.
Когда элементы объединяются другим способом (параллельно), это увеличивает возможный ток батареи, который можно рассматривать как общее количество электронов, протекающих через элементы, но не ее напряжение.
Электролит
Но электроды — это всего лишь часть батареи.Помните обрывки бумаги Вольты, пропитанные соленой водой? Соленая вода была электролитом, еще одной важной частью картины. Электролит может быть жидкостью, гелем или твердым веществом, но он должен обеспечивать движение заряженных ионов.
Электронов имеют отрицательный заряд, и поскольку мы посылаем поток отрицательных электронов по нашей цепи, нам нужен способ уравновесить это движение заряда. Электролит обеспечивает среду, через которую могут протекать положительные ионы, уравновешивающие заряд.
Поскольку химическая реакция на аноде производит электроны, для поддержания баланса нейтрального заряда на электроде также производится соответствующее количество положительно заряженных ионов. Они не проходят по внешнему проводу (только для электронов!), А попадают в электролит.
В то же время катод должен также уравновешивать отрицательный заряд электронов, которые он принимает, поэтому реакция, которая здесь происходит, должна втягивать положительно заряженные ионы из электролита (альтернативно, он также может высвобождать отрицательно заряженные ионы из электрода в электролит. электролит).
Итак, в то время как внешний провод обеспечивает путь для потока отрицательно заряженных электронов, электролит обеспечивает путь для переноса положительно заряженных ионов, чтобы уравновесить отрицательный поток. Этот поток положительно заряженных ионов так же важен, как и электроны, обеспечивающие электрический ток во внешней цепи, которую мы используем для питания наших устройств. Роль балансировки заряда, которую они выполняют, необходима для поддержания всей реакции.
Так вот, если бы все ионы, высвобожденные в электролит, могли полностью свободно перемещаться через электролит, они в конечном итоге покрыли бы поверхности электродов и забили бы всю систему.Таким образом, в клетке обычно есть какой-то барьер, чтобы этого не произошло.
При использовании батареи возникает ситуация, когда происходит непрерывный поток электронов (через внешнюю цепь) и положительно заряженных ионов (через электролит). Если этот непрерывный поток остановлен — если цепь разомкнута, например, когда ваш фонарик выключен — поток электронов остановлен. Заряды будут накапливаться / накапливаться, и химические реакции, приводящие в движение аккумулятор, прекратятся.
По мере использования батареи и протекания реакций на обоих электродах возникают новые химические продукты.Эти продукты реакции могут создавать своего рода сопротивление, которое может помешать продолжению реакции с такой же эффективностью. Когда это сопротивление становится слишком большим, реакция замедляется. Электронное перетягивание каната между катодом и анодом также теряет свою силу, и электроны перестают течь. Аккумулятор медленно разряжается.
Зарядка аккумулятора
Некоторые распространенные батареи предназначены только для одноразового использования (так называемые первичные или одноразовые батареи).Электроны перемещаются от анода к катоду в одну сторону. Либо их электроды истощаются по мере того, как они выделяют свои положительные или отрицательные ионы в электролит, либо накопление продуктов реакции на электродах препятствует продолжению реакции, и это делается и вытирается пыль. Батарея оказывается в мусорном ведре (или, надеюсь, на переработку, но это уже другая тема Nova).
Но. Изящная вещь в этом потоке ионов и электронов, который имеет место в некоторых типах батарей с соответствующими материалами электродов, заключается в том, что он также может двигаться в обратном направлении, возвращая нашу батарею в исходную точку и давая ей совершенно новую жизнь. .Подобно тому, как батареи изменили способ использования различных электрических устройств, аккумуляторные батареи еще больше изменили полезность этих устройств и их продолжительность жизни.
Когда мы подключаем почти разряженную батарею к внешнему источнику электричества и отправляем энергию обратно в батарею, происходит обратная химическая реакция, которая произошла во время разряда. Это отправляет положительные ионы, выпущенные из анода, в электролит, обратно к аноду, а электроны, которые катод принимает, также обратно к аноду.Возврат как положительных ионов, так и электронов обратно в анод подготавливает систему, так что она снова готова к работе: ваша батарея заряжена.
Однако процесс не идеален. Замена отрицательных и положительных ионов электролита обратно на соответствующий электрод при перезарядке батареи не такая аккуратная и не такая хорошо структурированная, как электрод вначале. Каждый цикл зарядки еще больше ухудшает состояние электродов, а это означает, что батарея со временем теряет производительность, поэтому даже аккумуляторные батареи не работают вечно.
В течение нескольких циклов зарядки и разрядки форма кристаллов аккумулятора становится менее упорядоченной. Это усугубляется, когда аккумулятор разряжается / заряжается с высокой скоростью — например, если вы едете на электромобиле с большой скоростью, а не с постоянной скоростью. Высокоскоростное переключение приводит к тому, что кристаллическая структура становится более неупорядоченной, что приводит к менее эффективной батарее.
Эффект памяти и саморазряд
Практически, но не полностью обратимые реакции разряда и перезарядки также способствуют так называемому «эффекту памяти».Когда вы перезаряжаете некоторые типы аккумуляторных батарей, не разрядив их сначала, они «запоминают», где находились в предыдущих циклах разрядки, и не перезаряжаются должным образом.
В некоторых элементах это вызвано тем, как металл и электролит реагируют с образованием соли (и тем, как эта соль затем снова растворяется и металл заменяется на электродах при перезарядке). Мы хотим, чтобы наши клетки имели красивые, однородные, маленькие кристаллы соли, покрывающие идеальную металлическую поверхность, но это не то, что мы получаем в реальном мире! Некоторые кристаллы образуются очень сложно, а некоторые металлы откладываются во время перезарядки, поэтому некоторые типы батарей имеют больший эффект памяти, чем другие.Дефекты в основном зависят от первоначального состояния заряда батареи, температуры, напряжения заряда и тока зарядки. Со временем недостатки в одном цикле зарядки могут вызвать то же самое в следующем цикле зарядки и так далее, и наша батарея накапливает некоторые плохие воспоминания. Эффект памяти силен для некоторых типов элементов, таких как батареи на никелевой основе. Другие типы, такие как литий-ионные, не страдают этой проблемой.
Другой аспект аккумуляторных батарей заключается в том, что химический состав, делающий их перезаряжаемыми, также означает, что они имеют более высокую тенденцию к саморазряду.Это когда внутренние реакции происходят внутри аккумуляторного элемента, даже когда электроды не подключены через внешнюю цепь. Это приводит к тому, что клетка со временем теряет часть своей химической энергии. Высокая скорость саморазряда серьезно ограничивает срок службы аккумуляторов — и приводит к их разрядке во время хранения.
Литий-ионные аккумуляторы в наших мобильных телефонах имеют довольно хорошую скорость саморазряда около 2–3 процентов в месяц, и наши свинцово-кислотные автомобильные аккумуляторы также довольно разумны — они, как правило, теряют 4–6 процентов. месяц.Никелевые батареи теряют около 10–15 процентов своего заряда в месяц, что не очень хорошо, если вы планируете хранить фонарик в течение всего сезона, когда он вам не нужен! Неперезаряжаемая щелочная батарея теряет около 2–3% своего заряда в год.
Напряжение, сила тока, мощность, емкость… в чем разница?
Все эти слова в основном описывают мощность батареи, не так ли? Ну вроде как.Но все они немного разные.
Напряжение = сила, при которой реакция, приводящая в движение аккумулятор, проталкивает электроны через элемент. Это также известно как электрический потенциал и зависит от разницы потенциалов между реакциями, которые происходят на каждом из электродов, то есть от того, насколько сильно катод оттянет электроны (через цепь) от анода. Чем выше напряжение, тем больше работы может совершить то же количество электронов.
Ток = количество электронов, которые проходят через любую точку цепи в данный момент времени.Чем выше ток, тем больше работы он может выполнять при том же напряжении. Внутри ячейки ток можно также рассматривать как количество ионов, проходящих через электролит, умноженное на заряд этих ионов.
Мощность = напряжение x ток. Чем выше мощность, тем быстрее батарея может работать — это соотношение показывает, как напряжение и ток важны для определения того, для чего подходит батарея.
Емкость = мощность батареи как функция времени, которая используется для описания продолжительности времени, в течение которого батарея может обеспечивать питание устройства.Аккумулятор большой емкости сможет проработать более длительный период, прежде чем разрядится / разрядится. У некоторых батарей есть небольшая печальная особенность — если вы слишком быстро попытаетесь извлечь из них слишком много энергии, химические реакции не успеют поспеть, и емкость станет меньше! Итак, мы всегда должны быть осторожны, когда говорим о емкости батареи, и помнить, для чего она будет использоваться.
Еще один популярный термин — «плотность энергии». Это количество энергии, которое устройство может удерживать на единицу объема, другими словами, сколько энергии вы получите за свои деньги с точки зрения мощности по сравнению сразмер. С батареей, как правило, чем выше плотность энергии, тем лучше, поскольку это означает, что батарея может быть меньше и компактнее, что всегда является плюсом, когда вам нужно, чтобы она питала то, что вы хотите держать в кармане. Для электромобилей это даже плюс — аккумулятор должен как-то влезать в машину!
Для некоторых приложений, таких как хранение электроэнергии на возобновляемых электростанциях, таких как ветряная или солнечная ферма, высокая плотность энергии не является большой проблемой, поскольку в них, скорее всего, будет достаточно места для хранения батарей.Основная цель такого использования — просто хранить как можно больше электроэнергии, как можно безопаснее и дешевле.
Почему так много типов?
Ряд материалов (раньше это были просто металлы) могут использоваться в качестве электродов в батарее. За прошедшие годы было опробовано множество различных комбинаций, но лишь немногие из них действительно прошли дистанцию.Но зачем вообще использовать разные комбинации металлов? Если у вас есть пара металлов, которые хорошо работают вместе в качестве электродов, зачем возиться с другими?
Различные материалы имеют разные электрохимические свойства, поэтому они дают разные результаты, когда вы соединяете их в аккумуляторном элементе. Например, некоторые комбинации будут производить высокое напряжение очень быстро, но затем быстро падают, не в состоянии поддерживать это напряжение в течение длительного времени. Это хорошо, если вам нужно произвести, скажем, внезапную вспышку света, такую как вспышка фотоаппарата.
Другие комбинации будут производить только тонкую струйку тока, но они будут поддерживать эту струйку целую вечность. Например, нам не нужен большой ток для питания детектора дыма, но мы хотим, чтобы наши детекторы дыма работали долгое время.
Еще одна причина для использования различных комбинаций металлов заключается в том, что часто два или более аккумуляторных элемента необходимо уложить в стопку для получения необходимого напряжения, и оказывается, что некоторые комбинации электродов складываются вместе намного лучше, чем другие комбинации.Например, литий-железо-фосфатные батареи (тип литий-ионных аккумуляторов), используемые в электромобилях, складываются вместе для создания систем высокого напряжения (100 или даже более вольт), но вы никогда не сделаете этого с теми батареями NiCad Walkman, которые имеют горячий!
Наши различные потребности с течением времени привели к разработке огромного количества типов батарей. Чтобы узнать больше о них и о том, что ждет аккумулятор в будущем, ознакомьтесь с другими нашими темами о Nova.
Эта тема является частью нашей серии из четырех статей об аккумуляторах.Для дальнейшего чтения ознакомьтесь с типами аккумуляторов, литий-ионных аккумуляторов и аккумуляторов будущего.Как работают батарейки?
Как работают батарейки?Как работают батарейки?
Электричество, как вы, наверное, уже знаете, это поток электронов. через проводящий путь, как провод. Этот путь называется цепью .
Батареи состоят из трех частей: анода (-), катода (+), и электролит .Катод и анод (положительный и отрицательный стороны на обоих концах традиционной батареи) подключены к электрическому схема.
Химические реакции в батарее вызывают накопление электронов на аноде. Это приводит к электрической разнице между анодом и катод. Вы можете думать об этой разнице как о нестабильном накоплении электроны. Электроны хотят перестроиться, чтобы избавиться от этой разницы.Но они делают это определенным образом. Электроны отталкиваются друг от друга и пытаются уйти в место с меньшим количеством электронов.
В батарее единственное место, куда можно подойти, — это катод. Но электролит не позволяет электронам идти прямо от анода к катоду внутри батареи. Когда цепь замкнута (провод соединяет катод и анод) электроны смогут попасть на катод. На картинке выше электроны проходят по проводу, зажигая лампочку вдоль способ.Это один из способов описания того, как электрический потенциал вызывает появление электронов. протекать по контуру.
Однако эти электрохимические процессы изменяют химические вещества. в аноде и катоде, чтобы они перестали подавать электроны. Итак, есть ограниченное количество энергии, доступной в батарее.
Когда вы перезаряжаете аккумулятор, вы меняете направление потока электронов с помощью другого источника энергии, например солнечных батарей.В электрохимические процессы происходят в обратном порядке, и анод и катод восстанавливаются в исходное состояние и снова может обеспечить полную мощность.
Что есть батареи?
Что это энергия?
Что такое схема?
Что такое электрон?
Что такое поток электронов?
Что такое DS1 срок службы батареи?
Что значит электрически заряженный?
Как атомы заряжены?
Где энергия приходит и уходит?
Инженерная школа Массачусетского технологического института | »Как работает аккумулятор?
Как работает аккумулятор?
Ваши часы, ноутбук и лазерная указка питаются от одного и того же: химии…
Мэри БейтсСуществует много разных типов батарей, но все они работают на основе одной и той же концепции.«Батарея — это устройство, способное накапливать электрическую энергию в форме химической энергии и преобразовывать эту энергию в электричество», — говорит Антуан Алланор, научный сотрудник отдела материаловедения и инженерии Массачусетского технологического института. «Вы не можете улавливать и хранить электричество, но вы можете хранить электрическую энергию в химических веществах внутри батареи».
Батарея состоит из трех основных компонентов: две клеммы, изготовленные из разных химикатов (обычно металлов), анод и катод; и электролит, разделяющий эти выводы.Электролит — это химическая среда, которая обеспечивает прохождение электрического заряда между катодом и анодом. Когда устройство подключено к батарее — лампочке или электрической цепи — на электродах происходят химические реакции, которые создают поток электрической энергии к устройству.
Более конкретно: во время разряда электричества химическое вещество на аноде высвобождает электроны на отрицательный вывод и ионы в электролите в результате так называемой реакции окисления.Между тем, на положительном выводе катод принимает электроны, замыкая цепь для потока электронов. Электролит предназначен для того, чтобы привести различные химические вещества анода и катода в контакт друг с другом таким образом, чтобы химический потенциал мог уравновеситься от одного вывода к другому, преобразовывая накопленную химическую энергию в полезную электрическую энергию. «Эти две реакции происходят одновременно», — говорит Алланор. «Ионы переносят ток через электролит, в то время как электроны текут во внешней цепи, и это то, что генерирует электрический ток.”
Если батарея одноразовая, она будет вырабатывать электричество до тех пор, пока не закончатся реагенты (одинаковый химический потенциал на обоих электродах). Эти батареи работают только в одном направлении, преобразуя химическую энергию в электрическую. Но в других типах аккумуляторов реакция может быть обратной. Перезаряжаемые батареи (например, в вашем мобильном телефоне или в вашем автомобиле) сконструированы таким образом, что электрическая энергия из внешнего источника (зарядное устройство, которое вы подключаете к стене или динамо-машина в вашем автомобиле) может подаваться на химическую систему и наоборот. его работу, восстанавливая заряд аккумулятора.
Лаборатория Group Sadoway в Массачусетском технологическом институте работает над созданием более эффективных батарей для многоцелевого использования. Для крупномасштабного хранения энергии команда работает над жидкометаллической батареей, в которой электролит, анод и катод являются жидкими. Для портативных приложений они разрабатывают тонкопленочные полимерные батареи с гибким электролитом из негорючего геля. Еще одна цель лаборатории — создать батареи с использованием ранее не изученных материалов, уделяя особое внимание распространенным, дешевым и безопасным веществам, которые имеют такой же коммерческий потенциал, как и популярные литиевые батареи.
Спасибо 18-летнему Стивену Минкусу из Гленвью, штат Иллинойс, за этот вопрос.
Отправлено: 1 мая 2012 г.
Типы батарей / источники питания: принципы работы и преимущества
Батареи — наиболее распространенный источник питания для основных портативных устройств и крупномасштабных промышленных приложений. Батарею можно определить как; это комбинация одной или нескольких электрохимических ячеек, которые способны преобразовывать накопленную химическую энергию в электрическую.
Работа батареи:
Батарея — это устройство, которое состоит из различных гальванических элементов. Каждый гальванический элемент состоит из двух полуэлементов, соединенных последовательно проводящим электролитом, содержащим анионы и катионы. Одна полуячейка включает электролит и электрод, к которому перемещаются анионы, то есть анод или отрицательный электрод; другая полуячейка включает электролит и электрод, к которому движутся катионы, то есть катод или положительный электрод.
В окислительно-восстановительной реакции, которая приводит в действие аккумулятор, происходит восстановление катионов на катоде, в то время как окисление происходит до анионов на аноде.Электроды не касаются друг друга, а электрически связаны электролитом. В основном полуэлементы имеют разные электролиты. Учитывая все обстоятельства, каждая полуячейка заключена в контейнер, а сепаратор, пористый для ионов, но не большая часть электролитов, предотвращает смешивание.
Работа батареиКаждая половина элемента имеет электродвижущую силу (ЭДС), определяемую ее способностью передавать электрический ток изнутри во внешнюю часть элемента. Чистая ЭДС ячейки — это разница между ЭДС ее полуячеек.Таким образом, если электроды имеют ЭДС, иными словами, чистая ЭДС представляет собой разность восстановительных потенциалов полуреакций.
Как ухаживать за аккумулятором?
Чтобы поддерживать аккумулятор в хорошем состоянии, необходимо выравнивание заряда аккумулятора. Из-за старения все элементы заряжаются по-разному, некоторые элементы заряжаются очень быстро, а другие заряжаются постепенно. Выравнивание может быть выполнено путем небольшой перезарядки аккумулятора, чтобы позволить более слабым элементам также полностью зарядиться.Напряжение на клеммах полностью заряженной батареи составляет 12 В, автомобильная батарея показывает 13,8 В на клеммах, а 12-вольтовая трубчатая батарея — 14,8 В. Автомобильный аккумулятор должен быть надежно закреплен в автомобиле, чтобы избежать тряски. Батарею инвертора следует по возможности поставить на деревянную доску.
2 типа батарей
1) Основные батареи:
Как видно из названия, эти батареи предназначены для одноразового использования. После того, как эти батареи используются, их нельзя перезарядить, так как устройства не могут быть легко восстановлены, и активные материалы могут не вернуться к своей первоначальной форме.Производители батарей не рекомендуют перезаряжать первичные элементы.
Некоторыми примерами одноразовых батареек являются обычные батарейки AA, AAA, которые мы используем в настенных часах, пультах дистанционного управления от телевизора и т. Д. Другое название этих батарей — одноразовые батарейки. Типы
Батарея2) Вторичные батареи:
Вторичные батареи также называются аккумуляторными батареями. Эти батареи можно использовать и заряжать одновременно. Обычно они собираются с активными материалами, причем активный элемент находится в разряженном состоянии.Перезаряжаемые батареи заряжаются с помощью электрического тока, который обращает вспять химические реакции, происходящие во время разряда. Зарядные устройства — это устройства, обеспечивающие необходимый ток.
Некоторыми примерами таких аккумуляторных батарей являются батареи, используемые в мобильных телефонах, MP3-плеерах и т. Д. В таких устройствах, как слуховые аппараты и наручные часы, используются миниатюрные элементы, а в таких местах, как телефонные станции или компьютерные центры обработки данных, используются батареи большего размера.
Вторичные батареиТипы вторичных (перезаряжаемых) батарей:
SMF, свинцово-кислотные, Li и Nicd
SMF батареи:
SMF — это герметичные необслуживаемые батареи , обеспечивающие надежную, постоянную и низкую потребность в техническом обслуживании. Приложения ИБП.Эти батареи могут подвергаться глубокому разряду и минимальному техническому обслуживанию в сельской местности и в районах с дефицитом электроэнергии. Эти батареи доступны от 12 В.
В современном информационном мире нельзя упускать из виду требование к аккумуляторным системам, предназначенным для восстановления важных квалифицированных данных и информации и запуска основных контрольно-измерительных приборов в течение желаемого времени. Батареи необходимы для мгновенной подачи энергии. Ненадежные и некачественные батареи могут привести к потере данных и отключению оборудования, что может стоить компаниям значительных финансовых потерь.Следовательно, сегменты ИБП требуют использования надежной и проверенной аккумуляторной системы.
Батарея SMFЛитиевая (Li) батарея:
Все мы используем ее в портативных устройствах, таких как сотовый телефон, портативный компьютер или электроинструмент. Литиевая батарея была одним из величайших достижений портативной энергетики за последнее десятилетие; Благодаря использованию литиевых батарей мы смогли перейти с черно-белых мобильных телефонов на цветные с дополнительными функциями, такими как GPS, оповещения по электронной почте и т. д.Это устройства с потенциалом высокой плотности энергии для более высоких мощностей. И относительно невысокий саморазряд аккумуляторов. Также специальные элементы могут обеспечивать очень высокий ток для таких приложений, как электроинструменты.
Li-батареяНикель-кадмиевая (Nicd) батарея:
Никель-кадмиевые батареи имеют то преимущество, что их можно перезаряжать много раз, они обладают относительно постоянным потенциалом во время разряда и имеют большую электрическую и физическую стойкость. В этой батарее используется оксид никеля для катода, соединение кадмия для анода и раствор гидроксида калия в качестве электролита.
Когда аккумулятор заряжается, химический состав катода изменяется, и гидроксид никеля превращается в NIOOH. В аноде образование ионов кадмия происходит из гидроксида кадмия. Когда аккумулятор разряжен, кадмий реагирует с NiOOH с образованием гидроксида никеля и гидроксида кадмия.
Cd + 2h3O + 2NiOOH -> 2Ni (OH) 2 + Cd (OH) 2
Свинцово-кислотная батарея:
Свинцово-кислотные батареишироко используются в автомобилях, инверторах, системах резервного питания и т. Д.В отличие от трубчатых и необслуживаемых батарей, свинцово-кислотные батареи требуют надлежащего ухода и обслуживания для продления срока их службы. Свинцово-кислотная батарея состоит из ряда пластин, погруженных в раствор серной кислоты. Пластины имеют решетки, на которые крепится активный материал. Пластины делятся на положительные и отрицательные. Положительные пластины содержат чистый свинец в качестве активного материала, в то время как оксид свинца прикреплен к отрицательным пластинам.
Свинцово-кислотная батареяПолностью заряженная батарея может разрядить ток при подключении к нагрузке.В процессе разряда серная кислота соединяется с активными материалами на положительной и отрицательной пластинах, что приводит к образованию сульфата свинца. Вода — самый важный шаг в обслуживании свинцово-кислотной батареи. Периодичность подачи воды зависит от использования, способа зарядки и рабочей температуры. Во время процесса атомы водорода серной кислоты реагируют с кислородом с образованием воды.
Это приводит к высвобождению электронов из положительных пластин, которые будут приняты отрицательными пластинами.Это приводит к образованию электрического потенциала на батарее. Электролит в свинцово-кислотной батарее представляет собой смесь серной кислоты и воды, имеющую удельный вес. Удельный вес — это вес кислотно-водной смеси по сравнению с равным объемом воды. Удельный вес чистой воды, не содержащей ионов, составляет 1.
Свинцово-кислотные батареи обеспечивают наилучшее соотношение мощности и энергии на киловатт-час; имеют самый продолжительный жизненный цикл и большое экологическое преимущество, поскольку они перерабатываются с чрезвычайно высокой скоростью.Никакая другая химия не может коснуться инфраструктуры, которая существует для сбора, транспортировки и переработки свинцово-кислотных аккумуляторов.
Наряду с этой статьей обсуждается литий-ионный аккумулятор, его достоинства и недостатки.
Работа литий-ионных аккумуляторов
Литий-ионные аккумуляторы сейчас популярны в большинстве портативных электронных устройств, таких как мобильные телефоны, ноутбуки, цифровые фотоаппараты и т. Д., Благодаря их длительной энергоэффективности. Это самые популярные аккумуляторные батареи с такими преимуществами, как лучшая плотность энергии, незначительные потери заряда и отсутствие эффекта памяти.Литий-ионный аккумулятор использует ионы лития в качестве носителей заряда, которые перемещаются от отрицательного электрода к положительному во время разряда и обратно при зарядке. Во время зарядки внешний ток от зарядного устройства вызывает перенапряжение, чем в аккумуляторе. Это заставляет ток проходить в обратном направлении от положительного электрода к отрицательному, где ионы лития внедряются в пористый электродный материал в результате процесса, называемого интеркаляцией. Ионы лития проходят через неводный электролит и разделительную диафрагму.Материал электрода — интеркалированное соединение лития.
Отрицательный электрод литий-ионной батареи состоит из углерода, а положительный электрод — из оксида металла. Чаще всего для отрицательного электрода используется графит, а для положительного электрода — оксид лития-кобальта, литий-ионный фосфат или оксид лития-марганца. Литиевая соль в органическом растворителе используется в качестве электролита. Электролит обычно представляет собой смесь органических карбонатов, таких как этиленкарбонат или диэтилкарбонат, содержащих ионы лития.В электролите используются анионные соли, такие как гексафторфосфат лития, моногидрат гексафторарсената лития, перхлорат лития, гексафторборат лития и т. Д. В зависимости от используемой соли напряжение, емкость и срок службы батареи различаются. Чистый литий бурно реагирует с водой с образованием гидроксида лития и ионов водорода. Таким образом, в качестве электролита используется неводный органический растворитель. Электрохимическая роль заряда электродов между анодом и катодом зависит от направления тока.
Реакция ионно-литиевой батареиВ литий-ионной батарее оба электрода могут принимать и выделять ионы лития. Во время процесса интеркаляции ионы лития перемещаются в электрод. Во время обратного процесса, называемого деинтеркаляцией, ионы лития возвращаются. Во время разряда положительные ионы лития извлекаются из отрицательных электродов и вставляются в положительный электрод. В процессе зарядки происходит обратное движение ионов лития.
Преимущества литий-ионных аккумуляторов:
Литий-ионные аккумуляторы превосходят никель-кадмиевые аккумуляторы и другие вторичные аккумуляторы.Некоторые из преимуществ:
- Легкий вес по сравнению с другими батареями аналогичного размера.
- Доступны в другой форме, включая плоскую.
- Высокое напряжение холостого хода, которое увеличивает передачу мощности при низком токе.
- Отсутствие эффекта памяти.
- Очень низкая скорость саморазряда 5-10% в месяц. Саморазряд составляет около 30% в никель-кадмиевых и никель-металлгидридных батареях.
- Экологичный аккумулятор без свободного металлического лития
Но наряду с преимуществами, как и у других аккумуляторов, литий-ионный аккумулятор также страдает некоторыми недостатками.
Недостатки литий-ионного аккумулятора:
- Отложения внутри электролита со временем будут препятствовать прохождению заряда. Это увеличивает внутреннее сопротивление батареи, и способность элемента передавать ток постепенно уменьшается.
- Высокая зарядка и высокая температура могут привести к потере емкости.
- При перегреве литий-ионная аккумуляторная батарея может подвергнуться тепловому уходу и разрушению элемента.
- Глубокая разрядка может привести к короткому замыканию литий-ионного аккумулятора. Поэтому, чтобы предотвратить это, некоторые производители имеют внутреннюю схему отключения, которая отключает аккумулятор, когда его напряжение превышает безопасный уровень от 3 до 4.2 вольта. В этом случае, когда аккумулятор не используется в течение длительного времени, внутренняя схема будет потреблять энергию и разряжать аккумулятор ниже напряжения отключения. Так что для зарядки таких аккумуляторов обычные зарядные устройства не пригодятся.
Как работает автомобильный аккумулятор
Свинцово-кислотный автомобильный аккумулятор на 12 В. Эти большие и довольно тяжелые батареи используются в каждом автомобиле с двигателем внутреннего сгорания на планете. Они являются неотъемлемой частью автомобиля. Итак, что он делает и как работает? Это то, о чем мы расскажем в этой статье, спонсируемой Squarespace.Зайдите на squarespace.com, чтобы начать бесплатную пробную версию, или воспользуйтесь набором идей разработки кода, чтобы сэкономить 10% на сайтах и доменах.
Прокрутите вниз, чтобы просмотреть руководство по YouTube.
Что такое автомобильный аккумулятор?
Свинцово-кислотный аккумуляторАвтомобильный аккумулятор на 12 В выглядит примерно так.
Это свинцово-кислотный аккумулятор. Мы называем это свинцово-кислотной батареей, потому что внутри устройства находятся свинцовые пластины, погруженные в кислоту. Это создает химическую реакцию, которая высвобождает энергию и дает нам напряжение и ток.
Химическая реакцияТаким образом, аккумулятор накапливает энергию в виде химической энергии. Не хранит электричество. Эта химическая энергия преобразуется в электрическую, когда нам это нужно. Эта батарея также является перезаряжаемой, если мы подадим в батарею электричество, тогда мы сможем обратить вспять химическую реакцию и перезарядить батарею.
Зарядка с помощью генератора переменного токаЭти типы батарей могут обеспечивать большой ток, особенно по сравнению с типичными бытовыми щелочными батареями меньшего размера.
Мы рассмотрели, как работают щелочные батареи в нашей предыдущей статье, посмотрите ЗДЕСЬ.
Почему в автомобиле используется аккумулятор?
Типичный автомобильный аккумулятор находится в моторном отсеке автомобиля. Аккумулятор сначала используется для запуска двигателя, и он делает это, обеспечивая электричеством небольшой электродвигатель, известный как стартер. Он также подает электричество в систему зажигания, чтобы начать сгорание топлива.
Стартер включает небольшую шестерню на маховик двигателя.Он поворачивает коленчатый вал, который запускает двигатель внутреннего сгорания, после этого малая шестерня выключается, и двигатель запускается сам по себе. Стартер должен обеспечивать огромное усилие, чтобы вращать маховик, поэтому стартер будет потреблять очень большой ток, возможно, сотни ампер, но всего в течение нескольких секунд. Этот большой ток приведет к уменьшению энергии, хранящейся в батарее. Так что нам нужно снова пополнить его.
СтартерК двигателю подключен генератор переменного тока.Генератор приводится во вращение двигателем и вырабатывает электричество. Он возвращается в аккумулятор для его подзарядки.
ГенераторПока двигатель работает, генератор подзаряжает аккумулятор, но он также обеспечивает электроэнергией такие вещи, как освещение и музыкальная система. Когда потребность в электричестве превышает то, что может обеспечить генератор, аккумулятор обеспечивает дополнительную мощность, которая снова разряжает аккумулятор.
Если двигатель выключен, генератор перестанет вращаться и перезаряжать аккумулятор, поэтому аккумулятор будет обеспечивать полную электрическую мощность до тех пор, пока он не разрядится.На данный момент аккумулятор не может обеспечить достаточно электричества для запуска двигателя, поэтому нам нужно запустить машину от внешнего источника.
Основные части
Давайте взглянем на основные части автомобильного аккумулятора и поймем, как он работает.
Прежде всего, у нас есть пластиковый корпус, в котором собраны все внутренние компоненты. Сверху у нас есть пластиковая крышка и два вывода, положительный и отрицательный, которые называются клеммами.
Сняв крышку, мы можем заглянуть внутрь.Обратите внимание, что корпус разделен на 6 отдельных камер, каждая из которых разделена пластиковой стенкой. Каждая камера называется ячейкой. Каждая ячейка вырабатывает около 2,1 В постоянного или постоянного тока. Каждая ячейка соединена последовательно, отрицательная часть одной ячейки соединена с плюсом следующей ячейки, что дает нам общее напряжение около 12,6 В.
6 отдельных камерЭто то же самое, как если бы вы соединяли бытовые щелочные батареи вместе, их напряжения складываются вместе, чтобы обеспечить более высокое общее напряжение.
Каждая ячейка в батарее соединена с помощью пластинчатой ленты, которая сделана из свинца. Они свариваются через пластиковую стенку, образуя соединение.
Когда мы смотрим на батарею с этой точки зрения, мы видим, что ток течет через элементы батареи от положительного к отрицательному, и это с использованием традиционной теории тока. На самом деле происходит то, что электроны текут в противоположном направлении от отрицательного к положительному. Но мы поговорим об этом немного позже в статье.
Обратите внимание, что в каждой ячейке есть две планки для планшетов. Один положительный и один отрицательный. Они называются пластинчатыми лентами, потому что каждая полоса соединена с несколькими пластинами, которые представляют собой листы свинца.
Пластины имеют решетчатую структуру, увеличивающую площадь поверхности. Сетки покрыты пастой из оксида свинца. Паста — это место, где происходит химическая реакция, и мы увидим это чуть позже в статье. Паста действует как губка и впитывает часть электролитной жидкости, что улучшает характеристики аккумулятора.Размер пластины определяет, какой ток может обеспечить батарея, но не меняет напряжение. Используемые материалы и количество пластин определяют напряжение, создаваемое каждой ячейкой. Сетка удерживает пасту на месте, чтобы обеспечить равномерное распределение тока по пластине и помогает транспортировать электроны из батареи по электрической цепи.
Отрицательная пластина — это анод, и это пластина из чистого свинца, хотя небольшое количество добавок добавлено для упрочнения свинца и защиты его от коррозии.Положительная пластина — это катод, сделанный из оксида свинца. Пластины сделаны из разнородных материалов, которые образуют химическую реакцию и высвобождают электроны. Однако мы не хотим, чтобы положительная и отрицательная пластины соприкасались друг с другом, это может привести к короткому замыканию аккумулятора. Поэтому вместо этого мы помещаем каждую положительную пластину в разделитель конвертов. Это пористый материал, который позволяет ионам проходить сквозь него без прямого контакта материалов друг с другом.
Положительная пластинаПоложительная и отрицательная пластины располагаются между собой с небольшим зазором между ними.Затем камера заполняется жидким электролитом, состоящим из серной кислоты и воды. Следовательно, аккумулятор называется свинцово-кислотным аккумулятором.
Положительные и отрицательныеОсновы электроэнергетики
Мы хотим кратко рассказать об основах электричества, чтобы вы поняли, как работает аккумулятор в следующей части.
ЭлектроныЭлектричество — это поток электронов в цепи. Нам нужно, чтобы много электронов текло в одном направлении через провод, чтобы мы могли размещать на пути электронов предметы, например, лампочки.Электроны должны пройти через это, и при этом они излучают свет. Когда много электронов течет в одном направлении, хорошо называть это током.
АтомыКаждый материал состоит из атомов. Атомы имеют разное количество протонов, нейтронов и электронов, что и отличает материал. Некоторые материалы, такие как медь, имеют электрон, который может свободно перемещаться к другим атомам. Если мы подключим источник питания, например аккумулятор, к медному проводу, напряжение подтолкнет электроны, и они устремятся к положительной клемме аккумулятора.
Мы сказали, что электроны текут от отрицательного к положительному. Это называется потоком электронов, это теория о том, как работает электричество, и о том, что происходит на самом деле. Но, возможно, вы привыкли видеть обычный ток, который изменяется от положительного к отрицательному, это первоначальная теория, известная как обычный ток. Это было ошибочно доказано Джозефом Томпсоном, который открыл электрон и обнаружил, что они текут от отрицательного к положительному.
Джозеф ТомпсонОднако мы до сих пор используем традиционную теорию тока при проектировании электрических цепей.Если мы посмотрим на эту простую схему, мы всегда должны предположить, что ток течет от положительного к отрицательному, но инженеры и ученые знают, что электроны на самом деле текут в противоположном направлении. Используемые нами электрические формулы будут давать одни и те же ответы независимо от того, в каком направлении течет электричество, так что на самом деле это не имеет значения.
Постоянный токЕсть два типа электричества: постоянный ток, который мы получаем от батарей. Электроны в этом типе выталкиваются в одном направлении.Это называется постоянным током. Думайте об этом, как о воде, текущей по реке. Другой тип электричества — это переменный или переменный ток, который вы получаете от электрических розеток в своих домах. В этом типе электроны постоянно толкаются и тянутся вперед и назад. Думайте об этом типе как о приливе и отливе моря.
Переменный токКогда мы смешиваем вместе определенные материалы, мы можем вызвать химические реакции. Это когда атомы одного материала взаимодействуют с атомами другого материала.Во время этого взаимодействия атомы будут связываться или распадаться. Электроны также могут быть освобождены или захвачены атомами во время реакции.
Химическая реакцияКогда мы говорим об атомах, вы обычно слышите термин ион. Ион — это атом, у которого неравное количество протонов или электронов. Атом имеет нейтральное изменение, когда у него одинаковое количество протонов и электронов, потому что протоны положительно изменены, а электроны заряжены отрицательно, поэтому они уравновешиваются. Если в атоме больше электронов, чем протонов, то это отрицательный ион.Если в атоме протонов больше, чем электронов, это положительный ион.
IonКак это работает
Вместо того, чтобы пытаться понять эту сложную конструкцию, мы собираемся упростить ее до этой простой модели ячейки с одним катодом и анодом.
В этой ячейке находится жидкий электролит, состоящий на 1/3 серной кислоты и 2/3 воды.
У нас есть положительный электрод, который является катодом, он сделан из оксида свинца (PbO 2 )
У нас есть положительный электрод, который является анодом, он сделан из чистого свинца (Pb)
Катод и анодКогда эти материалы объединить, мы получим небольшую химическую реакцию между атомами.Мы покажем атомы этих материалов этими цветными сферами.
Положительный катодный вывод оксида свинца (PbO 2 ) будет реагировать с сульфатом (SO 4 -2 ) в электролите, это сформирует слой сульфата свинца (PbSO4) на катодном выводе. . Во время этой реакции ион кислорода (O 2 -2 ) выбрасывается с катода в электролит. Попадая в электролит, эти ионы кислорода объединяются с ионами водорода (H +) с образованием воды (H 2 O).
В то же время атомы свинца на аноде будут реагировать с ионами сульфата (SO 4 -2 ) в электролите. Эта реакция приведет к образованию слоя сульфата свинца (PbSO 4 ) вокруг электрода. Во время этой реакции два электрона высвобождаются и собираются на отрицательной клемме.
Итак, теперь у нас есть скопление электронов на отрицательной клемме. Поскольку электроны заряжены отрицательно, это означает, что у нас есть разница в заряде на двух клеммах, и мы можем измерить это с помощью вольтметра или мультиметра.
Если вы думаете о магните, противоположные концы притягиваются, а одинаковые концы отталкиваются. Электроны заряжены отрицательно, поэтому они отталкиваются друг от друга и притягиваются к положительному полюсу, на котором меньше электронов. Но они не могут этого достичь. Если мы обеспечим путь для электронов, например, провод, то электроны будут проходить через него, чтобы добраться до положительного вывода. Затем мы можем поместить на пути этих электронов такие предметы, как лампу, и использовать их для выполнения такой работы, как освещение лампы.
Пока существует путь, химическая реакция продолжается, но это не будет длиться вечно. Химические вещества, необходимые для реакции, закончатся. Кислота становится разбавленной и более слабой, и наложения сульфата свинца покрывают оба электрода, это означает, что материалы становятся более похожими, и поэтому химическая реакция становится труднее.
Но, к счастью, эта химическая реакция может быть обращена вспять, поэтому, если мы запитаем батарею электричеством от генератора переменного тока, мы можем начать обратную реакцию.
Может обратная реакцияЭлектроны входят в отрицательную клемму и снова соединяются с сульфатом свинца, высвобождая сульфат в электролит, оставляя только свинец на отрицательной пластине. Ионы сульфата попадают в электролит и объединяются с ионом водорода, высвобождая ион кислорода, так что кислота электролита становится сильнее. Ион кислорода соединяется со свинцом, образуя оксид свинца, который высвобождает сульфат обратно в электролит, снова делая его сильнее.
Если мы оставим батарею полностью разряжаться слишком долго или слишком много раз, будет очень трудно обратить вспять химическую реакцию.Кроме того, слой сульфата может оторваться от электродов и акклиматизироваться на дне батареи, что означает, что он больше не участвует в химической реакции, поэтому батарею необходимо отремонтировать или заменить.
Итак, когда мы смотрим на батарею, эта химическая реакция происходит между каждой пластиной в каждой ячейке, чтобы обеспечить ток в сотни ампер для запуска стартера, а также обеспечить напряжение для питания фонарей и т. Д. Затем он перезаряжается с помощью генератор.
Проверка автомобильного аккумулятора мультиметром
Чтобы проверить напряжение автомобильного аккумулятора, мы просто переключаемся на настройку постоянного напряжения на нашем мультиметре, а затем подключаем красный провод к положительному, а черный провод к отрицательному. Мы должны увидеть напряжение около 12,6 В, если оно ниже 12, значит, батарея не работает должным образом.
Двигатель выключенКогда мы заводим автомобиль, напряжение падает, потому что стартер потребляет большой ток. Напряжение упадет примерно до 11 вольт, если оно упадет ниже примерно 10 вольт, аккумулятор не работает должным образом.
Запуск двигателяПосле запуска двигателя генератор переменного тока должен вырабатывать электричество, поэтому мы должны увидеть более высокое напряжение около 14 вольт, потому что генератор перезаряжает батарею, и напряжение должно быть выше, чтобы помочь вернуть электроны и обратная химическая реакция.
Engine RunningНо теперь, когда вы все заряжены, зайдите на сайт squarespace.com, чтобы создать свое собственное присутствие в Интернете, наполненное функциями, позволяющими людям запускать, публиковать и продвигать свои собственные проекты.
Существуют мощные инструменты для ведения блога, позволяющие демонстрировать фотографии, видео и новости о ваших проектах.
Вы можете легко запланировать встречи на занятиях и занятия с членами команды и клиентами с помощью встроенного инструмента. И вы даже можете собирать платежи или пожертвования, чтобы поддержать свое дело.
Зайдите на squarespace.com, чтобы получить бесплатную пробную версию, а когда будете готовы к запуску, перейдите на squarespace.com/engineeringmindset, чтобы сэкономить 10% на первой покупке веб-сайта или домена.
Как работают батареи? | Живая наука
Батарейки везде. Современный мир зависит от этих портативных источников энергии, которые можно найти во всем: от мобильных устройств до слуховых аппаратов и автомобилей.
Но, несмотря на то, что они широко используются в повседневной жизни людей, батареям часто не уделяют должного внимания. Подумайте об этом: вы действительно знаете, как работает аккумулятор? Не могли бы вы объяснить это кому-нибудь другому?
Вот краткое изложение научных данных об источниках энергии для смартфонов, электромобилей, кардиостимуляторов и многого другого.[Тест: электрические и газовые автомобили]
Анатомия аккумулятора
Большинство аккумуляторов состоят из трех основных частей: электродов, электролита и сепаратора, по словам Энн Мари Састри, соучредителя и генерального директора Sakti3, базирующейся в Мичигане. запуск аккумуляторных технологий.
В каждой батарее по два электрода. Оба изготовлены из токопроводящих материалов, но выполняют разные функции. Один электрод, известный как катод, подключается к положительному концу батареи и является местом, где электрический ток выходит (или электроны входят) в батарею во время разряда, когда батарея используется для питания чего-либо.Другой электрод, известный как анод, подключается к отрицательному полюсу батареи и является местом, где электрический ток входит (или электроны покидают) батарею во время разряда.
Между этими электродами, а также внутри них находится электролит. Это жидкое или гелеобразное вещество, содержащее электрически заряженные частицы или ионы. Ионы соединяются с материалами, из которых состоят электроды, производя химические реакции, которые позволяют батарее генерировать электрический ток.[Взгляд изнутри на работу батарей (инфографика)]
Типичные батареи питаются за счет химической реакции. [См. Полную инфографику] (Изображение предоставлено Карлом Тейтом, художником по инфографике)Последняя часть батареи, разделитель, довольно проста. Роль сепаратора состоит в том, чтобы удерживать анод и катод отдельно друг от друга внутри батареи. По словам Састри, без разделителя два электрода соприкоснутся, что приведет к короткому замыканию и нарушит нормальную работу батареи.
Как это работает
Чтобы представить себе, как работает батарейка, представьте, как вы вставляете щелочные батарейки, такие как двойные AA, в фонарик. Когда вы вставляете эти батарейки в фонарик, а затем включаете его, на самом деле вы замыкаете цепь. Сохраненная в батарее химическая энергия преобразуется в электрическую, которая выходит из батареи в основание лампы фонарика, заставляя ее загораться. Затем электрический ток снова входит в батарею, но на противоположном конце от того места, где он выходил изначально.
Все части батареи работают вместе, чтобы фонарик загорелся. Электроды в батарее содержат атомы определенных проводящих материалов. Например, в щелочной батарее анод обычно изготавливается из цинка, а диоксид марганца действует как катод. Электролит между этими электродами и внутри них содержит ионы. Когда эти ионы встречаются с атомами электродов, между ионами и атомами электродов происходят определенные электрохимические реакции.
Серия химических реакций, протекающих в электродах, вместе известна как окислительно-восстановительные (окислительно-восстановительные) реакции.В батарее катод известен как окислитель, потому что он принимает электроны от анода. Анод известен как восстановитель, потому что он теряет электроны.
В конечном итоге эти реакции приводят к потоку ионов между анодом и катодом, а также к освобождению электронов от атомов электрода, — сказал Састри.
Эти свободные электроны собираются внутри анода (нижняя плоская часть щелочной батареи). В результате два электрода имеют разные заряды: анод становится отрицательно заряженным, когда высвобождаются электроны, а катод становится положительно заряженным, поскольку электроны (которые заряжены отрицательно) поглощаются.Эта разница в заряде заставляет электроны двигаться к положительно заряженному катоду. Однако у них нет возможности попасть внутрь батареи, потому что разделитель не позволяет им сделать это.
Когда вы щелкаете выключателем на фонарике, все меняется. У электронов теперь есть путь к катоду. Но сначала они должны пройти через основание лампы фонарика. Схема замыкается, когда электрический ток снова входит в батарею через верхнюю часть батареи у катода.
Перезаряжаемые и неперезаряжаемые
Для первичных батарей, таких как батареи фонарика, реакции, питающие батарею, в конечном итоге прекратятся, а это означает, что электроны, которые обеспечивают батарею ее зарядом, больше не будут создавать электрический ток. Когда это происходит, аккумулятор разряжен или «мертв», — сказал Састри.
Вы должны выбросить такие батареи, потому что электрохимические процессы, которые заставили батарею производить энергию, не могут быть обращены вспять, объяснил Састри.Однако электрохимические процессы, происходящие во вторичных или перезаряжаемых батареях, можно обратить вспять, подав в батарею электрическую энергию. Например, это происходит, когда вы подключаете аккумулятор мобильного телефона к зарядному устройству, подключенному к источнику питания.
Некоторые из наиболее распространенных используемых сегодня вторичных батарей — это литий-ионные (литий-ионные) батареи, от которых питается большинство бытовых электронных устройств. Эти батареи обычно содержат угольный анод, катод из диоксида лития-кобальта и электролит, содержащий соль лития в органическом растворителе.Другие перезаряжаемые батареи включают никель-кадмиевые (NiCd) и никель-металлогидридные (NiMH) батареи, которые можно использовать в таких вещах, как электромобили и беспроводные электроинструменты. Свинцово-кислотные (Pb-кислотные) батареи обычно используются в автомобилях и других транспортных средствах для запуска, освещения и зажигания.
Все эти аккумуляторные батареи работают по одному и тому же принципу, сказал Састри: когда вы подключаете батарею к источнику питания, поток электронов меняет направление, и анод и катод возвращаются в исходное состояние.[10 лучших подрывных технологий]
Battery lingo
Хотя все батареи работают более или менее одинаково, разные типы батарей имеют разные характеристики. Вот несколько терминов, которые часто встречаются при любом обсуждении батарей:
Напряжение : Когда дело доходит до батарей, напряжение — также известное как номинальное напряжение ячейки — описывает величину электрической силы или давления, при которой свободные электроны — переходите от положительного полюса батареи к отрицательному, — пояснил Састри.В батареях с более низким напряжением ток выходит из батареи медленнее (с меньшей электрической силой), чем в батареях с более высоким напряжением (с большей электрической силой). Батареи в фонарике обычно имеют напряжение 1,5 В. Однако, если фонарик использует две батареи последовательно, эти батареи или элементы имеют общее напряжение 3 вольта.
Свинцово-кислотные батареи, подобные тем, которые используются в большинстве неэлектрических автомобилей, обычно имеют напряжение 2,0 вольт. Но обычно в автомобильном аккумуляторе последовательно соединено шесть таких элементов, поэтому вы, вероятно, слышали, что такие аккумуляторы называются 12-вольтовыми батареями.
Литий-кобальтооксидные батареи — наиболее распространенный тип литий-ионных батарей, используемых в бытовой электронике — имеют номинальное напряжение около 3,7 вольт, сказал Састри.
Ампер : Ампер или ампер — это мера электрического тока или количества электронов, которые проходят через цепь в течение определенного периода времени.
Емкость : Емкость, или емкость элемента, измеряется в ампер-часах, то есть количество часов, в течение которых батарея может подавать определенное количество электрического тока, прежде чем ее напряжение упадет ниже определенного порога, согласно сообщению Райса. Кафедра электротехники и вычислительной техники университета.
9-вольтовая щелочная батарея, используемая в портативных радиоприемниках, рассчитана на 1 ампер-час, что означает, что эта батарея может непрерывно обеспечивать один ампер тока в течение 1 часа, прежде чем она достигнет порогового значения напряжения и будет считаться разряженной.
Плотность мощности : Плотность мощности описывает количество энергии, которое батарея может выдать на единицу веса, сказал Састри. По словам Састри, для электромобилей важна плотность мощности, потому что она показывает, насколько быстро автомобиль может разогнаться от 0 до 60 миль в час (97 км / ч).Инженеры постоянно пытаются найти способы уменьшить размеры батарей без уменьшения их удельной мощности.
Плотность энергии : Плотность энергии описывает, сколько энергии способна отдать батарея, деленное на ее объем или массу, сказал Састри. Это число соответствует вещам, которые имеют большое влияние на пользователей, например, сколько времени вам нужно пройти, прежде чем зарядить мобильный телефон, или как далеко вы можете проехать на электромобиле, прежде чем остановиться, чтобы подключить его. techEpalermo .Подпишитесь на Live Science @livescience , Facebook и Google+ .
Дополнительные ресурсы
Как работает литий-ионная батарея?
Представьте себе мир без литий-ионных батарей (часто называемых литий-ионными батареями или LIB ). Нужна помощь? Мобильные устройства не будут выглядеть так, как сейчас. Представьте себе огромные, тяжелые сотовые телефоны и ноутбуки. Также представьте, что обе эти вещи настолько дороги, что их могут себе позволить только очень богатые люди.Вы представляете 1980-е. Страшно, правда?
Литий-ионные батареиЗнаете ли вы?
Литий-ионные батареи были впервые произведены и произведены компанией SONY в 1991 году.
стали огромной частью нашей мобильной культуры. Они обеспечивают питание большей части технологий, которые использует наше общество.
Из каких частей состоит литий-ионный аккумулятор?
Батарея состоит из нескольких отдельных ячеек , которые соединены друг с другом.Каждая ячейка содержит три основные части: положительный электрод (катод ), отрицательный электрод (анод ) и жидкий электролит .
Части литий-ионной батареи (© Let’s Talk Science, 2019 г., на основе изображения ser_igor с iStockphoto).Литий-ионные батареи, подобно сухим щелочным батареям, используемым в часах и пультах дистанционного управления от телевизора, обеспечивают питание за счет движения ионов. Литий в своей элементарной форме чрезвычайно реактивен.Вот почему в литий-ионных батареях не используется элементарный литий. Вместо этого литий-ионные батареи обычно содержат оксид лития-металла, такой как оксид лития-кобальта (LiCoO 2 ). Это поставляет литий-ионы. В катоде используются оксиды лития-металла, а в аноде — литий-углеродные соединения. Эти материалы используются, потому что они допускают интеркаляцию. Интеркаляция означает, что молекулы могут что-то в них вставлять. В этом случае электроды могут легко перемещать ионы лития в свою структуру и выходить из нее.
Каков химический состав литий-ионных аккумуляторов?
Внутри литий-ионной батареи протекают окислительно-восстановительные реакции.
Восстановление происходит на катоде. Там оксид кобальта соединяется с ионами лития с образованием оксида лития-кобальта (LiCoO 2 ). Половина реакции:
CoO 2 + Li + + e — → LiCoO 2
Окисление происходит на аноде.Здесь соединение интеркаляции графита LiC 6 образует графит (C 6 ) и ионы лития. Половина реакции:
LiC 6 → C 6 + Li + + e —
Вот полная реакция (слева направо = разрядка, справа налево = зарядка):
LiC 6 + CoO 2 ⇄ C 6 + LiCoO 2
Как работает подзарядка литий-ионного аккумулятора?
Когда литий-ионный аккумулятор в мобильном телефоне питает его, положительно заряженные ионы лития (Li +) перемещаются от отрицательного анода к положительному катоду.Они делают это, перемещаясь через электролит, пока не достигнут положительного электрода. Там они хранятся. С другой стороны, электроны движутся от анода к катоду.
Что происходит в литий-ионной батарее при разряде (© Let’s Talk Science, 2019 г., на основе изображения ser_igor с iStockphoto). Иллюстрация — текстовая версияКогда батарея используется, ионы лития текут от анода к катоду, а электроны движутся от катода к аноду.
Когда вы заряжаете литий-ионный аккумулятор, происходит прямо противоположный процесс. Ионы лития возвращаются от катода к аноду. Электроны движутся от анода к катоду.
Что происходит с литий-ионным аккумулятором при зарядке (© Let’s Talk Science, 2019 г., на основе изображения ser_igor с iStockphoto). Иллюстрация — текстовая версияКогда батарея заряжается, ионы лития текут от катода к аноду, а электроны движутся от анода к катоду.
Пока ионы лития переходят от одного электрода к другому, существует постоянный поток электронов. Это дает энергию для работы вашего устройства. Поскольку этот цикл может повторяться сотни раз, этот тип аккумулятора перезаряжаемый .
Знаете ли вы?
Иногда литий-ионные батареи называют «батареями для кресел-качалок». Это потому, что ионы лития «качаются» между электродами.
Что делает литий-ионные аккумуляторы подходящими для мобильных технологий?
Все просто. Литий-ионные батареи имеют самую высокую плотность заряда среди всех сопоставимых систем. Это означает, что они могут дать вам массу энергии, не будучи очень тяжелыми.
Это по двум причинам. Во-первых, литий является наиболее электроположительным элементом . Электроположительность — это мера того, насколько легко элемент может отдавать электроны для образования положительных ионов. Другими словами, это показатель того, насколько легко элемент может производить энергию.Литий очень легко теряет электроны. Это означает, что он может легко производить много энергии.
Литий также самый легкий из всех металлов. Как вы узнали, в качестве электродов в литий-ионных батареях используются интеркаляционные материалы, а не настоящий металлический литий. Тем не менее, эти батареи весят намного меньше, чем батареи других типов, в которых используются такие металлы, как свинец или никель.
Есть ли риски при использовании литий-ионных батарей?
Хотя эти батареи впечатляют, у них есть свои недостатки.Самая большая жалоба заключается в том, что они довольно быстро изнашиваются, независимо от того, используете вы их или нет. Обычный литий-ионный аккумулятор прослужит около 2–3 лет, прежде чем его потребуется заменить. Это может обойтись дорого! Производство и утилизация литий-ионных батарей также оказывает большое влияние на окружающую среду, поэтому чем дольше эти батареи могут прослужить, тем лучше.
Как вы узнали, литий чрезвычайно реактивен. Когда производители производят литий-ионные батареи, они должны принимать определенные меры предосторожности, чтобы их можно было безопасно использовать.Однако вы, возможно, слышали о некоторых электронных устройствах, таких как ноутбуки или сотовые телефоны, которые загорелись из-за своих батарей. Хотя это может быть хорошим предлогом для того, чтобы не сдать эссе на английском вовремя, это довольно опасная ситуация. По соображениям безопасности литий-ионные батареи включают сепаратор. Это предотвращает соприкосновение электродов элементов батареи друг с другом. Но если этот разделитель будет порван или поврежден, электроды могут соприкоснуться. Это может вызвать сильное перегревание. Если это нагревание вызывает искру, легко воспламеняющийся электролит может загореться.
Как только в одной камере возникает пламя, оно может быстро распространиться на другие. И прежде чем вы это заметите, ваш ноутбук представляет собой лужу расплавленного пластика. Накопление тепла также может вызвать очень быстрое повышение давления в вашем ноутбуке и БУМ!
Посмотрите, что происходит при коротком замыкании литий-ионного аккумулятора (1:13 мин.).Однако не стоит особо волноваться. Эти события очень редки. На самом деле литий-ионные батареи очень безопасны. Кроме того, прямо сейчас ведется много исследований по улучшению каждой части этих батарей.Например, исследователи создали жидкий электролит, который при ударе превращается в твердое тело. Это поможет предохранить батареи от нагрева или возгорания в случае их повреждения! Вскоре литий-ионные батареи, вероятно, станут еще безопаснее, прослужат дольше и будут стоить еще дешевле.
.Знаете ли вы?
Большинство электромобилей работают на литий-ионных батареях. Мы начинаем видеть все больше и больше автомобилей, которые подключаются к сети вместо того, чтобы заправляться бензином!

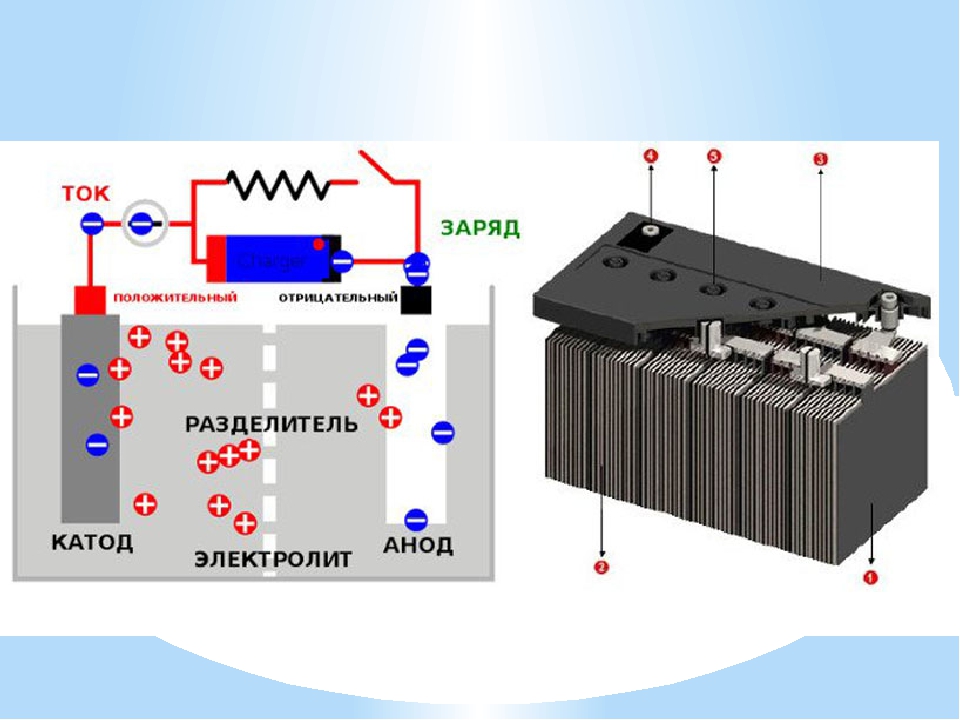 Сурьма увеличивает прочность пластин, однако усиливает процесс электролиза — вода разлагается на кислород и водород. Такие аккумуляторы требуют постоянного контроля уровня содержимого банок и доливки дистиллированной воды.
Сурьма увеличивает прочность пластин, однако усиливает процесс электролиза — вода разлагается на кислород и водород. Такие аккумуляторы требуют постоянного контроля уровня содержимого банок и доливки дистиллированной воды.
