Аккумуляторная кислота – Как заменить электролит в аккумуляторе автомобиля: уровень, плотность, необходимые инструменты
- 25.09.2017
Какая кислота в аккумуляторе
Знать, какая кислота в аккумуляторе автомобиля, обязан каждый водитель, самостоятельно обслуживающий своё транспортное средство. Этот вопрос вызван не праздным любопытством, имеющим цель расширить кругозор. Применяя знания такого рода на практике, можно не только продлить срок службы аккумуляторной батареи, но и избежать возникновения неприятных, а подчас и опасных ситуаций, в которые рискует попасть неподготовленный человек.
Для чего нужна кислота
Прежде чем приступать к описанию процессов, протекающих при разряде/заряде, стоит сразу сказать, какая кислота используется в аккумуляторе любого автомобиля – это серная (h3SO4), а не соляная или, например, фосфорная.
Она необходима для приготовления электролита – жидкости, в которой присутствуют заряженные частицы – ионы. Электролит представляет собой не просто пассивный раствор, в котором частицы воды и кислоты перемешаны друг с другом. Это активная жидкость, отличительная особенность которой – постоянное протекание в ней взаимно исключающих друг друга процессов – диссоциации и ассоциации.
 В аккумуляторе присутствует серная кислота
В аккумуляторе присутствует серная кислотаПри диссоциации, которая протекает лишь в водном растворе h3SO4. Молекулы кислоты образуют ионы с положительными и отрицательными зарядами:
 Диссоциация кислоты
Диссоциация кислотыПараллельно с диссоциацией протекает обратный процесс – превращение ионов в молекулы кислоты. Полной ионизации электролита, а также полной нейтрализации заряженных частиц не происходит. Процессы находятся в динамическом равновесии, которое может измениться лишь под влиянием внешнего воздействия.
Именно наличие ионов и превращает раствор в электролит. Под влиянием электрического поля (во время зарядки) заряженные частицы переносят заряд к пластинам аккумулятора. При реакции между ионами и веществом пластин происходит высвобождение электронов. Они способны двигаться по проводнику при подключении его к электродам (их выводам).
Основные процессы, протекающие при разряде
Отрицательные пластины АКБ и их обмазка изготовлены из свинца (Pb), а у положительных активная масса имеет основой его диоксид (PbO2). Металлический свинец обладает большим количеством свободных электронов, чем его диоксид. Если положительную и отрицательную пластины соединить проводником, то разность потенциалов практически сразу уравновесится и электрический ток не возникнет.
Но если эти пластины погрузить в сернокислотный электролит, то перенос электронов вызовет химические реакции окисления металлического свинца и восстановления его диоксида:
PbO2 + SO42- + 4H++ 2e- = PbSO4 + h3O
Как видите, «конечными продуктами» этих реакций являются:
- Сульфат свинца PbSO4, образующийся на поверхности пластин.
- Вода.
- Свободные электроны (e-), благодаря которым и возникает электрический ток.
При достаточно продолжительном разряде серная кислота может полностью «израсходоваться» на образование сульфата и воды, в результате чего прекратятся химические реакции и свободные электроны не будут образовываться. Поэтому особенно ценным в плане практического использования свинцовых аккумуляторных батарей является возможность протекания обратных реакций при подключении к выводам электрического напряжения.
При зарядке сульфат свинца, прореагировав с водородом, снова становится серной кислотой, в результате чего плотность электролита восстанавливается, а поверхность пластин аккумулятора приобретает первоначальный состав.

Состав электролита
Химический состав раствора прост – 35% серной кислоты + 65% воды. Такое соотношение обусловлено как необходимостью сохранить работоспособность батареи при низких температурах (до -65 С). А также избежать чрезмерной коррозии пластин – серная кислота очень агрессивна.
Разумеется, вода должна быть дистиллированной, а кислота соответствовать по чистоте ГОСТ 667-73, устанавливающему минимальные нормы содержания примесей.
При обслуживании аккумуляторов состав аккумуляторной кислоты оценивается по плотности, измеряемой ареометром. При температуре воздуха +20 С её значение должно быть 1,28 г/см3.
Но для автомобилистов необходимость самостоятельно изготавливать электролит для батареи практически отпадает. В автомагазинах продаётся как готовый раствор (плотностью 1,28 г/см3), так и корректирующий (1,4 г/см3). Также можно купить и дистиллированную воду – при необходимости её доливки.
Контроль за состоянием электролита
В первую очередь, на что должен обращать внимание владелец при уходе за батареей – это уровень электролита. Пластины должны быть полностью погружены в раствор. Расстояние от поверхности жидкости до верхнего края пластин – около 10-15 мм.
Знать, сколько жидкости должно быть в аккумуляторе, нужно лишь в тех случаях, когда вы собираетесь её поменять целиком. Объём электролита зависит от ёмкости АКБ, примерные его значения приведены в таблице:

Но замена электролита потребует слива отработанного раствора. Для чего потребуется сверлить корпус батареи и затем восстанавливать его целостность. Опрокидыванием выливать ни в коем случае нельзя. Шлаком, скопившемся на дне, можно спровоцировать замыкание пластин и окончательный выход АКБ из строя.
Поэтому уход за батареей, который имеет практическую значимость, сводится к возобновлению уровня электролита и контролю его плотности.
Вконтакте
Google+
что залито в аккумулятор, состав кислотного электролита, из чего он состоит
Автомобильные аккумуляторы извлекают электрическую энергию из химической реакции, протекающей внутри него. по сути АКБ конвертируют энергию из электрической в химическую в процессе заряда и наоборот, когда выдают необходимый ток.
Для качественного протекания этих процессов требуются ингредиенты достаточной чистоты. Особенно это касается серной кислоты, вместе с дистиллированной водой являющейся тем, из чего состоит электролит в аккумуляторе.
Серная кислота в аккумуляторе
Собираясь на положительных и отрицательных электродах батареи, ионы создают на клеммах АКБ необходимый заряд. Со временем часть молекул связывается без возможности возобновить свою работу в банках, что снижает плотность электролита. Поэтому так важно следить за концентрацией аккумуляторной кислоты.
Процесс носит название электролитической диссоциации. При нём ионы с положительным зарядом(катионы) — устремляются к плюсовому электроду. К отрицательному электроду направляются анионы — отрицательно заряженные ионы.
Окислителем выступает диоксид свинца, который в результате взаимодействия с молекулами кислоты восстанавливается, отдавая отрицательный заряд на электроды. Растворы серной кислоты слабо проводят электрический ток, однако хорошо справляется с ионным обменом.
При разрядке АКБ положительные ионы свинца устремляются через электролит с губчатого свинца – восстановителя. Здесь происходит превращение в двухвалентный свинец из четырехвалентного, таким образом, оставляя заряд 2 электронов с каждого иона.
На аноде — PbO2 + SO42− + 4H+ + 2e− -> PbSO4 + 2H2O — окисление свинца.
На катоде — Pb + SO42− − 2e− ->PbSO4
Во время зарядки идут обратные реакции — свинец движется в сторону пластин.
Оба электрода покрываются слоем сульфата, который образовывается из отрицательных кислотных остатков и положительных двухвалентных ионов свинца. Это называется сульфатацией, которая для пластин аккумулятора весьма опасна и грозит быстрым износом. Выделяемые газы в процессе восстановительно-окислительных реакций считаются побочным эффектом, однако они могут серьёзно повлиять на работоспособность всей батареи.
В процессе разрядки батареи к отрицательно заряженному электроду устремляются электроны, где они производят нейтрализацию ионов свинца. В зависимости от уровня заряда батареи плотность электролита может иметь разное значение.
Измерения делаются при комнатной температуре + 25 °С. Использование кислоты происходит в 1,6 раз больше положительными электродами. Поэтому рост объема электролита наблюдается при разрядке батареи и уменьшение – при зарядке.
Состав кислотного электролита

Согласно ГОСТ 667 73 аккумуляторная кислота должна обладать следующими физико-химическими показателями.
Для высшего сорта массовые части:
- моногидрата – 92-94 %;
- железа – до 0,005 %;
- после прокаливания остатка – 0,02 %;
- окислов азота – 0,00003 %;
- мышьяка – не более 0,00005 %;
- хлористых соединений – 0,0002 %;
- марганца – до 0,00005 %;
- всех тяжелых металлов, пересчет на Рb – 0,01 %;
- меди – 0,0005 %;
- восстановителей для KМnO – до 4,5 %.
Прозрачность раствора определяется при комнатной температуре жидкости с помощью специального теста. Согласно ГОСТ 667 73 кислота аккумуляторная должна быть определенной прозрачности, что при установке на поле с шахматными клетками и подсвечивании его электрической лампой должно давать четкие очертания ячеек. Представленные данные — это эталонные показатели, и на практике то что заливают в аккумулятор всегда ниже качеством и больше загрязнено.
Поднятие плотности в АКБ
Повышение плотности электролита происходит как следствие повышения температуры и гидролиза в батарее. Для выравнивания этого показателя требуется постоянное добавление определенного количества дистиллята. При меньшей концентрации аккумуляторной кислоты в электролите, следует ее поднимать, если датчик показывает значение ниже 1,275 г на куб. см.
Важно! Кислота является агрессивной средой для тканей человека, одежды. Поэтому при работах с открытой батареей следует позаботиться о мерах защиты: надеть защитные очки и резиновые перчатки. Не помешает прорезиненный фартук или старая одежда.
Кислотность электролита поднимается двумя путями: внесением концентрированной кислоты с помощью постепенного разбавления или полная замена электролита новым.
В первом случае следует провести такие действия для каждой банки:
- Откачать по возможности максимальное количество электролитической жидкости с помощью резиновой груши или колбы;
- Внести в банку половину ее объема электролита с плотностью от 1,275 до 1,29 г на куб. см;
- Для перемешивания электролита на выводы подается нагрузка небольшой мощности, например при подключении обычной лампочки для автомобилей, или выдерживание на протяжении нескольких часов;
- При замере плотности следует определить нужный уровень. Если не было изменений, то в половину оставшегося объема следует внести еще электролит;
- Повторное перемешивание с замером;
С помощью подобных манипуляций следует довести до нужной плотности концентрацию серной кислоты в электролите.
При показателе индикатором значения плотности ниже 1,2 г на куб. см, требуется полная замена электролитической жидкости, поскольку подобным способом поднятие ее невозможно. Такой уровень в заряженном состоянии наводит на мысль о целесообразности операции.
Если батарее менее года, то процедура может увенчаться успехом, более старые элементы питания, скорее всего, реанимацию не переживут.
Полезное видео
Видеоинструкция по обслуживанию аккумулятора
Какой электролит заливать?
Для приготовления нового электролита требуется концентрированная кислота для аккумуляторов, которая продается с плотностью 1,835 – 1,84 г на куб. см. Разбавляется жидкость чистой дистиллированной водой, поскольку содержащиеся соли металлов в обычной проточной воде пагубно влияют на электроды АКБ.
Важно! Внесение дистиллята в кислоту строго запрещено. В результате таких действий возникает сильный нагрев, бурная реакция с разбрызгиванием вещества. Поэтому добавлять следует кислоты в дистиллированную воду тонкой струйкой.
Для того чтобы развести аккумуляторную жидкость, следует проделать такие операции:
- По возможности использовать защитную одежду: защитные очки, химически устойчивую одежду и резиновые перчатки.
- Подготовить все ингредиенты и инструменты: кислоту, дистиллированную воду, ареометр, химически стойкую посуду,
- Рассчитать количество кислоты и дистиллированной воды для необходимого результата. В среднем в АКБ залито 2,6-3,7 литра раствора, но лучше разведение производить с расчетом на объем 4 литра;
- В устойчивую к кислотным воздействиям емкость наливается нужный объем дистиллята;
- Постепенно разбавляется дистиллированная вода кислотой с постоянным перемешиванием, чтобы плотные слои разводились равномерно, а не опускались на дно емкости;
- Ареометром замеряется плотность полученного раствора;
- При наличии показателя, близкого к требуемому значению, раствор должен настояться несколько часов для лучшего перемешивания.
Таблица плотностей электролита и соотношения дистиллята и кислоты
При получении слишком концентрированной жидкости, следует провести разбавление ее дистиллятом. При смешивании дистиллированной воды и аккумуляторной кислоты в процессе реакций выделяется тепло, которое будет опасным для электродов. Поэтому заливать в банки следует только остывший раствор.
Заключение
Срок службы аккумуляторной батареи ограничивается ее техническими характеристиками. Однако неправильное использование и хранение может существенно снизить этот показатель. Чтобы АКБ не изнашивалась стремительно, нужно следить за плотностью электролита и его уровнем.
В результате химических процессов повышение плотности раствора происходит из-за высокой температуры и естественных реакций окисления и восстановления. Поэтому следует доливать дистиллят. Сильное падение плотности требует полноценной замены электролитической жидкости. Важно соблюдать меры предосторожности при работе с емкостью, а также следовать четким инструкциям.
Вконтакте
Google+
Какую кислоту заливают в аккумулятор автомобиля: серную, соляную или другую?
Какую кислоту заливают в аккумулятор
В некоторых видах автомобильных АКБ в качестве электролита может использоваться щелочь. К примеру, никель-кадмиевый тип АКБ. Помимо этого, есть группа гелевых аккумуляторов, где жидкость находится в связанном состоянии. Но, по сути, это раствор серной кислоты, переведенный в гелеобразное состояние или им пропитанное стекловолокно.
Серная кислота широко используется при производстве свинцово-кислотных АКБ для транспортных средств. Ее концентрация в электролите около 30-35%, остальное – дистиллированная вода. Применять обычную водопроводную воду запрещено, поскольку в ее состав входят соли многих металлов и их попадание в АКБ сократит срок его службы.
Как правило, в бытовой сфере серной кислоты с 30%процентов вполне достаточно, однако в сфере производства довольно часто используется кислота с более высокой концентрацией. Получить концентрированную серную кислоту можно в две стадии. Первая – это когда концентрация доводится до 65-70%, вторая – когда ее увеличивают до 98%. Такой состав наиболее пригоден для длительного хранения. Возможно получение высокой концентрации в 99 %, но в дальнейшем из-за значительной потери SO3 она снизится до 98,3%.
Применение серной кислоты и ее сорта

Существует несколько сортов серной кислоты, к ним относятся:
- Нитрозная или башенная. Концентрация составляет 75%, а плотность этого сорта находится в пределах 1,67 г/см3. Такое название он получил благодаря методу производства нитрозным способом в футерованных башнях. Обжиговый газ обрабатывается нитрозой и в процессе реакции получается кислота и оксиды азота.
- Контактная. Концентрация достигает 92,5-98%, плотность – 1,837 г/см3 . Данный сорт также получается из обжигового газа с содержанием двуокиси SO2. В процессе химической реакции происходит ее окисление при контакте с катализатором из ванадия.
- Аккумуляторная. Концентрация 92-94%, плотность – 1,835 г/см3.
- Сорт Олеум. Концентрация довольна высокая –104,5%, плотность – 1,897 г/см 3 , представляет собой концентрированный раствор из кислоты и SO3.
- Высокопроцентный олеум. Концентрация достаточно высокая –114,6%, плотность – 2,002 г/см3.
Процессы, происходящие в АКБ с участием электролита

Функционирование свинцово-кислотного АКБ основывается на химических процессах, протекающих с помощью электролита. АКБ автомобиля из пластин: положительных и отрицательных, погруженных в раствор кислоты. Пластины имеют токоотводящие решетки, выполненные из свинца с добавками (зависит от типа АКБ), а на решетках отрицательных электродов нанесен сероватый порошок свинца, на положительных – красновато-коричневый диоксид свинца.
Показатель плотности электролита на заряженном АКБ находится в диапазоне 1,128─1,300 г/см3. При разрядке АКБ в результате химической реакции из электролита стремительно расходуется кислота и плотность значительно падает.
Полностью заряженный элемент аккумулятора транспортного средства выдает напряжение в пределах 2,5-2,7 В без нагрузки на выводах. В случае нагрузки данное напряжение несколько проседает до 2,1 В буквально за несколько минут. За этот короткий период на поверхности отрицательных электродов успевает сформироваться плотный слой PbSO4. Соответственно, напряжение элемента на подключенной к авто АКБ составляет 2,15 В.
Если разряжать АКБ транспортного средства небольшим током (примерно 10% от номинальной емкости), тогда через 1-2 ч разрядки напряжение элемента снизится до 2 В. Это обусловлено тем, что в этом момент формируется большое количество PbSO4, который, в свою очередь сильно забивает поры активной массы. Помимо этого, проявляется рост внутреннего сопротивления элементов аккумулятора и значительно снижается концентрация жидкости.
Контроль за состоянием электролита
Контроль за электролитом – важная процедура, которая должна проводиться регулярно. От владельца транспортного средства требуется контролировать как уровень электролита в АКБ, так и его плотность. Чтобы проверить уровень электролита рекомендуется использовать стеклянную трубочку, но если ее нет, то можно использовать прозрачный корпус от ручки. Для измерения нужно открыть пробки всех банок и погрузить пластиковую/стеклянную трубочку до пластин. После чего с верхнего конца ее плотно зажать пальцем и поднять.

Оптимальный уровень электролита в трубке должен быть 10-12 мм. В случае нехватки электролита доливается вода до требуемого уровня. Выше необходимого уровня воду заливать не следует.
Срок службы электролита
Стоит знать, что кислотный электролит – это раствор, который не имеет срока годности. Срок службы для такой жидкости определяется исключительно исходя из того, как она способна выполнять свои функции.
К показателям, которые влияют на срок использования АКБ, относятся:
- Плотность электролита.
- Температурный режим функционирования АКБ.
- Степень заряженности аккумулятора.
Если эти показатели соответствуют норме, срок службы электролита довольно продолжительный.
Как поднять плотность электролита
Повышение плотности жидкости происходит вследствие повышения температуры и в результате процесса, который называется гидролиз. Чтобы этот показатель находился на необходимом уровне, требуется регулярное добавление дистиллята. Если датчик концентрации кислоты в электролите показывает значение ниже, чем 1,275 г/см3, следует его поднимать.
Кислотность электролита можно поднять двумя способами: полной заменой старого электролита на новый или внесением разбавленной концентрированной кислоты.
В случае разбавления жидкости следует провести ряд действий для каждой банки:
- Постараться откачать максимальное количество электролита посредством шприца или резиновой груши.
- Внести в банку 0,5 его объема плотностью от 1,26 до 1,28 г/см3.
- Чтобы тщательно перемешать жидкость, необходимо на выводы подать нагрузку с минимальной мощностью.
При замере плотности стоит определить необходимый уровень. Если не произошло изменений, тогда в половину оставшегося объема требуется внести еще электролит.
С помощью подобных манипуляций можно довести до оптимальной плотности концентрацию кислоты в электролите.
В случае, если показатель индикатора показывает значения плотности ниже, чем 1,2 г/см3, требуется полная замена электролита, так как способом доливки поднять ее не получится. Однако если батарее менее года, то стоит попробовать.
Важно! Серная кислота – агрессивная средой для кожных покровов человека и его одежды. Поэтому во время работ с открытой батареей рекомендуется позаботиться о мерах защиты: обязательно надеть резиновые перчатки, защитные очки. Так же пригодится прорезиненный фартук.
Порядок заливки и доливки кислотного электролита в АКБ
Составляющие компоненты электролита – кислоту и дистиллированную воду, нужно смешать в разных пропорциях. Так, если необходимо получить электролит с уровнем плотности 1,29 г/см³, то к 1 литру необходимо добавить 0,36 л кислоты, то есть в соотношении 1:3.
Заливку электролита производят стеклянной или полиэтиленовой трубочкой до уровня 10-15 мм над свинцовыми пластинами. После этого аккумулятор оставляют на два часа, однако в некоторых случаях плотность при этом падает. Далее АКБ заряжают током в десять раз меньшим его емкости в течение 4 часов.
Проверять плотность АКБ необходимо раз в 2-3 месяца. Для этого используется специальный прибор – ареометр.
Важно! В целях техники безопасности необходимо знать, что заливать нужно именно серную кислоту в дистилированную воду, но не наоборот, поскольку высока вероятность возникновения химической реакции данной смеси с выделением брызг и тепла.
Процесс приготовления электролита

Электролит для АКБ можно, конечно, приобрести в специализированных магазинах, но можно сделать его самостоятельно и при этом научиться регулировать плотность.
Для приготовления электролита потребуются следующие компоненты:
- Вода дистиллированная.
- Серная кислота.
- Емкость из материала, устойчивого к воздействию концентрированного химического вещества: стекла, керамики, свинца.
- Эбонитовая палочка (для размешивания жидкости).
Для приготовления в специальную емкость заливается вода, после – серная кислота. Компоненты тщательно палочкой смешиваются. Процедуру проводят последовательно, поскольку при обратном варианте есть вероятность получить ожоги.
Полученное вещество плотно накрывается и оставляется минимум на сутки до выпадения осадка и остывания. Стоит знать, что при обратном проведении заливки (сначала серная кислота, потом – вода), возможна гидратации и образование в кислоте тепла. Соответственно, вода может закипеть и спровоцировать разбрызгивание.
Срок службы АКБ ограничен ее техническими характеристиками. Однако при неправильном его использовании и хранении этот показатель может существенно снизиться. Чтобы АКБ не изнашивалась слишком стремительно, специалисты рекомендуют следить за плотностью электролита и его уровнем.
Какая кислота в аккумуляторе автомобиля и какова ее плотность
Владельцы автомобилей часто задаются вопросом о том, какая кислота в аккумуляторе автомобиля, от которой зависит срок его службы. Производители этой продукции в основном заливают серную кислоту, представляющую кислотно-водный раствор определенной плотности и концентрации. Она называется электролитом, и для контроля его качества следует знать определенные особенности обращения, проверки и технические характеристики. В некоторых АКБ используется щелочной электролит, состоящий из элементов лития, натрия, калия и их комбинаций. В основном это сухозаряженные источники питания, которые применяются в суровых климатических условиях.
Состав электролита
Электролит, или серная кислота используется современной промышленностью для производства источников тока:
- в батареях;
- аккумуляторах;
- электрических конденсаторах.
В аккумуляторы заливается серная кислота разбавленного соотношения с водой — примерно 70% воды, 30% H2SO4. При ее отсутствии устройство не пригодно к работе. Особого внимания также заслуживает плотность жидкости, которую следует проверять и при необходимости увеличивать.
Контроль плотности
Плотность в автомобильном свинцово-кислотном аккумуляторе измеряют в гр/см³, и она должна быть пропорциональна концентрации раствора с обратной зависимостью температур жидкости. Нормальный показатель — 1,27-1,29 гр/см³. Этот показатель позволяет определить состояние батареи, и если она не держит заряда, то необходимо проверить количество вещества. Со временем уровень электролита аккумулятора автомобиля сокращается, и соответственно, увеличивается плотность при гидролизе воды и нагрева. Для этого требуется периодически доливать дистиллированную воду, снижая концентрацию серной кислоты. Процедуру можно выполнить самостоятельно, если знать, сколько требуется для определенной модели вещества.

Электролит для аккумуляторов можно приобрести в магазинах, либо сделать своими руками и научиться регулировать плотность, своевременно измерять и ухаживать за устройством для продления срока службы.
Для приготовления потребуются следующие компоненты:
- Серная кислота.
- Вода дистиллированная.
- Емкость из стекла, свинца, керамики, устойчивая к воздействию химического вещества.
- Эбонитовая баночка для размешивания.
Для приготовления в емкость заливается дистиллированная вода, затем серная кислота, и палочкой параллельно помешивается получаемая смесь. Процедуру проводят последовательно, так как при обратном варианте можно получить ожоги. Если места эксплуатации автотранспорта климат умеренный, то следует придерживаться такой пропорции веществ: на 1 л воды — 0,36 л кислоты. Для теплого климата на 1 л воды следует заливать кислоту в объеме 0,33 л. Полученное вещество накрывается и оставляется на сутки до образования осадков и остывания. При замене электролита в аккумуляторе надевают резиновые перчатки и очки для защиты глаз.
Напомним, что при обратном проведении заливки, в частности, первой воды, возможна реакция гидратации и образования тепла в кислоте. Вероятно, что вода закипит и спровоцирует разбрызгивание.
Проверять плотность аккумулятора необходимо раз в три месяца. Для этого пользуются ареометром.
Составляющий компонент строения АКБ
Без наличия в аккумуляторе электролита не будет выполняться его основная функция, так как вещество является активатором заряда и разряда. В емкости устройства жидкости должно быть много, и, соответственно, вес аккумулятора не маленький. Примерное соотношение конструкции представляет до 20 % веса жидкости, до 25 % пластика и свинцовая составляющая достигает до 80 % веса. Плюсовые пластины состоят из диоксида свинца, минусовые монолитные пластины — чистый свинец. Пластины служат для сборки пакетов, способствующих накоплению заряда.

Следует отметить, что АКБ различается по моделям, и, в частности, модель 55 А/ч относится к одной из самых легких, какую можно встретить в легковых автомобилях достаточно часто. Ее вес не превышает 16 кг. Есть более компактные модели с незначительным весом, как, например, 40 А/ч и другие варианты.
Нейтрализация электролита
Если аккумулятор вышел полностью из строя, его требуется утилизировать грамотно. Но также в случае течи электролита из батареи необходимо узнать, чем нейтрализовать ее.
Бывают ситуации, когда при поломке аккумулятора может быть залита отдельная часть в месте его нахождения. Для этого необходимо вытащить батарею и провести очистку. Нейтрализация этого вещества из аккумулятора, как правило, проводится при помощи специального оборудования и применения технологий. Это важно с экономической и экологической точек зрения. Если проводить неорганизованную нейтрализацию, можно нанести значительный вред окружающей среде.
В настоящее время имеются два варианта нейтрализующего вещества с кислотами промышленным способом. Первый предусматривает устранение фильтрующим методом сброса кислоты в стоки, с пропусканием через магнезит, известняк и другие материалы, а второй способ – регенерация кислоты специальной обработкой с последующим получением товарного продукта. Но на практике многие водители рекомендуют в случае пролива опасного вещества использовать щелочный раствор, который делается из пищевой соды и воды.
При регулярной проверке аккумулятора, в том числе контроле за плотностью и уровнем электролита, можно избежать многих проблем и продлить срок эксплуатации батареи, не допустить механических разрушений. Всегда требуется внимательно относиться к устройствам при эксплуатации, особенно в зимнее время, когда при низких температурах и сниженной плотности электролита может произойти его замерзание или разрушение пластин.
Какая кислота в аккумуляторе автомобиля и для чего нужен электролит


Многие автолюбители задают себе вопрос о том, какая кислота залита в аккумуляторе автомобиля. По незнанию высказываются различные неверные предположения. Кто-то говорит, что там соляная кислота. Некоторые считают, что там вода. Пора внести ясность в этот вопрос. В свинцово-кислотном аккумуляторе автомобиля залита серная кислота. Если выражаться совсем точно, то залит раствор серной кислоты в дистиллированной воде. Этот раствор получил название электролит.
Содержание статьи
Применение серной кислоты и её сорта
Вообще, в качестве электролита в некоторых видах автомобильных аккумуляторов может использоваться щёлочь. Например, никель-кадмиевый или никель-железный тип АКБ. Есть ещё группа гелевых аккумуляторов AGM и GEL, где электролит находится в связанном состоянии. Но это тот же раствор серной кислоты. Просто он либо переведён в гелеобразное состояние с помощью добавок (GEL), либо им пропитано стекловолокно (AGM). Наиболее распространёнными на сегодняшний день остаются свинцово-кислотные автомобильные аккумуляторы с жидким электролитом. Поэтому речь пойдёт именно о водном растворе серной кислоты, предназначенном для заливки в АКБ.

Электролит

Дистиллированная вода
Серная кислота используется в самых разных отраслях народного хозяйства. К примеру, с её помощью очищается поверхность металла перед нанесением покрытия, она используется при приготовлении различных синтетических красителей. Кроме того, серная кислота востребована в сфере производства удобрений, взрывчатки, фармакологической промышленности, переработке нефти.
Серная кислота нашла широкое применение при производстве свинцово-кислотных аккумуляторов для автомобилей. Концентрация кислоты в электролите составляет 30-35 процентов (вес.). Остальное дистиллированная вода. Использовать обычную водопроводную воду нельзя, поскольку в ней содержатся соли различных металлов. Их попадание в аккумулятор автомобиля значительно сократит срок его службы.
В бытовой сфере концентрации Н2SO4 в 30 процентов достаточно, но в сфере производства часто используется серная кислота более высокой концентрации. Концентрированную серную кислоту получают в две стадии. На первой стадии концентрация доводится до 70 процентов, а затем увеличивают до 98 процентов. Серная кислота такой концентрации наиболее пригодна для последующего хранения. Возможно, получение концентрации 99 процентов, но в дальнейшем из-за потери SO3 она снижается до 98,3 процента.
Существуют основные сорта серной кислоты, которые перечислены ниже:
- Башенная или нитрозная. Концентрация 75 процентов. Плотность этого сорта составляет 1,67 гр/см3. Название этот сорт получил из-за метода производства в футерованных башнях нитрозным способом. Обжиговый газ с двуокисью серы (SO2) обрабатывается нитрозой (H2SO4 с добавками оксидов азота). В ходе химической реакции получается оксиды азота и кислота. При этом оксиды постоянно циркулируют в производственном цикле;
- Контактная. Концентрация от 92,5 до 98 процентов. Плотность сорта составляет 1,837 гр/см3. Этот сорт также производится из обжигового газа, в котором содержится двуокись SO2. В ходе реакции происходит ее окисление до SO3 при контакте с твёрдым катализатором из ванадия;
- Сорт Олеум. Концентрация 104,5 процента. Плотность составляет 1,897 гр/см3. Сорт представляет собой раствор SO3 в серной кислоте (H2SO4). Соотношение SO3 — 20 процентов, H2SO4 — 104,5 процента;
- Высокопроцентный олеум. Концентрация 114,6 процента, а плотность 2,002 гр/см3;
- Аккумуляторная. Концентрация от 92 до 94 процента, а плотность 1,835 гр/см3.
Вернуться к содержанию
Процессы, происходящие в АКБ с участием электролита
Работа свинцово-кислотного автомобильного аккумулятора основывается на электрохимических процессах, которые протекают с участие электролита. Аккумулятор автомобиля состоит из положительных и отрицательных пластин, погруженных в водный раствор серной кислоты. Положительные и отрицательные пластины имеют токоотводящие решётки из свинца с различными добавками в зависимости от типа аккумулятора.
На решётках положительных электродов нанесён красновато-коричневый диоксид свинца (PbO2). На отрицательных электродах — сероватый порошок свинца (Pb). Электрические характеристики аккумулятора напрямую зависят от плотности электролита. Для понимания назначения электролита нужно рассмотреть основные процессы, происходящие в аккумуляторе автомобиля.
При разряде аккумулятор на положительном электроде (аноде) идёт следующая реакция:
PbO2 + SO42− + 4H+ + 2e− -> PbSO4 + 2H2O
На отрицательном электроде (катоде) протекает такой процесс:
Pb + SO42− − 2e− ->PbSO4
При заряде АКБ эти реакции протекают в обратном направлении.
Электролит в свинцово-кислотном автомобильном аккумуляторе имеет разную плотность в зависимости от степени заряженности АКБ. Как уже говорилось выше, концентрированная кислота аккумуляторного сорта имеет плотность 1,835 гр/см3. Плотность электролита на заряженном аккумуляторе лежит в диапазоне 1,127─1,300 гр/см3. При разрядке аккумулятора автомобиля в результате электрохимической реакции из электролита расходуется серная кислота и его плотность падает. Пока через батарею проходит ток разряда кислота рядом с электродами расходуется в результате вышеописанной реакции. Идёт диффузия H2SO4 из объёма к электродам. Таким образом, поддерживается напряжение на выводах аккумулятора.
В начале разрядки процесс диффузии кислоты в электроды. Это объясняется тем, что в активной массе электродов поры ещё не забиты сульфатом. По мере того, как на них образуется слой сульфата и забивает поры, процесс диффузии притормаживается. В теории процесс разряда может идти до того момента, пока электролит не превратится в воду. Но на практике разряд идёт до тех пор, пока плотность не опуститься до значения 1,15 гр/см3. К моменту падения плотности до 1,15 гр/см3 выделяется столько сульфата свинца, что его хватило для закупоривания активной массы пластин. По плотности электролита можно судить о степени заряженности АКБ. Для этого можно использовать таблицу, представленную ниже.
| Плотность электролита, г/см. куб. (+15 гр. Цельсия) | Напряжение, В (в отсутствии нагрузки) | Напряжение, В (с нагрузкой 100 А) | Степень заряда АКБ, % | Температура замерзания электролита, гр. Цельсия |
|---|---|---|---|---|
| Плотность электролита, г/см. куб. (+15 гр. Цельсия) | Напряжение, В (в отсутствии нагрузки) | Напряжение, В (с нагрузкой 100 А) | Степень заряда АКБ, % | Температура замерзания электролита, гр. Цельсия |
| 1,11 | 11,7 | 8,4 | 0 | -7 |
| 1,12 | 11,76 | 8,54 | 6 | -8 |
| 1,13 | 11,82 | 8,68 | 12,56 | -9 |
| 1,14 | 11,88 | 8,84 | 19 | -11 |
| 1,15 | 11,94 | 9 | 25 | -13 |
| 1,16 | 12 | 9,14 | 31 | -14 |
| 1,17 | 12,06 | 9,3 | 37,5 | -16 |
| 1,18 | 12,12 | 9,46 | 44 | -18 |
| 1,19 | 12,18 | 9,6 | 50 | -24 |
| 1,2 | 12,24 | 9,74 | 56 | -27 |
| 1,21 | 12,3 | 9,9 | 62,5 | -32 |
| 1,22 | 12,36 | 10,06 | 69 | -37 |
| 1,23 | 12,42 | 10,2 | 75 | -42 |
| 1,24 | 12,48 | 10,34 | 81 | -46 |
| 1,25 | 12,54 | 10,5 | 87,5 | -50 |
| 1,26 | 12,6 | 10,66 | 94 | -55 |
| 1,27 | 12,66 | 10,8 | 100 | -60 |
Полностью заряженный элемент АКБ автомобиля выдаёт напряжение 2,5─2,7 вольт без нагрузки на выводах. При подключении нагрузки напряжение проседает до 2,1 вольта за несколько минут. За это время успевает сформироваться слой PbSO4 на поверхности отрицательных электродов. То есть, напряжение одного элемента на подключённой к автомобилю АКБ составляет примерно 2,15 вольта.
Если разряжать аккумулятор автомобиля небольшим током (10 процентов от номинальной ёмкости), то через час разрядки напряжение элемента снижается до 2 вольт. Это происходит из-за того, что в этом момент быстро формируется большое количество PbSO4, который забивает поры активной массы. В результате растёт внутреннее сопротивление элементов АКБ и падает концентрация электролита. Через некоторое время процесс разрядки выходит на прямую (см. график).
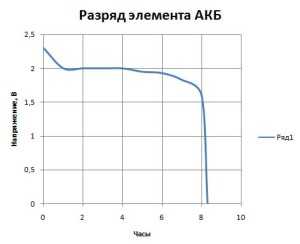
График разрядки аккумулятора
Эта прямая соответствует балансу плотностью электролита около электродов и в остальном объёме. Постепенно кислота поступает из объёма к электродам и вступает в реакцию с выделением сульфата свинца. Плотность электролита постепенно снижается, а напряжение падает медленнее, чем на начальной стадии. И на конечной стадии, когда активная масса блокируется образовавшимся сульфатом свинца, реакция замедляется и напряжение быстро падает.
Вернуться к содержанию
Контроль за состоянием электролита в АКБ?
От владельца автомобиля требуется периодически контролировать уровень электролита в аккумуляторе и его плотность. Для контроля уровня электролита можно использовать стеклянную трубочку. Если её под рукой нет, то можно использовать прозрачный пластиковый корпус от старой шариковой ручки. Для измерения уровня электролита отворачиваете пробки банок батареи и погружаете трубочку до пластин. Затем с верхнего конца плотно зажимаете пальцем и поднимаете. Уровень электролита в трубочке должен составлять 10─12 миллиметров.
В случае нехватки электролита долейте дистиллированной воды до необходимого уровня. Лучше покупайте дистиллированную воду в аптеке. В автомобильных магазинах под видом дистиллированной воды часто продают обычную водопроводную. Выше требуемого уровня воды также заливать не следует. В необслуживаемых автомобильных аккумуляторах (ссылка на материал) доливка дистиллированной воды не требуется. У них сниженный расход воды и они, как правило, имеют крышку с системой рециркуляции электролита.
Внимание! Не допускайте эксплуатации аккумуляторной батареи с уровнем электролита ниже верхней части пластин. Это значительно сокращает срок его службы.
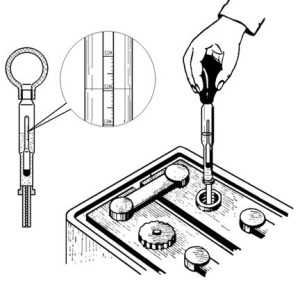
Для того, чтобы измерить плотность Вам потребуется ареометр. Это приспособление представляет собой запаянную стеклянную трубку, в которой находиться ртуть или дробь. На верхнем конце ареометра имеется градуированная шкала. Диапазон измерений плотности 1,100─1,300 гр/см3. Ареометр помещён в разборную колбу с грушей.

Ареометр
Вам нужно опустить нижнюю часть в банку и набрать электролита. После этого вынимаете и смотрите, на каком значении находится уровень электролита. Сам ареометр будет плавать в электролите наподобие поплавка. На некоторых моделях ареометров шкала со значениями может быть заменена надписями «Полный заряд», «Половина», «Разряжен».
Вернуться к содержанию
Как поднять плотность электролита?
Выше уже говорилось о том, что в результате гидролиза воды и нагрева АКБ под капотом уровень электролита постепенно уменьшается и растёт его плотность. Поэтому периодически нужно доливать дистиллированной воды. А что, если плотность электролита на заряженном аккумуляторе автомобиля, наоборот, меньше нормы (1,275 гр/см3)? Тогда нужно поднять концентрацию кислоты.
Внимание! Во время работ с кислотой одевайте резиновые перчатки и защитные очки. Если вы будете самостоятельно разводить электролит из концентрированной кислоты и дистиллированной воды, помните, что нельзя наливать воду в кислоту. В этом случае начинается реакция гидратации с выделением большого количества тепла. В результате вода закипает и провоцирует брызги кислоты, что очень опасно. Поэтому при разбавлении нужно лить кислоту в воду.
При поднятии плотности электролита может быть два варианта. Если средняя плотность по всем банкам не ниже 1,2 гр/см3, то нужно поднять плотность постепенным разбавлением.
Для каждой из банок нужно проделать следующие действия:
- Откачиваете как можно больше электролита из банки. Для этого можно использовать резиновую грушу или ту же колбу. После этого в банку заливаете электролит (плотность 1,275─1,29 гр/см3) половину откачанного объёма;
- Для того чтобы электролит перемешался, можно дать на выводы нагрузку (например, подключить автомобильную лампочку) или просто подождать некоторое время;
- Затем делаете замер плотности. Если она не поднялась до нужного уровня, то заливаете электролит в половину от оставшегося объема;
- Перемешивание и снова замер;
- Доводите плотность кислоты до требуемого уровня.
Если плотность электролита ниже 1,2 гр/см3, то здесь уже нужно его менять полностью. То есть, сливать старый и заливать новый, требуемой плотности. Но, если электролит имеет такую низкую плотность в заряженном состоянии, то возникают сомнения в целесообразности его дальнейшего использования. В этом случае электролит имеет смысл менять только если АКБ относительно новая (до года). Иногда встречаются аккумуляторы автомобиля с такой плотностью электролита прямо из магазина. Если это уже отработавшая несколько лет батарея, то лучше купить новую. При утилизации аккумуляторов отработавший электролит также идет на переработку.
Вернуться к содержанию
Что мы узнали?
Из этой статьи читатели должны были узнать о том, какая кислота залита в аккумулятор автомобиля, какую плотность она должна иметь. Отдельно были рассмотрены химические реакции, проходящие в автомобильном аккумуляторе с участием электролита. Также были даны рекомендации по поддержанию уровня и плотности электролита и приспособлениях, которые для этого требуются. Если у вас остались вопросы или есть пожелания, пишите их в комментариях.
Вернуться к содержанию
Кислотные аккумуляторы; чтобы больше не было отвратительно читать то что люди о них пишут
Случайно узрел статью с комментариями к ней, и так злость во мне закипела по поводу безграмотности людей в области кислотных (свинцовых в простонародье) аккумуляторов, что не выдержал и решил написать «гикам» (чтобы быть гиком, как оказывается, мало купить дорогой телефон) краткую статью об аккумуляторах. С рассмотрением тех ошибок, которые мне постоянно мусолят глаза и вызывают праведное желание их исправить.Начнем с названия. Я очень часто вижу что тремя буквами А-К-Б называют все что можно зарядить, абсолютно любой аккумулятор. Особенно тремя буквами люди любят называть аккумуляторы типа Li-ion. На самом-же деле АКБ аббревиатура от Аккумуляторная Кислотная Батарея. Под ними подразумевается лишь один тип аккумулятора — свинцовый кислотный. С современной точки зрения это название вызывает некоторый когнитивный диссонанс т.к. на данный момент значение слова «батарейка» т.е. гальванического элемента который зарядить нельзя перешло на слово «батарея». И получается как будто бы из-за слова «аккумуляторная» это аккумулятор который зарядить можно, а из-за слова «батарея» это как будто батарейка которую зарядить нельзя. В реальности-же батарея — просто цепь гальванических элементов и со словом «батарейка» имеет общий лишь корень.
Далее перейдем к некоторым мифам, а именно главный миф — АКБ для автомобиля имеет некие существенные отличия от АКБ для ИБП. И вот нельзя их применять и там и там.
С химической точки зрения любые АКБ абсолютно одинаковы. Как-же они устроены? Очень кратко — если аккумулятор заряжен, то один электрод представляет собой свинцовую решетку с нанесенной на нее пастой из PbO2, второй -такую-же решетку с пастой губчатого свинца. Электролитом служит раствор серной кислоты. В процессе разряда PbO2 восстанавливается и взаимодействуя с серной кислотой образует PbSO4. Свинец на другом электроде окисляется и опять-же образует PbSO4. В конце разрядки мы имеем обе решетчатые пластины заполненные (более или менее) сульфатом свинца. При зарядке аккумулятора происходит электролиз и из сульфата свинца вновь образуется диоксид и металлический свинец. Конечно-же, тут нужно подчеркнуть, что электроды при этом не равны и путать их полярность не стоит т.к. еще на стадии производства в намазку электродов вводятся соответствующие добавки, улучшающие их эксплуатационные свойства. При этом добавки полезные для одного электрода вредны для другого. В очень старые времена, где-то в начале прошлого века, в условиях простых аккумуляторов, вероятно, была допустима переполюсовка аккумулятора по ошибке или с какими-то целями и он какое-то время после этого работал. В том что она допустима сейчас я сомневаюсь.
Таких ячеек в 12В аккумуляторе 6 шт, в 6В — 3 шт. и т.д. Многих вводит в заблуждение значение напряжения на аккумуляторах. Причем значений напряжения номинального, заряда, разряда. С одной стороны, аккумуляторы называются 12В (и 6В, 24В тоже есть, по-моему, даже 4В изредка встречаются) но на корпусе тех-же аккумуляторов для ИБП производитель указывает напряжение выше 13.5В.
Например:
Тут мы видим, что в форсированном режиме напряжение заряда может быть аж 15В.
Все разъяснит кривая напряжения на АКБ:

Слева мы видим напряжение для аккумулятора из 12 ячеек (24В номинальных), 6 (12В номинальных) и, самое полезное, для одной ячейки. Там-же отмечены области нежелательных напряжений при разряде/ заряде. Из кривой можно сделать выводы:
1 Напряжение 12В, 24В и т.д. являются номинальными и показывают лишь число гальванических ячеек (путем деления на два) в батарее. Это просто название для удобства.
2 Напряжение при заряде могут достигать 2.5 В/ ячейку что для 12В аккумулятора соответствует 15В.
3 Напряжение заряженной батареи считается допустимым при значении 2.1-2.2 В/ячейку, что для 12В аккумулятора соответствует 12.6-13.2В.
Теоретически, батарею можно зарядить и до значений 2.4 В/ячейку или даже немного выше, однако, такая зарядка будет негативно сказываться как на состоянии электродов, так и на концентрации электролита. Однажды, перед сдачей в утиль, я легко зарядил 12В батарею до напряжения ок. 14.5В (уже не помню точное значение).
Итак, автор статьи с которой я начал, решил, что напряжение заряда автомобильной АКБ и АКБ от ИБП отличаются. Это неверно, у них одинаковый тип электродов и одинаковая концентрация серной кислоты в электролите (подобранная давным-давно экспериментальным путем, чтобы предоставлять максимальное напряжение и минимальном саморазряде). Однако, что-же происходит в батарее, почему ее нельзя заряжать при слишком высоком значении напряжения?
Почему в автомобильную АКБ нужно подливать воду, а в АКБ от ИБП не нужно? Эти вопросы позволяют нам плавно перейти в область напряжения разложения воды. Как я написал выше, при зарядке аккумулятора происходит электролиз. Однако, не весь ток расходуется на превращение PbSO4 в PbO2 и Pb. Часть тока будет неизбежно расходоваться и на разложение воды, составляющей значительную часть электролита:
2H2O = 2H2 + O2
Теоретический расчет дает значение напряжения для этой реакции ок. 1.2В. Напоминаю, что напряжение на ячейке при заряде заведомо более 2В. К счастью, активно вода начинает разлагаться только выше 2В, а в промышленности для получения водорода и кислорода из нее процесс ведут и вовсе при 2.1-2.6В (при повышенной температуре). Как бы то ни было, тут мы приходим к выводу, что в конце процесса заряда АКБ будет неизбежно происходить процесс разложения воды в электролите на элементы. Образующиеся кислород и водород попросту улетучиваются из сферы реакции. Про них бытуют следующие мифы:
1. Водород крайне взрывоопасен! Перезарядишь аккумулятор и как минимум лишишься комнаты где тот был!
На самом деле, водорода в процессе электролиза выделяется ничтожно мало по сравнению с объемом комнаты. Водород взрывается при концентрации от 4% в воздухе. Если мы допустим, что электролиз ведется в комнате размером 3*3*3 метра или 27 метров куб., то нам понадобится наполнить помещение 27*0.04=1.1 метров куб. водорода. Для получения такого количества h3 нужно было бы полностью разложить ок. 49 моль воды или 884 грамма ее. Если кто-то наблюдал электролиз, то поймет насколько это много. Или попробуем перейти ко времени. При силе тока в стандартной зарядке для крупногабаритных АКБ в 6А, уравнение Фарадея дает время, необходимое для получения этого количества водорода, аж 437 часов или 18.2 дня. Чтобы наполнить комнату водородом до взрывоопасной концентрации нужно забыть про зарядку на 2 с половиной недели! Но даже если это случится, концентрация серной кислоты просто будет расти пока ее раствор не приобретет слишком высокое сопротивление для жалких 12В зарядки и сила тока не станет ничтожной. Да и водород попросту улетучится.
Очень редко случаются взрывы непосредственно в корпусах крупногабаритных АКБ из-за того, что выделяющийся водород по какой-то причине не может покинуть замкнутого пространства. Но и в этом случае нечего страшного не бывает — чаще всего взрыва хватает только на небольшую деформацию верхней части корпуса, но не на разрыв свинцовых соединений. И АКБ еще может работать дальше даже после таких повреждений.
2. При электролизе может образоваться смертельно ядовитый и, не менее взрывоопасный чем водород, сероводород!
Не наш, периодически попадался миф в англоязычных постах. Теоретически конечно возможно подать такое большое напряжение и создать т.о. такую большую силу тока, что на катоде начнется процесс восстановления сульфат-иона. Напряжение для этого будет достаточным, а продукты восстановления не будут успевать диффундировать подальше от электрода и восстановление будет идти дальше. Но зарядка в пределах десятка-трех вольт и с ограничением силы тока в 6А на такое едва ли способна. Однажды, я наблюдал процесс восстановления сульфата до SO2, да, это возможно; однокурсницы по ошибке что-то сделали не то во время опыта. Но это большая редкость т.к. там концентрация серной кислоты была заметно выше той, что используется в АКБ, была иная конструкция электрода и иной его материал и, естественно, напряжения и сила тока были были непомерными. И SO2 не H2S.
3. При электролизе мышьяк и сурьма из материала решеток будут восстанавливаться до ядовитых арсина и стибина!
Действительно, решетки содержат относительно много сурьмы, мышьяка в современных решетках, вероятно, нет вообще. При работе АКБ та решетка на которой происходит восстановление, т.е. катод, разрушению не может подвергаться. Выделяйся даже каким-то образом стибин, он бы тут-же взаимодействовал с PbSO4, восстанавливая его до металла.
Однако, некоторая практическая неприятность тут есть. Газообразные водород и кислород могут увлекать за собой капельки электролита, создавая аэрозоль серной кислоты. Аэрозоль серной кислоты, даже концентрированной, для человека не опасен и просто вызывает кашель. Однако, серная кислота — кошмар для тканей и бумаги. Стоит даже небольшому количеству серной кислоты попасть на одежду и там обязательно появятся дырки или ткань разорвется по этому месту. Через недели, если кислоты много, через месяц, но одежда истлеет.
Так что газовыделения опасаться не стоит с бытовой точки зрения или стоит, но нужно ориентироваться именно на аэрозоль серной кислоты.
Итак, вода начала разлагаться на водород кислород, ее в электролите становится все меньше, что-же дальше? Если это АКБ в котором электролит просто налит в виде слоя жидкости, то начнется повышение саморазряда из-за повышения концентрации серной кислоты. Занятно, что это будет сопровождаться небольшим повышением напряжения (концентрация кислоты растет) на ячейке. Именно поэтому автовладельцы должны постоянно контролировать концентрацию серной кислоты в своих АКБ (при помощи ареометра) и доливать туда воду. Процедура доливания воды — необходимая часть процесса обслуживания любой АКБ. Кроме одного их типа, и мы сейчас об этом поговорим.
Иметь аккумулятор в котором болтается слой едкой, по отношению к металлам, жидкости конечно-же неудобно, а потому попытки избавиться непосредственно от жидкости предпринимались давно, начались чуть ли не в первой половине 20-го века. К слову сказать, не то чтобы слой серной кислоты прямо плескался вокруг электродов. В реальности она неплохо распределена между электродами и окружающими их сепараторами даже в дешевых моделях. Итак, первым вариантом было использование стекловолокна. Достаточно просто окружить электроды стекловолокном которое пропитано серной кислотой и большинство проблем решится. Этот тип АКБ носит название AGM (absorbent glass mat) и таких АКБ для ИБП подавляющее большинство. Хотя такие АКБ малого форм-фактора и зачастую позиционируются как те, которые можно эксплуатировать в любом положении, с этим нельзя вполне согласиться. Вскрытие крышки стандартного дешевого AGM аккумулятора показывает, что никаких особых крышек там нет, а следовательно, электролит от вытекания удерживают лишь капиллярные силы. Я почти уверен, что если погонять AGM аккумулятор перевернутым вверх дном, то уже после одной зарядки из него польется серная кислота под давление газов.
Второй распространенный тип интереснее, это т.н. гелевые АКБ. А получаются они благодаря следующему. Если подкислять растворимые силикаты, то будет происходить выделение кремневой кислоты:
Na2SiO3 + H2SO4 = Na2SO4 + SiO2 + H2O
Если исходный раствор силиката не отличается качеством, то кремневая кислота будет выделяться в виде стекловидной массы, но если он достаточно чист, то кремневая кислота осадится в виде красивого куска однородного полупрозрачного геля. На этом и основан способ получения гелевых АКБ — простое добавление силикатов к электролиту вызывает его затвердение в гелеобразную массу. Соответственно, вытекать оттуда уже нечему и АКБ действительно можно эксплуатировать в любом положении. Сам по себе процесс образования геля не повышает емкости АКБ и не улучшает его качеств, однако, производители его используют при производстве наиболее качественных моделей, а потому эти АКБ отличаются высоким качеством и большей емкостью. Занятно, что в обоих случаях носителем электролита является SiO2 в той или иной форме.
Оба типа АКБ объединяются в славный тип VRLA — valve-regulated lead-acid battery который и применяется в ИБП. Формально они считаются необслуживаемыми и терпящими эксплуатацию в любом положении, но это не совсем так. Более того, многие уже встречались с эффектом, когда буквально несколько мл воды возвращают к жизни, казалось бы, дохлую АКБ от ИБП. Так получается, потому что и эти аккумуляторы не капли не застрахованы от электролиза воды в электролите, а следовательно, и пересыхания. Все происходит точно так-же, как в крупногабаритных АКБ. А вот самые дорогие и крутые необслуживаемые АКБ содержат катализатор для рекомбинации выделяющихся газов обратно в воду и вот уже у них корпус действительно выполнен абсолютно герметичным. Обращаю внимание, что по-настоящему герметичным и необслуживаемым может быть и аккумулятор типа AGM и GEL, но они-же могут ими и не быть и не содержать катализатора рекомбинации кислорода и водорода. Тогда, несмотря на казалось бы продвинутую конструкцию, пользователю придется либо чаще покупать новые аккумуляторы, либо доливать воду при помощи шприца.
Хотелось бы добавить несколько слов о режимах разряда. Производители АКБ указывают какой ток максимально допустим для той или иной модели, но нужно понимать, что аккумулятор — просто смесь химических веществ и ЭДС генерируется исключительно химическим путем. Это не конденсатор который, по электрогидравлической аналогии, можно сравнить с неким механическим сосудом (с гибкой мембраной). Хотя АКБ могут выдавать очень большие значения силы тока, в реальности они лучше всего эксплуатируются как раз при небольших токах, что в разряде, что в заряде. Поэтому ИБП, рассчитанные на заряды небольших АКБ, при работе с крупногабаритными будут заряжать их в наиболее щадящем режиме. Впрочем, в течении далеко не одних суток. Интересно обратить внимание на то, что чем выше мощность ИБП, тем больше аккумуляторов последовательно предпочитает собирать производитель. Тут все логично — большие токи разряда маленькие АКБ выдерживают очень плохо.
Подводя итоги:
1. Малогабаритные и крупногабаритные АКБ идентичны по устройству.
2. Для подавляющего большинства АКБ любого размера доливание воды является необходимой частью текущего обслуживания.
3. Лишь немногие из дорогих моделей АКБ содержат механизм рекомбинации газов и могут быть названы действительно необслуживаемыми.
4. Сам по себе водород, который выделяется при заряде (а это равно постоянной работе в ИБП) АКБ, не является существенной угрозой или проблемой.
5. Нужно очень внимательно работать с АКБ, тщательно избегая пролива даже малейших капель электролита, или лишитесь одежды.
6. Разряд и заряд малыми токами являются наиболее предпочтительными режимами эксплуатации АКБ.
емкость автомобильного АКБ, концентрация и тип применяемой кислоты

Современные аккумуляторные батареи способны питать автомобиль на протяжении длительного периода, а также генерировать мощный пусковой ток, которого достаточно для быстрого старта двигателя. Конструкция большинства автомобильных АКБ предусматривает наличие специальной кислоты, за счет которой обеспечивается прохождение требуемых процессов. При обслуживании источника энергии следует учитывать, какая кислота в аккумуляторе автомобиля.
Понятие электролита
Кислота в автомобильном аккумуляторе может находиться в жидком и гелевом состоянии. Внутри АКБ есть катод и анод, между которыми находятся специальная смесь из кислоты и дистиллированной воды.
При изготовлении специального состава для автомобильного аккумулятора нельзя использовать обычную воду. Это связано с тем, что она может содержать самые различные примеси, которые существенно ухудшают эксплуатационные качества источника питания.

Аккумуляторная жидкость может быть представлена щелочью. В продаже встречаются модели никель-кадмиевого и никель-железного типа, а также гелевые батареи. Гель получается при добавлении различных химических веществ, либо проводится пропитка стекловолокном.
Несмотря на довольно большое количество различных источников питания, которые находятся в продаже, на сегодняшний день остаются востребованными свинцово-кислотные АКБ с жидким электролитом. При необходимости они могут обслуживаться путем добавления воды или специального раствора.
Серная кислота в аккумуляторе применяется в качестве связующего элемента. Подобное вещество получило широкое применение в различных отраслях промышленности, добавляется в синтетические красители.
При создании источника питания кислота разбавляется водой, так как при высокой концентрации она может разъедать основные элементы конструкции. Рекомендуемый показатель концентрации составляет 30−35%.
В продаже встречается несколько типов серной кислоты:
- Нитрозная или башенная. Показатель концентрации в этом случае достигает значение 75%, плотность 1,67 гр/м3. Название этой разновидности кислоты связано с особенностями метода производства. Во время химической реакции происходит образование кислоты и азота. При этом оксиды постоянно циркулируют при производстве.
 Сорт Олеум. Концентрация подобной кислоты составляет 104,5%. При поставке показатель плотности выдерживается на уровне 1,897%.
Сорт Олеум. Концентрация подобной кислоты составляет 104,5%. При поставке показатель плотности выдерживается на уровне 1,897%.- Контактная. Поставляется подобная кислота при концентрации от 92 до 98%. Плотность сорта составляет 1,837%. Производство предусматривает применение обжигового газа, в ходе реакции происходит окисление основных элементов.
- Высокопроцентный олеум. Подобная кислота сегодня встречается в продаже крайне редко по причине высокой концентрации (114,6%), а также повышенной плотности (2,002 гр/см3).
- Аккумуляторная. Этот тип вещества имеет концентрацию 92%, а плотность составляет 1,833 гр/см3. Именно этот тип вещества рассматривается при поиске того, какая кислота в автомобильном аккумуляторе.
Электролит — это какая кислота, которая разводится в дистиллированной воде. Она должна обладать определенными качествами, при их изменении эксплуатационные характеристики изменяются.
Проходящие химические реакции
Свинцово-кислотные аккумуляторы получили широкое распространение по причине их простой конструкции. Накопление заряда и его отдача происходит за счет электрохимических процессов, которые могут протекать только при условии наличия электролита. К особенностям подобных источников питания можно отнести следующие моменты:
 Конструкция представлена сочетанием положительных и отрицательных пластин, которые погружены в водный раствор соляной кислоты.
Конструкция представлена сочетанием положительных и отрицательных пластин, которые погружены в водный раствор соляной кислоты.- Пластины имеют проводящие ток решетки. При их изготовлении применяется свинец, в который добавляются различные легирующие элементы. Тип применяемых добавок зависит от типа аккумулятора.
- Решетка положительных электродов покрывается диоксидом свинца, отрицательные пластины черным порошком.
- Во многом электрические характеристики аккумуляторов зависят от плотности используемого применяемого электролита.
Для защиты конструкции от воздействия внешних факторов проводится создание герметичного корпуса, который имеет отверстие для отвода газов. Электролит может менять свою плотность в зависимости от степени зарядки аккумулятора.
Для машин применяется батарея, в которой применяется кислота с плотностью 1,835 гр/см3. При добавлении дистиллированной воды плотность становится 1,3 гр/см3. Сильная разрядка источника питания приводит к падению плотности по причине уменьшения количества кислоты.
Разрядка автомобильного АКБ
Распространенные свинцово-кислотные аккумуляторы не выдерживают глубокий разряд и большое количество циклов полной зарядки. Эта особенность также связана с особенностями проходимых электрохимических процессов. К особенностям процесса разрядки отнесем:
- В начале потери заряда происходит диффузия кислоты в электроды. Этот процесс связан с тем, что в активной массе электродов поры не забиваются сульфатом.
 При постепенном забивании пор процесс диффузии притормаживается.
При постепенном забивании пор процесс диффузии притормаживается.- Процесс разряда в теории может проходить до момента, пока электролит не станет чистой водой. На практике источник энергии приходится заменять при плотности 1,15 гр/см3.
- При столь низкой плотности выделяется огромное количество сульфата свинца, что приводит к закупориванию активной массы установленных пластин.
- Показатель плотности электролита учитывается для определения степени разряженности используемого аккумулятора. Для определения требуемого показателя может использоваться специальная таблица.
При глубокой разрядке автомобильный аккумулятор способен выдавать напряжение около 2,5 В при условии отсутствия внешней нагрузки. Подключение нагрузки приводит к падению показателя до 2,1 В всего за несколько минут. Падение напряжения можно связать с тем, что на отрицательной пластине начинает формироваться слой активного вещества.

Разрядка автомобильного аккумулятора может проводиться при небольшом токе, который составляет 10% от номинальной мощности. При эксплуатации на протяжении часа напряжение падает до 2 В. Это связано с тем, что на пластинах также формируется определенное вещество, способное забирать поры активной массы. Подобные процессы становятся причиной стремительного роста внутреннего сопротивления, а также падения показателя концентрации электролита. Через некоторое время автомобильный аккумулятор полностью теряет свою способность накапливать и удерживать электрическую энергию.
Контроль состояния батареи
Важно контролировать основные показатели автомобильного аккумулятора на момент его эксплуатации. Это связано с тем, что при небольшом их изменении есть возможность провести восстановление конструкции. Контроль количества электролита в аккумуляторе проводится следующим образом:
 Некоторые автомобильные батареи имеют нанесенную шкалу, которая позволяет быстро определить уровень жидкости в корпусе.
Некоторые автомобильные батареи имеют нанесенную шкалу, которая позволяет быстро определить уровень жидкости в корпусе.- Простой способ определения емкости предусматривает использование стеклянную трубку. Для начала проводится откручивание всех пробок банок, после чего трубка погружается в конструкцию. Рекомендуемый уровень активного вещества составляет 10−12 мм.
При незначительном падении электролита восполнить уровень можно путем добавления дистиллированной воды. Рекомендуется ее приобретать в аптеке, так как в обычном магазине часто под видом дистиллированной воды продается обычная. Не рекомендуется восполнять уровень выше требуемого, так как это приводит к повышению давления и разрушению основных конструктивных элементов.
Отдельное внимание нужно уделить необслуживаемым аккумуляторам. У них сниженный показатель расхода воды, крышка имеет систему рециркуляции электролита. Однако существенно продлить срок службы конструкции можно за счет восполнения уровня жидкости путем ее добавления.
Плотность также является важным показателем, который измерить достаточно сложно. Для определения плотности применяется ареометр, который представлен сочетанием запаянной стеклянной трубки с дробью и ртутью. Определить требуемый параметр можно за счет градуированной шкалы.
Измерения плотности проводится следующим образом:
- Для начала следует снять верхнюю крышку, после чего будет получен доступ к пробкам. После этого снимаются все пробки каждой банки.
- Применяемый инструмент следует опустить в банку и набрать электролит. При этом нельзя смешивать или взбалтывать конструкцию.
- После этого инструмент вынимается и можно определить показатель плотности по нанесенной шкале.
- Некоторые ареометры имеют значение с надписями «полный заряд», «половина» или «разряженное состояние».
Проводить тестирование источника питания рекомендуется периодически или при возникновении проблем со стартом двигателя или движение при включении большого количества потребителей. При определении низкого уровня электролита или изменении плотности нужно восстановить состояние источника питания.
Поднятие плотности электролита
Поднять уровень электролита намного проще, чем повысить или снизить значение плотности. При нагреве АКБ и в результате гидролиза воды плотность может существенно подняться. Именно поэтому проводится периодический долив дистиллированной воды. Слишком низкая плотность определяет то, что нужно добавлять кислоту.
При работе с кислотой рекомендуется одевать резиновые перчатки и защитные очки. При самостоятельном разводе электролита при применении кислоты и дистиллированной воды стоит учитывать, что при их соединении проходит химическая реакция и выделяется большое количество тепла. Слишком высокая температура становится причиной закипания воды и образования брызг, что очень опасно, так как вещество может попасть на открытые участки кожи.
При средней плотности 1,2 гр/см3 поднять ее можно следующим образом:
 Для начала проводится откачивание жидкости из банок, для чего можно использовать резиновую грушу. После этого проводится вливание электролита с требуемой плотностью для восполнения половины откаченного объема.
Для начала проводится откачивание жидкости из банок, для чего можно использовать резиновую грушу. После этого проводится вливание электролита с требуемой плотностью для восполнения половины откаченного объема.- Перемешать вещество можно путем подключения небольшой нагрузки. На процесс смешивания потребуется всего несколько минут.
- Следующий шаг заключается в замере плотности. Если она низкая, электролит заливается повторно.
- Проводится повторное перемешивается, количество жидкости восполняется до требуемого уровня.
Если жидкость имеет низкий показатель плотности в заряженном состоянии аккумулятора после проведения процедуры восстановления, то старый источник питания рекомендуется заменить на новый. При своевременном обслуживании можно продлить срок эксплуатации аккумулятора до 5−7 лет. В некоторых случаях АКБ уже с магазина поставляется с низким показателем плотности, что свидетельствует о неправильном хранении.

 Сорт Олеум. Концентрация подобной кислоты составляет 104,5%. При поставке показатель плотности выдерживается на уровне 1,897%.
Сорт Олеум. Концентрация подобной кислоты составляет 104,5%. При поставке показатель плотности выдерживается на уровне 1,897%. Конструкция представлена сочетанием положительных и отрицательных пластин, которые погружены в водный раствор соляной кислоты.
Конструкция представлена сочетанием положительных и отрицательных пластин, которые погружены в водный раствор соляной кислоты. При постепенном забивании пор процесс диффузии притормаживается.
При постепенном забивании пор процесс диффузии притормаживается. Некоторые автомобильные батареи имеют нанесенную шкалу, которая позволяет быстро определить уровень жидкости в корпусе.
Некоторые автомобильные батареи имеют нанесенную шкалу, которая позволяет быстро определить уровень жидкости в корпусе. Для начала проводится откачивание жидкости из банок, для чего можно использовать резиновую грушу. После этого проводится вливание электролита с требуемой плотностью для восполнения половины откаченного объема.
Для начала проводится откачивание жидкости из банок, для чего можно использовать резиновую грушу. После этого проводится вливание электролита с требуемой плотностью для восполнения половины откаченного объема.