Как устроен кислотный аккумулятор – Свинцово-кислотный Аккумулятор: как Правильно Заряжать АКБ Зарядным Устройством, Типы Восстановления Батареи, Номинальное Напряжение
- 11.12.2020
Свинцово кислотный аккумулятор — принцип работы, как правильно заряжать
Свинцово-кислотный аккумулятор – один из самых надёжных АКБ, разработанный ещё в XIX веке, но до сих пор используемый во многих областях. В его основе лежит химическая реакция с переносом электронов от анода к катоду. Аккумулятор со временем портится при разрядке-подзарядке, так что данный процесс должен выполняться по всем правилам, чтобы продлить жизнь батареи.
Устройство и принцип работы свинцово-кислотного аккумулятора
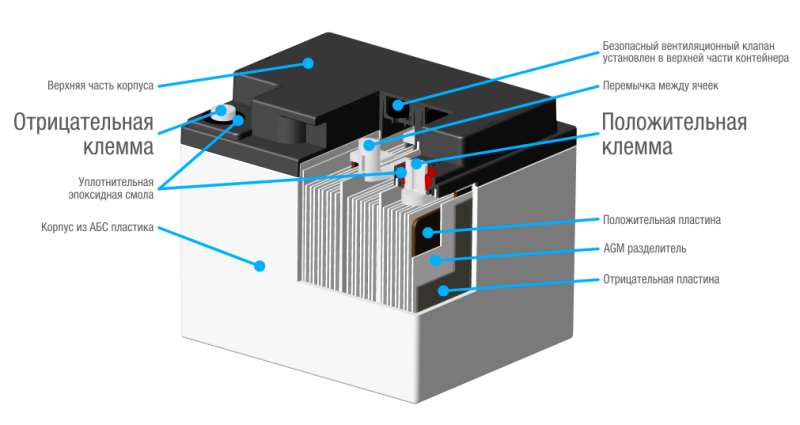

Данный тип стационарного АКБ довольно тяжёлый, так как состоит из плотно параллельно упакованных плёнок свинца и оксида свинца. И те и другие в аккумуляторе расположены очень густо. Свинцовые пластины тёмно-серого цвета с синим оттенком, оксидно-свинцовые – тёмно-коричневые с рыжим оттенком.
Обе пластины находятся в серной кислоте, из-за чего в названии АКБ есть соответствующее слово. При включении аккумулятора ток протекает от оксидно-свинцового катода к свинцовому аноду. При этом свинец выделяет электроны, которые оксид свинца принимает.
В результате изменения заряда двух пластин они вступают в реакцию с серной кислотой вокруг и превращаются в сульфаты свинца.
Pb + HSO4– => PbSO4 + H+ + 2e–
PbO2 + HSO4– + 3H+ + 2e– => PbSO4 + 2h3O
Пара пластин производит 2 вольта, поэтому, чтобы увеличить количество вольт, которое может дать аккумулятор, пластины соединяют параллельно во множество пар слоёв. Они упаковываются плотно в банку, чтобы уменьшить объём батареи. Но так как электроны должны передаваться через терминалы, то пары пластин разъединяются специальными изоляционными плёнками.
При этом аккумулятор может иметь либо высокую плотность энергии, либо мощности. То есть аккумулятор или сохраняет большое количество энергии и отдаёт её в течение длительного времени, или он отдаёт огромный заряд очень быстро. В автомобилях используется второй вариант, так как надо отдать более 400 ампер, чтобы завести двигатель.
При глубокой разрядке батареи на пластинах образуется налёт сульфата свинца. Именно из-за этого если посадить аккумулятор до нулевого заряда несколько раз, то можно просто уничтожить его. Сульфат свинца полностью покрывает поверхность пластин, после чего его уже невозможно будет зарядить.
Типы и особенности свинцово-кислотных АКБ


Идеальных аккумуляторов не существует, в инженерных конструкциях часто приходится жертвовать желаемыми характеристиками, чтобы получить необходимые параметры. Для каждой цели создан свой тип устройства.
В первую очередь АКБ делят на герметичные и негерметичные батареи. Вторые требуют постоянного контроля над уровнем электролита и состоянием катодов и анодов, могут работать лишь в определённых положениях. Аккумулятор герметичный свинцово-кислотный используется чаще, так как не нуждается в особом уходе.
Кроме того, все батареи можно разделить на следующие группы:
- Стартерные. Выдают большое количество энергии за одно мгновение, из-за чего обладают большим саморазрядом. Отлично подходят для того, чтобы заводить автомобили. Требуют определённого обслуживания и вентиляции.
- Буферные батареи. Предназначены для краткосрочного хранения небольшого количества энергии, работают в постоянном режиме подзарядки.
- Аккумуляторы для бесперебойной аппаратуры. Устанавливаются в офисах для аварийного завершения работ.
- Аккумуляторы длительного электроснабжения. Большие тяжёлые батареи, которые выдают достаточно много энергии длительное время. Используются в реанимационных отделениях на случай отключения электричества.
- Гелевые аккумуляторы. Хорошо переносят циклы заряжения-разряжения. Благодаря этому могут использоваться в сильных морозах. Среди них отдельно можно выделить солнечные батареи, которые рассчитаны на многократные циклы.
Как достигается такая вариация характеристик свинцово-кислотных аккумуляторных батарей? Если требуется выдавать огромное количество энергии за короткое время, то пластины делаются тонкими, но высокими и широкими (больше по площади поверхности), а расстояние между ними уменьшается. Благодаря этому увеличивается соотношение поверхности и массы, в результате энергия отдаётся быстрее.
Если требуется дольше сохранять энергию, но можно уменьшить мощность, то пластины делаются толще, но короче и уже (меньше по площади поверхности), а расстояние между ними увеличивается. Из-за чего уменьшается соотношение поверхности и массы, в итоге электроэнергия отдаётся медленнее.
Кроме того, на свойства аккумулятора влияют характеристики электролита и другие параметры. Гелевые электролиты хуже реагируют со свинцовыми и оксидно-свинцовыми плитами, а также делают конструкцию защищённой от вытекания. Повышает срок эксплуатации использование свинцово-кальциевых сплавов.
Области применения свинцово-кислотных аккумуляторов
Свинцово-кислотные аккумуляторы используются повсеместно, так как свинец и его оксид отвечают наиболее важным требованиям:
- элементы часто встречаются в природе и довольно легко добываются;
- они в паре способны накапливать и отдавать энергию лучше, чем все другие элементы;
- аккумуляторы из них просты и дешевы в производстве;
- долгий срок службы, возможность многократной перезарядки;
- простое обслуживание, что особенно характерно для герметичных конструкций.
Из-за этого батареи применяются в следующих областях:
- сигнализационные системы;
- стартёры в автомобилях;
- системы пожарной безопасности;
- системы аварийной подачи электроэнергии на телевидении, в реанимационных отделениях;
- электрические весы и кассовые аппараты;
- системы бесперебойного электроснабжения или аварийного отключения в компьютерной технике или их сетях;
- детские игрушки;
- в лёгких самолётах.
Тем не менее, имеются некоторые минусы:
- аккумуляторы чувствительны с холоду;
- отходы из них опасны для экологии;
- количество циклов довольно ограничено;
- есть лимиты у выдаваемой мощности.
Как правильно заряжать свинцово-кислотные аккумуляторы


Принцип зарядки состоит в том, что нужно изменить направление тока. Из-за этого электролит и материя двух пластин восстанавливает свой прежний химический состав. Данный процесс именуется циклом, и он может быть многократным. Но чтобы не повредить и продлить срок службы батареи, надо знать, как правильно заряжать свинцово-кислотный аккумулятор.
Важно! Для процедуры потребуется источник тока и устройство, которым можно регулировать силу тока и напряжение.
Прежде всего, нужно знать параметры аккумулятора, которые можно посмотреть на самой коробке устройства. Производители часто указывают информацию на английском языке. Обозначается всё это следующим образом:
| На английском | На русском |
| 12V | 12 вольт |
| 7.2Ah | 7.2 ампер-часов |
Также производитель может указывать напрямую, каким током можно заряжать аккумулятор:
| На английском | На русском |
| Standby use – 13.5-13,8V | Если вы используете батарею, как резервный источник электричества – 13,5-13,8 вольт |
| Cycle use – 14.4V | Если вы его применяете в качестве стартёра, то есть циклическое использование – 14.4 вольт |
| 2.16A MAX | При любой зарядке ток не должен превышать 2.16 ампера |
А что если производитель не указал, каким током заряжать аккумулятор? В этом случае можно пользоваться простым правилом – напряжение не должно превышать 10% от его номинальной ёмкости. То есть если у батареи указан параметр 7.2Ah, то заряжать надо при 0.72A.
После того как разобрались с основными параметрами, нужно сделать прибор, которым можно зарядить аккумулятор. Для этого потребуется крепкая коробка (лучше пластиковая) с отверстиями для вентиляции, блок питания от ноутбука, плата для регулировки тока и напряжения.
Дополнительно можно встроить многооборотистые переменные резисторы для более тонкой настройки, а также вольтамперметр. Для зарядки автомобильных аккумуляторов потребуется понижающий преобразователь напряжения и более мощный блок питания.
Собрав конструкцию, можно переходить непосредственно к главной процедуре. Для начала на неподключенном к аккумулятору устройстве нужно выставить напряжение, которым надо заряжать АКБ. Далее необходимо убавить силу тока до минимума, в результате чего сразу же упадёт напряжение. После этого подключаем устройство к аккумулятору (плюс к плюсу, минус к минусу).
В этот момент вольтамперметр будет показывать напряжение, которое есть на батарее. Включаем устройство в розетку и поднимаем силу тока до необходимой величины (метод её расчёта описан выше). В этот момент возможно незначительное снижение напряжения, говорящее о том, что ток уходит на прогрев электролита и преодоление сопротивления аккумулятора. Это нормально.
К концу зарядки аккумулятора сила тока на вольтамперметре будет практически равна нулю.
Свинцово-кислотный аккумулятор — это… Что такое Свинцово-кислотный аккумулятор?

Свинцово-кислотный аккумулятор — наиболее распространенный на сегодняшний день тип аккумуляторов, изобретен в 1859 году французским физиком Гастоном Планте. Основные области применения: аккумуляторные батареи в автомобильном транспорте, аварийные источники электроэнергии.
История
Свинцовый аккумулятор разработал в 1859—1860 годах Гастон Планте, сотрудник лаборатории Александра Беккереля. В 1878 году Камилл Фор усовершенствовал его конструкцию, покрыв пластины аккумулятора свинцовым суриком.
Принцип действия
Принцип работы свинцово-кислотных аккумуляторов основан на электрохимических реакциях свинца и диоксида свинца в сернокислотной среде.
Энергия возникает в результате взаимодействия оксида свинца и серной кислоты до сульфата (классическая версия). Проведенные в СССР исследования показали, что внутри свинцового аккумулятора протекает как минимум ~60 реакций, порядка 20 из которых протекают без участия кислоты электролита (нехимические)
Во время разряда происходит восстановление диоксида свинца на катоде[2][1] и окисление свинца на аноде. При заряде протекают обратные реакции, к которым в конце заряда добавляется реакция электролиза воды, сопровождающаяся выделением кислорода на положительном электроде и водорода — на отрицательном.
Химическая реакция (слева направо — разряд, справа налево — заряд):
В итоге получается, что при разряде аккумулятора расходуется серная кислота из электролита (и плотность электролита падает, а при заряде, серная кислота выделяется в раствор электролита из сульфатов, плотность электролита растёт). В конце заряда, при некоторых критических значениях концентрации сульфата свинца у электродов, начинает преобладать процесс электролиза воды. При этом на катоде выделяется водород, на аноде — кислород. При заряде не стоит допускать электролиза воды, в противном случае необходимо её долить для восполнения потерянного в ходе электролиза количества.
Устройство

Элемент свинцово-кислотного аккумулятора состоит из электродов (положительных и отрицательных) и разделительных изоляторов (сепараторов), которые погружены в электролит. Электроды представляют собой свинцовые решётки. У положительных активным веществом является перекись свинца (PbO
На самом деле электроды выполнены не из чистого свинца, а из сплава с добавлением сурьмы в количестве 1-2 % для повышения прочности и примесей. Иногда в качестве легирующего компонента используются соли кальция, в обеих пластинах, или только в положительных. Применение солей кальция вносит не только положительные но и много отрицательных моментов в эксплуатацию свинцового аккумулятора, например, у такого аккумулятора при глубоких разрядах существенно и необратимо снижается емкость.
Электроды погружены в электролит, состоящий из разбавленной дистиллированной водой серной кислоты (H2SO4). Наибольшая проводимость этого раствора наблюдается при комнатной температуре (что означает наименьшее внутреннее сопротивление и наименьшие внутренние потери) и при его плотности 1,23 г/см³
Однако на практике, часто в районах с холодным климатом применяются и более высокие концентрации серной кислоты, до 1,29 −1,31 г/см³.
Существуют экспериментальные разработки аккумуляторов где свинцовые решетки заменяют вспененным карбоном, покрытым тонкой свинцовой пленкой. Используя меньшее количество свинца и распределив его по большой площади, батарею удалось сделать не только компактной и легкой, но и значительно более эффективной — помимо большего КПД, она заряжается значительно быстрее традиционных аккумуляторов.
В батареях для бытовых ИБП жидкий электролит сгущают водным щелочным раствором силикатов натрия (Na2Si2O4)жидкое стекло до пастообразного состояния.
Физические характеристики
 Аккумулятор электромобиля
Аккумулятор электромобиля- Теоретическая энергоёмкость (Вт·ч/кг): около 133.
- Удельная энергоёмкость (Вт·ч/кг): 30-60.
- Теоретическая удельная энергоплотность (Вт·ч/дм³): 1250.[4]
- ЭДС заряжённого аккумулятора = 2,11 — 2,17 В, рабочее напряжение = 2 В (3 или 6 секций в итоге дают стандартные 6 В или 12 В (12 В)).[1]
- Напряжение полностью разряженного аккумулятора = 1,75 — 1,8 В (из расчета на 1 секцию). Ниже разряжать их нельзя.[1]
- Рабочая температура: от −40 °C до +40 °C.
- КПД: порядка 80-90 %
Эксплуатационные характеристики
- Номинальная ёмкость, показывает количество электричества, которое может отдать данный аккумулятор. Обычно указывается в ампер-часах, и измеряется при разряде[5] малым током (1/20 номинальной емкости, выраженной в А*ч).
- Стартерный ток (для автомобильных аккумуляторов). Характеризует способности отдавать сильные токи при низких температурах. В большинстве случаев замеряется при −18 °C (0 °F) в течение 30 секунд. Различные методики[6] замера отличаются, главным образом, допускаемым конечным напряжением.
- Резервная емкость (для автомобильных аккумуляторов). Характеризует время, в течение которого аккумулятор может отдавать ток 25А до конечного напряжения 10,5В согласно ГОСТ Р 53165-2008[7].
Эксплуатация
Ареометр может быть использован для проверки удельного веса электролита каждой секцииПри эксплуатации «обслуживаемых» аккумуляторов (с открываемыми крышками над банками) на автомобиле при движении по неровностям неизбежно происходит просачивание проводящего электролита на корпус аккумулятора. Во избежание сильного саморазряда необходимо периодически нейтрализовывать электролит протиранием корпуса, например слабым раствором пищевой соды или разведенным в воде до состояния консистенции жидкой сметаны хозяйственным мылом. Кроме того, особенно в жаркую погоду, происходит испарение воды из электролита, что увеличивает его плотность, увеличивая напряжение на аккумуляторе, и может оголить свинцовые пластины. Поэтому необходимо следить за уровнем электролита и своевременно доливать дистиллированную воду.
Такие нехитрые операции вместе с проверкой автомобиля на утечку тока и периодической подзарядкой аккумулятора могут на несколько лет продлить срок эксплуатации батареи.
Свинцово-кислотный аккумулятор при низких температурах
По мере снижения окружающей температуры, параметры аккумулятора ухудшаются, однако в отличие от прочих типов аккумуляторов, свинцово-кислотные снижают их относительно медленно, что не в последнюю очередь обусловило их широкое применение на транспорте. Считается что свинцово-кислотный аккумулятор теряет ~1% ёмкости на каждый градус от +20°C. Т.е. в -30°C свинцово-кислотный аккумулятор будет иметь 50% ёмкости.
Снижение ёмкости и токоотдачи при низких температурах обусловлено, в первую очередь, ростом вязкости электролита, который уже не может в полном объёме поступать к электродам, и вступает в реакцию лишь в непосредственной близости от них, быстро истощаясь.
Не полностью заряженный аккумулятор в мороз может раздуться из-за замерзания электролита низкой плотности (близкой к 1.10)
Хранение
Свинцово-кислотные аккумуляторы необходимо хранить только в заряжённом состоянии. При температуре ниже −20 °C заряд аккумуляторов должен проводиться постоянным напряжением 2,45 В/секцию 1 раз в год в течение 48 часов. При комнатной температуре — 1 раз в 8 месяцев постоянным напряжением 2,35 В/секцию в течение 6-12 часов. Хранение аккумуляторов при температуре выше 30 °C не рекомендуется.
Слой грязи и накипи на поверхности аккумулятора создаёт проводник для тока от одного контакта к другому и приводит к саморазряду аккумулятора,после чего начинается преждевременная сульфатизация пластин и поэтому поверхность аккумулятора необходимо поддерживать в чистоте. Хранение свинцово-кислотных аккумуляторов в разряженном состоянии приводит к быстрой потере их работоспособности.
При длительном хранении аккумуляторов и разряде их большими токами (в стартерном режиме), или при уменьшении ёмкости аккумуляторов, нужно проводить контрольно-тренировочные циклы, то есть разряд-заряд токами номинальной величины.
Износ свинцово-кислотных аккумуляторов
При использовании технической серной кислоты и не дистиллированной воды, ускоряются саморазряд, сульфатация, разрушение пластин и уменьшение ёмкости аккумуляторной батареи.
В результате каждой реакции образуется нерастворимое вещество — сернокислый свинец PbSO4, осаждающийся на пластинах, который образует диэлектрический слой между токоотводами и активной массой. Это один из факторов, влияющий на срок службы свинцово-кислотной аккумуляторной батареи.
Основными процессами износа свинцово-кислотных аккумуляторов являются:
- сульфатация пластин[1], заключающаяся в образовании крупных кристаллитов сульфата свинца, который препятствует протеканию обратимых токообразующих процессов;
- коррозия электродов, то есть электрохимические процессы окисления и растворения в электролите, что вызывает осыпание материала электродов;
- слабая механическая прочность или плохое сцепление активной массы с токоотводами, что приводит к опаданию активной массы;[9][1]
- оползание и осыпание активной массы положительных электродов, связанное с разрыхлением, нарушением однородности.[1]
Хотя батарею, вышедшую из строя по причине физического разрушения пластин, самому починить нельзя, некоторые источники описывают химические растворы и прочие способы способные «десульфатировать» пластины. Простой но вредный для жизни аккумулятора способ предполагает использование раствора сульфата магния.[1] Раствор заливается в секции после чего батарею разряжают и заряжают несколько раз. Сульфат свинца и прочие остатки химической реакции осыпаются при этом на дно батареи, что может привести к замыканию секции поэтому обработанные секции желательно промыть и заполнить новым электролитом номинальной плотности. Это позволяет несколько продлить срок использования устройства. Если батарея имеет одну или несколько секций которые не работают (то есть не дают 2.17 вольта — например если корпус имеет трещины) возможно соединить две (или больше) батареи последовательно: к плюсовому контакту первой батареи подключаем плюсовой провод потребителя, к минусовому контакту второй батареи — минусовой провод потребителя, а две оставшихся контакта батареи соединяются кабелем. Такая батарея имеет суммарное напряжение работающих секций и поэтому количество работающих секций должно быть не более шести — то есть необходимо слить электролит из излишних секций. Такой вариант подходит для транспортных средств с большим моторным отсеком.
Вторичная переработка
 Кодовый символ указывающий, что свинцовые батареи могут быть вторично переработаны
Кодовый символ указывающий, что свинцовые батареи могут быть вторично переработаныВторичная переработка для этого вида аккумуляторов играет важную роль, так как свинец, содержащийся в аккумуляторах является тяжелым металлом и наносит серьёзный вред при попадании в окружающую среду. Свинец и его соли должны быть переработаны на специальных предприятиях для возможности его вторичного использования.
Выброшенные аккумуляторы часто используются как источник свинца для кустарной переплавки, например, в рыболовные грузила, дробь или гири. Для этого из аккумулятора сливается электролит, остатки нейтрализуются промыванием каким-либо безвредным основанием (например, гидрокарбонатом натрия), после чего корпус батареи разбивается и извлекается металлический свинец.
См. также
Примечания
Ссылки
Принцип работы свинцово-кислотного аккумулятора | AUTO-GL.ru

Свинцово-кислотный аккумулятор — один из самых распространенных типов батарей, использующийся в качестве источника электроэнергии для автомобиля, мотоцикла, мопеда, или в случае необходимости создания запасных источников питания.
Содержание статьи
Первая модель свинцово-кислотного аккумулятора была создана в середине XIX века ученым Гастоном Планте. Тогда его конструкция подразумевала две свинцовых пластины, стеклянную колбу с серной кислотой и обычное полотно в роли сепаратора. Это устройство обладало малой емкостью заряда и не получило достаточного распространения. Но идею оценили другие ученые и стали экспериментировать с составом электродов. В итоге самой удачной оказалась решетчатая конструкция из сплава с добавлением сурьмы. Изобретение генераторов постоянного тока решило проблему с подходящим источником энергии, и свинцово-кислотные аккумуляторные батареи наконец-таки получили широкое распространение.
В конце ХХ века их конструкция усложнилась, появились необслуживаемые аккумуляторы, в электроды которых был добавлен кальций. Это нововведение позволило существенно сократить расход воды. В идеале, батареи такого типа способны работать без пополнения количества воды в электролите весь срок службы. Кстати, при необходимости утратившее работоспособность устройство можно попробовать восстановить, используя принцип действия кислотных аккумуляторов.
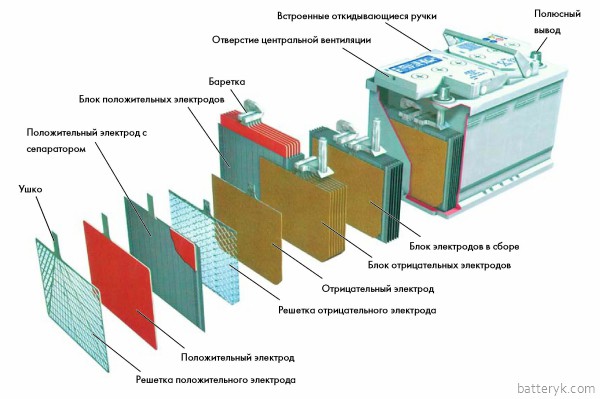
Кислотные аккумуляторы — вторичные источники тока, который образуется за счет реакций восстановления и окисления, проходящих между материалом электродов и электролитом. В качестве электролита используется водный раствор серной кислоты. Остановимся на подробнее на устройстве аккумуляторов этого типа.
По конструктивным особенностям современные батареи делятся на три типа:
- С жидким электролитом. Могут быть как обслуживаемыми, так и необслуживаемыми. Электролит — смесь серной кислоты и воды, находящаяся в жидком виде. В версии, требующей обслуживания, пластины изготавливаются из свинца с добавлением сурьмы и мышьяка. В таких батареях высок расход воды, что делает обслуживание аккумулятора не очень простой задачей. После замены сурьмы на кальций в состав сплава отрицательной пластины появились так называемые гибридные аккумуляторы, более удобные в эксплуатации, чем их предшественники. И, наконец, с добавлением кальция в обе пластины началась эра устройств, не требующих восстановления количества воды весь срок службы. Несмотря на совершенство конструкции, у них есть один минус — плохо переносят почти полный разряд, особенно в условиях отрицательной температуры.
- Гелевые АКБ. В этих конструкциях электролит находится в сгущенном состоянии благодаря добавлению кремния. Плюс такой конструкции в том, что батарея становится абсолютно герметичной. Газ, выделяющийся в процессе химических реакций, находит себе место в порах геля, а при обратных реакциях вновь присоединяется к раствору серной кислоты. Но это очень капризные батареи. Они требуют неукоснительного соблюдения условий эксплуатации, чувствительны к перепадам температур, справляются с высокой нагрузкой хуже, чем их жидкостные собратья. Но они хорошо справляются с сильной разрядкой, действительно не требуют дополнительного обслуживания. Гелевые АКБ чаще используются в качестве стационарно резервного источника питания и редко устанавливаются на транспорт.
- AGM-аккумуляторы. Это самый современный вид батарей, сочетающий все достоинства предыдущих вариантов. Электролит остается жидким, но циркулирует в пористой конструкции из тончайших стеклянных волокон. Два вида пор — большие и маленькие — обеспечивают свободное перемещение газа до того, как запустится обратная реакция. Конструкция устройства такова, что аккумулятор может работать, даже если его оболочка незначительно повреждена. Не боятся они и холода, глубокой разрядки, вибраций. Единственная уязвимость такого устройства — чувствительность к перепадам напряжения. Эту проблему можно решить, контролируя работу генератора и пользуясь надежным ЗУ.
У любого вида аккумулятора есть два основных параметра: емкость и напряжение. Емкость определяет количество энергии, которое аккумулятор может отдать при рабочем напряжении, измеряется в Ампер-часах. Она зависит от площади свинцовых пластин, участвующих в химических реакциях. При износе аккумулятора его емкость уменьшается из-за естественных потерь в размере пластин.

Напряжение — количество электрического тока, отдаваемое батареей. Измеряется в вольтах, зависит от плотности электролита. Оба параметра необходимо контролировать, так как от них зависит работоспособность устройства.
Для измерения напряжения используется вольтмер, правильные показатели — от 11 до 13 вольт (раньше производились аккумуляторы с напряжением 6 вольт, теперь они считаются устаревшими).
Чтобы измерить емкость, существует несколько методов:
- «Нагрузочная вилка» — измерение напряжения при эталонной нагрузке. Аккумулятор должен быть полностью заряжен.
- Специальный индикатор, способный посылать сигнал, определяющий площадь свинцовых пластин, и преобразовывать его в цифры. Не требует особых условий использования.
- В домашних условиях можно подключить мощную автомобильную галогеновую лампу и замерить в это время напряжение. Ели в течение 2 минут оно держится на уровне ~11 вольт, а свет лампы ровный и сильный — все в порядке.
В зависимости от типа используемого аккумулятора, условия его эксплуатации будут сильно отличаться. Единственная общая черта — всех их необходимо вовремя заряжать. Так, обслуживаемая батарея требует долива воды в аккумулятор, что может представлять собой опасность — кислота нагревает воду, и кипяток может ощутимо обжечь автовладельца.

Конструкция необслуживаемых аккумуляторов не предполагает возможности пополнения запаса воды в них. Но, даже если произвести небольшие изменения в конструкции, обжечься кипятком все равно будет проблематично. Для батарей такого типа важно не допускать больших колебаний напряжения. Это справедливо и для автомобильного, и для мотоциклетного аккумулятора. Но герметичный корпус уменьшает варианты восстановления устройства.
Как восстановить батарею? Часто снижение емкости или напряжения аккумулятора происходит из-за того, что некоторые участки электролита слишком уплотнились. При многоразовой небольшой зарядке эти области разжижаются, и потенциал устройства восстанавливается. Существует несколько рецептов восстанавливающего раствора, который несколько улучшает состояние устройства. К сожалению, его использование несколько затруднено на батареях с герметизированным корпусом, так как слить из него этот раствор будет проблематично.
Какой бы аккумулятор ни был установлен на транспортном средстве, важно соблюдать инструкцию по его использованию, вовремя заряжать и, при необходимости, пополнять запас воды в электролите. Тогда срок службы батареи будет максимально долгим.
Свинцово-кислотный аккумулятор: инструкция по обслуживанию и эксплуатации
Аккумуляторная батарея – неотъемлемая составляющая любого транспортного средства, которое приводится в движение за счёт двигателя. Первый аккумулятор, а именно свинцово-кислотный, появился ещё в XIX веке и по сей день не утратил своей актуальности. Время идёт, меняются эпохи, а замены столь востребованному устройству пока не придумали. Конечно, появляются его усовершенствованные виды, но это не новое оборудование, а лишь модернизация старого.
Что такое свинцово-кислотный аккумулятор
Прибор, который «прячется» под капотом и обеспечивает возможность запуска двигателя, есть не что иное, как свинцово-кислотный аккумулятор. Это устройство также обеспечивает питание бортовой сети транспортного средства при заглушенном моторе.
Сама батарея электрический ток не вырабатывает, а лишь накапливает его благодаря протекающим внутри неё электрохимическим реакциям.
Как правило, АКБ представляет собой компактный корпус, изготовленный из высокопрочного полипропилена – материала, являющегося хорошим диэлектриком и при этом химически пассивного – не способного вступать в реакцию с кислотой. Внутреннее пространство батареи занято электродами, которые разделены между собой не проводящими ток сепараторами. Всё остальное свободное пространство заполнено электролитом – водным раствором серной кислоты.
Растворять кислоту необходимо исключительно дистиллированной водой! Она полностью очищена от различных примесей, которые обязательно присутствуют в жидкости, взятой из естественного водоёма или водопроводного крана.
Электроды – это свинцовые пластины, собранные в блоки. Они имеют как положительный (катоды), так и отрицательный (аноды) заряд. При размещении внутри корпуса катоды и аноды чередуются.
Сверху прибор закрыт крышкой, на которую помещены токовыводящие клеммы. Они служат:
- для соединения с генератором и двигателем при установке на автомобиль;
- для подключения «крокодилов» зарядного устройства в случае необходимости восстановления потраченного заряда.
Автомобильные аккумуляторы бывают двух типов:
- Обслуживаемые – не очень удобны в эксплуатации, требуют постоянного контроля уровня электролита и его плотности, имеют на крышке специальные выкручивающиеся пробки для доливки жидкости и возможности осуществления замеров.
- Необслуживаемые – наиболее современный тип батарей, которые нуждаются лишь в своевременной и полноценной зарядке, имеют герметичный корпус, не позволяющий заглянуть во внутрь.
На корпусе каждого прибора установлена маркировочная табличка, содержащая информацию об основных характеристиках источника питания: ёмкость, напряжение, пусковой ток и так далее.
Кроме того, внедрение новейших технологий в производственный процесс позволило наладить выпуск АКБ, в которых жидкая среда заменена гелеобразной. Конечно, эти устройства более надёжны и практичны, но из-за высокой стоимости не нашли широкого применения.
Разновидности
Свинцово-кислотные аккумуляторные батареи не только отличаются типом конструкции, но и имеют множество разновидностей. К самым популярным и востребованным относятся:
- Lead-Acid – классический вид батарей обслуживаемого типа. Эта группа включает устройства, материалом для изготовления электродов которых служит свинец не только в чистом виде, но и с различными примесями: сурьма, кальций. В модельном ряду можно встретить источники с различной величиной напряжения. Из эксплуатационных недостатков отмечают предрасположенность к повышенному саморазряду и необходимость регулярного обслуживания.
- OPzV – компактные, долговечные и мощные устройства в герметичном корпусе, не требующие никакого обслуживания. Конструктивные особенности: пластины последнего поколения выполнены в форме трубок, вместо жидкого электролита используется гель. Срок службы составляет как минимум два десятка лет. Область применения – электромобили.
- VRLA, что в переводе с английского означает «клапанно-регулируемые свинцово-кислотные». Это герметичные необслуживаемые устройства, снабжённые клапаном для выхода газов в случае перезарядки или какой-то неисправности. Могут эксплуатироваться в любом положении.
- AGM VRLA – устройства нового поколения, изготовленные по уникальной технологии. Не требуют обслуживания, к тому же они лишены практически всех недостатков классических кислотных. Дело в том, что электролит в них отсутствует в жидком виде, а «заперт» в сепараторе абсорбирующего типа. Это позволило выпускать батареи, отличающиеся компактными размерами, увеличенной ёмкостью и повышенной надёжностью.
- GEL VLRA – довольно дорогие источники энергии, в которых электролит превращён в гелеобразную массу. Стоит отметить, что они надёжны в работе лишь в тёплое время года при положительных температурах наружного воздуха. В мороз гель застывает, и прибор создаёт множество проблем автовладельцам, особенно в условиях сурового российского климата.
Аккумуляторные батареи с технологией AGM
В конце прошлого века появились новейшие устройства – свинцово-кислотные необслуживаемые аккумуляторные батареи, при производстве которых впервые была применена самая передовая на тот момент технология AGM. Разработана она американскими учёными, а аббревиатура AGM дословно с английского переводится как «прокладка, пропитанная стекловолокном».
В чём же принципиальное отличие устройств-новинок от обычных классических?
Первое – отсутствие жидкой среды. Электролитом на основе серной кислоты заполняют поры сепараторов из стекловолокна. Пластины точно так же собираются в блоки, образуя электроды, а между ними прокладываются «брикеты с электролитом».
Второе – эта конструктивная особенность обеспечивает наиболее рациональное размещение пластин внутри корпуса, позволяя поместить их намного больше, чем при обычной компоновке батареи. Получается, что при одинаковых габаритах ёмкость AGM аккумулятора будет значительно выше.
Третье – материал пластин – чистейший свинец. Этим обусловлен во многом продолжительный срок службы и повышенная эффективность циклов «заряд – разряд».
Технология AGM предусматривает две конфигурации пластин:
- Обычные плоские. Устройства выпускаются как на территории Америки, так и в Европе. Редко, но всё-таки можно встретить в торговой сети.
- Спиральные. Батареи с ними производятся исключительно в Америке. Они отсутствуют на европейском и отечественном рынке. Используются преимущественно в военной авиации.
Преимущества свинцово-кислотных аккумуляторов
Если даже рассматривать обобщённо основные достоинства классических АКБ, то они во многом будут зависеть от типа батареи. В связи с чем рассмотрим отдельно преимущества обслуживаемых источников питания и главные плюсы герметичных свинцово-кислотных аккумуляторов.
Почему же стоит остановить свой выбор на классическом устройстве, нуждающемся в обслуживании?
Благодаря наличию специальных пробок на корпусе мы можем добраться до внутренностей прибора, а именно:
- визуально оценить состояние пластин;
- замерить уровень и плотность электролита;
- при необходимости долить дистиллированной воды.
Чем же так хороши современные необслуживаемые источники энергии:
- Удалось решить главную и самую злободневную проблему – избавиться от сульфатации пластин, ведь они всегда теперь находятся в электролитном растворе.
- Исключена возможность утечки жидкой среды благодаря полной герметичности корпуса.
- Отсутствует испарение воды из раствора при его нагревании – она просто оседает на стенках в виде конденсата, а потом стекает вниз. Таким образом удаётся сохранять неизменным уровень электролита.
Недостатки свинцово-кислотных аккумуляторов


У новейших устройств, которые не нуждаются в обслуживании, недостаток один – перемычки между банками находятся внутри герметичного корпуса и доступ к ним исключён. Следовательно, при необходимости осуществить замеры напряжения не представляется возможным.
У их предшественников, более устаревших, но ещё используемых довольно часто источников, недостатков намного больше:
- Высока вероятность сульфатации пластин:
- негерметичный корпус позволяет электролиту выкипать;
- вода в растворе испаряется, вследствие чего происходит повышение плотности оставшейся жидкости.
- Необходимость регулярного контроля уровня жидкой среды.
- Не исключена возможность замыкания клемм из-за вытекания жидкого содержимого из-под пробок.
Характеристики свинцово-кислотных аккумуляторов
Однотипные АКБ различаются между собой значениями параметров основных характеристик. Опираясь именно на эти данные, осуществляется подбор источника энергии для того или иного транспортного средства. Кроме того, величины самых важных характеристик помещаются на маркировочную табличку корпуса. К ним относят:
- Ёмкость. Она бывает двух видов:
- электрическая – это определённое количество энергии, которое способен отдать аккумулятор в процессе разряда, например, при запуске двигателя, выражается в Ампер-часах;
- разрядная – показывает количество электрической энергии, которое можно получить от данного источника.
- Номинальное напряжение, как правило, стандартно для определённых групп транспортных средств:
- легковые автомобили – 12 В;
- грузовые – 24 В;
- мотоциклы – 6 В.
- Саморазряд – это способность батареи утрачивать заряд при длительном хранении или отсутствии эксплуатации транспортного средства на протяжении долгого времени. Критериями, вызывающими самопроизвольный разряд, являются: условия хранения, приготовление электролитного раствора с использованием обычной воды, переворачивание источников обслуживаемого типа. Определяется в процентах. Чем ниже значение этого параметра, тем лучше.
Где применяются свинцово-кислотные аккумуляторы
Сфера применения аккумуляторных батарей свинцово-кислотного вида довольно обширна:
- Они просто незаменимы в автомобильной промышленности – все стартерные двигатели комплектуются именно этими источниками энергии.
- Авиационная промышленность. Сюда относятся AGM аккумуляторы, производство которых основано на применении передовых технологий.
- Источники бесперебойного питания.
- Различные виды мототехники.
- Лодочные моторы.
Принцип работы
Принцип действия кислотных батарей основан на протекании электрохимических процессов внутри корпуса. В результате взаимодействия свинцовых электродов с электролитом на основе серной кислоты между ними возникает разность потенциалов. Другими словами, при запуске двигателя происходит разряд батареи – металл и кислота вступают в электрохимическую реакцию, химическая энергия которой тут же преобразуется в электрическую.
При зарядке АКБ, наоборот, электрическая энергия превращается в химическую.
Эксплуатация свинцово-кислотных аккумуляторов
Эксплуатация современных аккумуляторных батарей не доставит особых хлопот даже новичкам. Но её правила различаются в зависимости от типа источника.
Общие правила эксплуатации любых АКБ:
- не допускать хранения устройства в полностью разряженном состоянии;
- строго соблюдать условия хранения, установленные производителем;
- не нарушать порядок подключения к клеммам;
- всегда иметь в наличии зарядное устройство для своевременного восстановления заряда;
- надёжно закреплять батарею в специальном углублении под капотом автомобиля;
- не забывать утилизировать вышедший из строя источник энергии.
Свинцово-кислотные аккумуляторы ремонту не подлежат.
Дополнительно для герметичных устройств: нельзя вскрывать корпус необслуживаемой батареи – неизбежно получение ожога путём выплёскивания электролита.
Рекомендации для обслуживаемых устройств:
- регулярно контролировать уровень и плотность электролита;
- использовать исключительно дистиллированную воду для заливки.
Как заряжать свинцово-кислотные аккумуляторы
Обычно в процессе эксплуатации транспортного средства осуществляется восстановление затраченной ёмкости – зарядка свинцового аккумулятора. При исправном генераторе автомобиля и регулярном использовании машины батарея будет всегда в заряженном состоянии, полностью готова к работе.
Но бывают ситуации, когда требуется вернуть мощность источнику энергии, воспользовавшись специальным зарядным устройством для свинцово-кислотных аккумуляторов, номинальное напряжение которых составляет 12 В. Такая необходимость может возникнуть в следующих случаях:
- при неисправности цепи «генератор – аккумуляторная батарея»;
- при эксплуатации авто редко и на короткие расстояния;
- при запуске мотора при слишком низких температурах воздуха.
Основные этапы зарядного процесса:
- Устанавливаем устройство на ровную горизонтальную поверхность.
- Подключаем «крокодильчики» зарядника к клеммам батареи, строго соблюдая полярность.
- Выставляем зарядный ток.
Приступить к зарядке можно только после того, как температура электролитной жидкости достигнет комнатной.
Ток заряда
Основные параметры зарядки свинцово-кислотных аккумуляторов во многом определяются их разновидностью. Так, классическое устройство, заполненное электролитом в жидком виде, требует установки токовой величины заряда в пределах 10 % номинальной ёмкости, указанной на маркировке.
Что же касается источников с гелеобразным наполнителем, то здесь параметр тока можно смело выставлять равным 20–30 % номинала ёмкостной характеристики.
Для AGM аккумуляторов сила тока может варьироваться в интервале от 10 % до 30 % от заявленной производителем ёмкости.
Время заряда
Как долго следует заряжать свинцово-кислотный аккумулятор? Продолжительность зарядного процесса напрямую зависит от степени разряженности батареи. В среднем на полноценную зарядку обычной АКБ, как правило, уходит от 8 до 12 часов. Сильно разряженное устройство можно привести в состояние полной готовности, используя высокие токи. Но такой способ следует использовать только в случае крайней нужды и очень редко.
Источники энергии, произведённые по AGM технологии, заряжаются намного быстрее, но для них требуется приобретение специального зарядного устройства, позволяющего осуществлять процесс поэтапно.
Ёмкость и напряжение
Желательно не допускать полной потери ёмкости. Чем больше величина остаточной ёмкости, тем меньше потребуется времени на зарядку.
Напряжение полностью заряженной аккумуляторной батареи без нагрузки обычно составляет 12,7–13 В. При работающем моторе этот показатель возрастает примерно на полторы единицы.
При зарядке максимальная величина напряжения в оптимальном варианте не должна превысить 14,6 В. В противном случае это может привести к перезарядке, закипанию электролитной жидкости, а также самым негативным образом сказаться на дальнейшей работе самого прибора.
Восстановление аккумулятора
Бытует мнение, что после глубокого разряда невозможно вернуть устройству номинал мощности, размер которого указан на маркировке. Но многочисленные исследования показали, что это абсолютно не так. Существуют методы, позволяющие вернуть источник энергии на первоначальный уровень мощности.
Как можно восстановить свинцово-кислотный аккумулятор, вернув ему полноценную функциональность? Алгоритм действий достаточно прост, но требует строгого соблюдения их последовательности:
- Подключить зарядное устройство к клеммам источника, соблюдая полярность.
- Установить следующие параметры зарядки:
- ток – 5 % от номинала ёмкости;
- напряжение – 2,45 В.
- Запустить восстановительный процесс, который будет протекать медленно и долго.
- Для достижения наилучшего результата рекомендуется осуществить 2–3 цикла «заряд – разряд»: сначала постепенно доводить мощность до максимально возможного предела, потом такая же неспешная глубокая разрядка, а затем всё по новому кругу.
Реанимацию нужно производить только при положительных температурах. Температура жидкости внутри устройства должна соответствовать аналогичному показателю окружающей среды.
Что же касается восстановления свинцово-кислотных AGM аккумуляторов, то их предварительно нужно «смочить». Случаются такие ситуации при нарушении правил эксплуатации, когда «брикеты» с электролитом высыхают, и батарея утрачивает способность принимать заряд. Нужно, набрав в шприц дистиллированной воды, впрыснуть её в сепараторы в небольшом количестве. А спустя несколько часов, можно приступать к реанимации устройства.
Свинцово-кислотный аккумулятор: принцип работы, виды
Свинцово-кислотный аккумулятор — один из самых распространенных типов батарей, использующийся в качестве источника электроэнергии для автомобиля, мотоцикла, мопеда, или в случае необходимости создания запасных источников питания.
Первая модель свинцово-кислотного аккумулятора была создана в середине XIX века ученым Гастоном Планте. Тогда его конструкция подразумевала две свинцовых пластины, стеклянную колбу с серной кислотой и обычное полотно в роли сепаратора. Это устройство обладало малой емкостью заряда и не получило достаточного распространения. Но идею оценили другие ученые и стали экспериментировать с составом электродов. В итоге самой удачной оказалась решетчатая конструкция из сплава с добавлением сурьмы. Изобретение генераторов постоянного тока решило проблему с подходящим источником энергии, и свинцово-кислотные аккумуляторные батареи наконец-таки получили широкое распространение.
В конце ХХ века их конструкция усложнилась, появились необслуживаемые аккумуляторы, в электроды которых был добавлен кальций. Это нововведение позволило существенно сократить расход воды. В идеале, батареи такого типа способны работать без пополнения количества воды в электролите весь срок службы. Кстати, при необходимости утратившее работоспособность устройство можно попробовать восстановить, используя принцип действия кислотных аккумуляторов.

Кислотные аккумуляторы — вторичные источники тока, который образуется за счет реакций восстановления и окисления, проходящих между материалом электродов и электролитом. В качестве электролита используется водный раствор серной кислоты. Остановимся на подробнее на устройстве аккумуляторов этого типа.
По конструктивным особенностям современные батареи делятся на три типа:
- С жидким электролитом. Могут быть как обслуживаемыми, так и необслуживаемыми. Электролит — смесь серной кислоты и воды, находящаяся в жидком виде. В версии, требующей обслуживания, пластины изготавливаются из свинца с добавлением сурьмы и мышьяка. В таких батареях высок расход воды, что делает обслуживание аккумулятора не очень простой задачей. После замены сурьмы на кальций в состав сплава отрицательной пластины появились так называемые гибридные аккумуляторы, более удобные в эксплуатации, чем их предшественники. И, наконец, с добавлением кальция в обе пластины началась эра устройств, не требующих восстановления количества воды весь срок службы. Несмотря на совершенство конструкции, у них есть один минус — плохо переносят почти полный разряд, особенно в условиях отрицательной температуры.
- Гелевые АКБ. В этих конструкциях электролит находится в сгущенном состоянии благодаря добавлению кремния. Плюс такой конструкции в том, что батарея становится абсолютно герметичной. Газ, выделяющийся в процессе химических реакций, находит себе место в порах геля, а при обратных реакциях вновь присоединяется к раствору серной кислоты. Но это очень капризные батареи. Они требуют неукоснительного соблюдения условий эксплуатации, чувствительны к перепадам температур, справляются с высокой нагрузкой хуже, чем их жидкостные собратья. Но они хорошо справляются с сильной разрядкой, действительно не требуют дополнительного обслуживания. Гелевые АКБ чаще используются в качестве стационарно резервного источника питания и редко устанавливаются на транспорт.
- AGM-аккумуляторы. Это самый современный вид батарей, сочетающий все достоинства предыдущих вариантов. Электролит остается жидким, но циркулирует в пористой конструкции из тончайших стеклянных волокон. Два вида пор — большие и маленькие — обеспечивают свободное перемещение газа до того, как запустится обратная реакция. Конструкция устройства такова, что аккумулятор может работать, даже если его оболочка незначительно повреждена. Не боятся они и холода, глубокой разрядки, вибраций. Единственная уязвимость такого устройства — чувствительность к перепадам напряжения. Эту проблему можно решить, контролируя работу генератора и пользуясь надежным ЗУ.
У любого вида аккумулятора есть два основных параметра: емкость и напряжение. Емкость определяет количество энергии, которое аккумулятор может отдать при рабочем напряжении, измеряется в Ампер-часах. Она зависит от площади свинцовых пластин, участвующих в химических реакциях. При износе аккумулятора его емкость уменьшается из-за естественных потерь в размере пластин.

Напряжение — количество электрического тока, отдаваемое батареей. Измеряется в вольтах, зависит от плотности электролита. Оба параметра необходимо контролировать, так как от них зависит работоспособность устройства.
Для измерения напряжения используется вольтмер, правильные показатели — от 11 до 13 вольт (раньше производились аккумуляторы с напряжением 6 вольт, теперь они считаются устаревшими).
Чтобы измерить емкость, существует несколько методов:
- «Нагрузочная вилка» — измерение напряжения при эталонной нагрузке. Аккумулятор должен быть полностью заряжен.
- Специальный индикатор, способный посылать сигнал, определяющий площадь свинцовых пластин, и преобразовывать его в цифры. Не требует особых условий использования.
- В домашних условиях можно подключить мощную автомобильную галогеновую лампу и замерить в это время напряжение. Ели в течение 2 минут оно держится на уровне ~11 вольт, а свет лампы ровный и сильный — все в порядке.
В зависимости от типа используемого аккумулятора, условия его эксплуатации будут сильно отличаться. Единственная общая черта — всех их необходимо вовремя заряжать. Так, обслуживаемая батарея требует долива воды в аккумулятор, что может представлять собой опасность — кислота нагревает воду, и кипяток может ощутимо обжечь автовладельца.

Конструкция необслуживаемых аккумуляторов не предполагает возможности пополнения запаса воды в них. Но, даже если произвести небольшие изменения в конструкции, обжечься кипятком все равно будет проблематично. Для батарей такого типа важно не допускать больших колебаний напряжения. Это справедливо и для автомобильного, и для мотоциклетного аккумулятора. Но герметичный корпус уменьшает варианты восстановления устройства.
Как восстановить батарею? Часто снижение емкости или напряжения аккумулятора происходит из-за того, что некоторые участки электролита слишком уплотнились. При многоразовой небольшой зарядке эти области разжижаются, и потенциал устройства восстанавливается. Существует несколько рецептов восстанавливающего раствора, который несколько улучшает состояние устройства. К сожалению, его использование несколько затруднено на батареях с герметизированным корпусом, так как слить из него этот раствор будет проблематично.
Какой бы аккумулятор ни был установлен на транспортном средстве, важно соблюдать инструкцию по его использованию, вовремя заряжать и, при необходимости, пополнять запас воды в электролите. Тогда срок службы батареи будет максимально долгим.
чтобы больше не было отвратительно читать то, что люди о них пишут
Случайно узрел статью с комментариями к ней, и так злость во мне закипела по поводу безграмотности людей в области кислотных (свинцовых в простонародье) аккумуляторов, что не выдержал и решил написать «гикам» (чтобы быть гиком, как оказывается, мало купить дорогой телефон) краткую статью об аккумуляторах. С рассмотрением тех ошибок, которые мне постоянно мусолят глаза и вызывают праведное желание их исправить.
Начнем с названия. Я очень часто вижу что тремя буквами А-К-Б называют все что можно зарядить, абсолютно любой аккумулятор. Особенно тремя буквами люди любят называть аккумуляторы типа Li-ion. На самом-же деле АКБ аббревиатура от Аккумуляторная Кислотная Батарея. Под ними подразумевается лишь один тип аккумулятора — свинцовый кислотный. С современной точки зрения это название вызывает некоторый когнитивный диссонанс т.к. на данный момент значение слова «батарейка» т.е. гальванического элемента который зарядить нельзя перешло на слово «батарея». И получается как будто бы из-за слова «аккумуляторная» это аккумулятор который зарядить можно, а из-за слова «батарея» это как будто батарейка которую зарядить нельзя. В реальности-же батарея — просто цепь гальванических элементов и со словом «батарейка» имеет общий лишь корень.
Далее перейдем к некоторым мифам, а именно главный миф — АКБ для автомобиля имеет некие существенные отличия от АКБ для ИБП. И вот нельзя их применять и там и там.
С химической точки зрения любые АКБ абсолютно одинаковы. Как-же они устроены? Очень кратко — если аккумулятор заряжен, то один электрод представляет собой свинцовую решетку с нанесенной на нее пастой из PbO2, второй -такую-же решетку с пастой губчатого свинца. Электролитом служит раствор серной кислоты. В процессе разряда PbO2 восстанавливается и взаимодействуя с серной кислотой образует PbSO4. Свинец на другом электроде окисляется и опять-же образует PbSO4. В конце разрядки мы имеем обе решетчатые пластины заполненные (более или менее) сульфатом свинца. При зарядке аккумулятора происходит электролиз и из сульфата свинца вновь образуется диоксид и металлический свинец.
Конечно-же, тут нужно подчеркнуть, что электроды при этом не равны и путать их полярность не стоит т.к. еще на стадии производства в намазку электродов вводятся соответствующие добавки, улучшающие их эксплуатационные свойства. При этом добавки полезные для одного электрода вредны для другого. В очень старые времена, где-то в начале прошлого века, в условиях простых аккумуляторов, вероятно, была допустима переполюсовка аккумулятора по ошибке или с какими-то целями и он какое-то время после этого работал. В том что она допустима сейчас я сомневаюсь.
Таких ячеек в 12В аккумуляторе 6 шт, в 6В — 3 шт. и т.д. Многих вводит в заблуждение значение напряжения на аккумуляторах. Причем значений напряжения номинального, заряда, разряда. С одной стороны, аккумуляторы называются 12В (и 6В, 24В тоже есть, по-моему, даже 4В изредка встречаются) но на корпусе тех-же аккумуляторов для ИБП производитель указывает напряжение выше 13.5В.
Например:

Тут мы видим, что в форсированном режиме напряжение заряда может быть аж 15В.
Все разъяснит кривая напряжения на АКБ:

Слева мы видим напряжение для аккумулятора из 12 ячеек (24В номинальных), 6 (12В номинальных) и, самое полезное, для одной ячейки. Там-же отмечены области нежелательных напряжений при разряде/ заряде. Из кривой можно сделать выводы:
- Напряжение 12В, 24В и т.д. являются номинальными и показывают лишь число гальванических ячеек (путем деления на два) в батарее. Это просто название для удобства.
- Напряжение при заряде могут достигать 2.5 В/ ячейку что для 12В аккумулятора соответствует 15В.
- Напряжение заряженной батареи считается допустимым при значении 2.1-2.2 В/ячейку, что для 12В аккумулятора соответствует 12.6-13.2В.
Теоретически, батарею можно зарядить и до значений 2.4 В/ячейку или даже немного выше, однако, такая зарядка будет негативно сказываться как на состоянии электродов, так и на концентрации электролита. Однажды, перед сдачей в утиль, я легко зарядил 12В батарею до напряжения ок. 14.5В (уже не помню точное значение).
Итак, автор статьи с которой я начал, решил, что напряжение заряда автомобильной АКБ и АКБ от ИБП отличаются. Это неверно, у них одинаковый тип электродов и одинаковая концентрация серной кислоты в электролите (подобранная давным-давно экспериментальным путем, чтобы предоставлять максимальное напряжение и минимальном саморазряде). Однако, что-же происходит в батарее, почему ее нельзя заряжать при слишком высоком значении напряжения?
Почему в автомобильную АКБ нужно подливать воду, а в АКБ от ИБП не нужно? Эти вопросы позволяют нам плавно перейти в область напряжения разложения воды. Как я написал выше, при зарядке аккумулятора происходит электролиз. Однако, не весь ток расходуется на превращение PbSO4 в PbO2 и Pb. Часть тока будет неизбежно расходоваться и на разложение воды, составляющей значительную часть электролита:
2h3O = 2h3 + O2
Теоретический расчет дает значение напряжения для этой реакции ок. 1.2В. Напоминаю, что напряжение на ячейке при заряде заведомо более 2В. К счастью, активно вода начинает разлагаться только выше 2В, а в промышленности для получения водорода и кислорода из нее процесс ведут и вовсе при 2.1-2.6В (при повышенной температуре). Как бы то ни было, тут мы приходим к выводу, что в конце процесса заряда АКБ будет неизбежно происходить процесс разложения воды в электролите на элементы. Образующиеся кислород и водород попросту улетучиваются из сферы реакции.
Про них бытуют следующие мифы:
1. Водород крайне взрывоопасен! Перезарядишь аккумулятор — и как минимум лишишься комнаты, где тот был!
На самом деле, водорода в процессе электролиза выделяется ничтожно мало по сравнению с объемом комнаты. Водород взрывается при концентрации от 4% в воздухе. Если мы допустим, что электролиз ведется в комнате размером 3*3*3 метра или 27 метров куб., то нам понадобится наполнить помещение 27*0.04=1.1 метров куб. водорода. Для получения такого количества h3 нужно было бы полностью разложить ок. 49 моль воды или 884 грамма ее. Если кто-то наблюдал электролиз, то поймет насколько это много. Или попробуем перейти ко времени. При силе тока в стандартной зарядке для крупногабаритных АКБ в 6А, уравнение Фарадея дает время, необходимое для получения этого количества водорода, аж 437 часов или 18.2 дня. Чтобы наполнить комнату водородом до взрывоопасной концентрации нужно забыть про зарядку на 2 с половиной недели! Но даже если это случится, концентрация серной кислоты просто будет расти пока ее раствор не приобретет слишком высокое сопротивление для жалких 12В зарядки и сила тока не станет ничтожной. Да и водород попросту улетучится.
Очень редко случаются взрывы непосредственно в корпусах крупногабаритных АКБ из-за того, что выделяющийся водород по какой-то причине не может покинуть замкнутого пространства. Но и в этом случае нечего страшного не бывает — чаще всего взрыва хватает только на небольшую деформацию верхней части корпуса, но не на разрыв свинцовых соединений. И АКБ еще может работать дальше даже после таких повреждений.
2. При электролизе может образоваться смертельно ядовитый и, не менее взрывоопасный чем водород, сероводород!
Не наш, периодически попадался миф в англоязычных постах. Теоретически конечно возможно подать такое большое напряжение и создать т.о. такую большую силу тока, что на катоде начнется процесс восстановления сульфат-иона. Напряжение для этого будет достаточным, а продукты восстановления не будут успевать диффундировать подальше от электрода и восстановление будет идти дальше. Но зарядка в пределах десятка-трех вольт и с ограничением силы тока в 6А на такое едва ли способна. Однажды, я наблюдал процесс восстановления сульфата до SO2, да, это возможно; однокурсницы по ошибке что-то сделали не то во время опыта. Но это большая редкость т.к. там концентрация серной кислоты была заметно выше той, что используется в АКБ, была иная конструкция электрода и иной его материал и, естественно, напряжения и сила тока были были непомерными. И SO2 не h3S.
3. При электролизе мышьяк и сурьма из материала решеток будут восстанавливаться до ядовитых арсина и стибина!
Действительно, решетки содержат относительно много сурьмы, мышьяка в современных решетках, вероятно, нет вообще. При работе АКБ та решетка на которой происходит восстановление, т.е. катод, разрушению не может подвергаться. Выделяйся даже каким-то образом стибин, он бы тут-же взаимодействовал с PbSO4, восстанавливая его до металла.
Однако, некоторая практическая неприятность тут есть. Газообразные водород и кислород могут увлекать за собой капельки электролита, создавая аэрозоль серной кислоты. Аэрозоль серной кислоты, даже концентрированной, для человека не опасен и просто вызывает кашель. Однако, серная кислота — кошмар для тканей и бумаги. Стоит даже небольшому количеству серной кислоты попасть на одежду и там обязательно появятся дырки или ткань разорвется по этому месту. Через недели, если кислоты много, через месяц, но одежда истлеет.
Так что газовыделения опасаться не стоит с бытовой точки зрения или стоит, но нужно ориентироваться именно на аэрозоль серной кислоты.
Итак, вода начала разлагаться на водород кислород, ее в электролите становится все меньше, что-же дальше? Если это АКБ в котором электролит просто налит в виде слоя жидкости, то начнется повышение саморазряда из-за повышения концентрации серной кислоты. Занятно, что это будет сопровождаться небольшим повышением напряжения (концентрация кислоты растет) на ячейке. Именно поэтому автовладельцы должны постоянно контролировать концентрацию серной кислоты в своих АКБ (при помощи ареометра) и доливать туда воду.
Процедура доливания воды — необходимая часть процесса обслуживания любой АКБ!
Кроме одного их типа, и мы сейчас об этом поговорим.
Иметь аккумулятор, в котором болтается слой едкой, по отношению к металлам, жидкости конечно-же неудобно, а потому попытки избавиться непосредственно от жидкости предпринимались давно, начались чуть ли не в первой половине 20-го века. К слову сказать, не то чтобы слой серной кислоты прямо плескался вокруг электродов. В реальности она неплохо распределена между электродами и окружающими их сепараторами даже в дешевых моделях. Итак, первым вариантом было использование стекловолокна. Достаточно просто окружить электроды стекловолокном которое пропитано серной кислотой и большинство проблем решится. Этот тип АКБ носит название AGM (absorbent glass mat) и таких АКБ для ИБП подавляющее большинство.
Хотя такие АКБ малого форм-фактора и зачастую позиционируются как те, которые можно эксплуатировать в любом положении, с этим нельзя вполне согласиться. Вскрытие крышки стандартного дешевого AGM аккумулятора показывает, что никаких особых крышек там нет, а следовательно, электролит от вытекания удерживают лишь капиллярные силы. Я почти уверен, что если погонять AGM аккумулятор перевернутым вверх дном, то уже после одной зарядки из него польется серная кислота под давление газов.
Второй распространенный тип интереснее, это т.н. гелевые АКБ. А получаются они благодаря следующему. Если подкислять растворимые силикаты, то будет происходить выделение кремневой кислоты:
Na2SiO3 + h3SO4 = Na2SO4 + SiO2 + h3O
Если исходный раствор силиката не отличается качеством, то кремневая кислота будет выделяться в виде стекловидной массы, но если он достаточно чист, то кремневая кислота осадится в виде красивого куска однородного полупрозрачного геля. На этом и основан способ получения гелевых АКБ — простое добавление силикатов к электролиту вызывает его затвердение в гелеобразную массу. Соответственно, вытекать оттуда уже нечему и АКБ действительно можно эксплуатировать в любом положении. Сам по себе процесс образования геля не повышает емкости АКБ и не улучшает его качеств, однако, производители его используют при производстве наиболее качественных моделей, а потому эти АКБ отличаются высоким качеством и большей емкостью. Занятно, что в обоих случаях носителем электролита является SiO2 в той или иной форме.
Оба типа АКБ объединяются в славный тип VRLA — valve-regulated lead-acid battery который и применяется в ИБП. Формально они считаются необслуживаемыми и терпящими эксплуатацию в любом положении, но это не совсем так. Более того, многие уже встречались с эффектом, когда буквально несколько мл воды возвращают к жизни, казалось бы, дохлую АКБ от ИБП. Так получается, потому что и эти аккумуляторы не капли не застрахованы от электролиза воды в электролите, а следовательно, и пересыхания. Все происходит точно так-же, как в крупногабаритных АКБ. А вот самые дорогие и крутые необслуживаемые АКБ содержат катализатор для рекомбинации выделяющихся газов обратно в воду и вот уже у них корпус действительно выполнен абсолютно герметичным. Обращаю внимание, что по-настоящему герметичным и необслуживаемым может быть и аккумулятор типа AGM и GEL, но они-же могут ими и не быть и не содержать катализатора рекомбинации кислорода и водорода. Тогда, несмотря на казалось бы продвинутую конструкцию, пользователю придется либо чаще покупать новые аккумуляторы, либо доливать воду при помощи шприца.
Хотелось бы добавить несколько слов о режимах разряда. Производители АКБ указывают какой ток максимально допустим для той или иной модели, но нужно понимать, что аккумулятор — просто смесь химических веществ и ЭДС генерируется исключительно химическим путем. Это не конденсатор который, по электрогидравлической аналогии, можно сравнить с неким механическим сосудом (с гибкой мембраной). Хотя АКБ могут выдавать очень большие значения силы тока, в реальности они лучше всего эксплуатируются как раз при небольших токах, что в разряде, что в заряде. Поэтому ИБП, рассчитанные на заряды небольших АКБ, при работе с крупногабаритными будут заряжать их в наиболее щадящем режиме. Впрочем, в течении далеко не одних суток. Интересно обратить внимание на то, что чем выше мощность ИБП, тем больше аккумуляторов последовательно предпочитает собирать производитель. Тут все логично — большие токи разряда маленькие АКБ выдерживают очень плохо.
Подводя итоги:
- Малогабаритные и крупногабаритные АКБ идентичны по устройству.
- Для подавляющего большинства АКБ любого размера доливание воды является необходимой частью текущего обслуживания.
- Лишь немногие из дорогих моделей АКБ содержат механизм рекомбинации газов и могут быть названы действительно необслуживаемыми.
- Сам по себе водород, который выделяется при заряде (а это равно постоянной работе в ИБП) АКБ, не является существенной угрозой или проблемой.
- Нужно очень внимательно работать с АКБ, тщательно избегая пролива даже малейших капель электролита, или лишитесь одежды.
- Разряд и заряд малыми токами являются наиболее предпочтительными режимами эксплуатации АКБ.
Утащено с HABRа, автор — @JohnHenry89
Михаил 05 ноября 2018 Автомобиль: Лендровер фрил 2
Взрываются все же.
Мой знакомый во время зарядки подошел к аккумулятору с сигаретой. Взрывом его опалило так, что сгорела слизистая носа и он перестал чувствовать запахи и вкусы еды. Точнее аромат, который мы считаем вкусом. Например отличить картон от клубники без слизистой носа вы не сможете. Знакомый грузин и любит хорошую еду, для него это было очень неприятно. К счастью нос и восприятие вкуса восстановились где-то через месяц.
Аккумулятор цел, и помещение естественно тоже.
Дмитрий К.
Курить вообще вредно. Об этом все знают, но не всегда ожидают, что вот прям настолько вредно
Павел 20 июня 2018 Автомобиль: Nissan
Отличная статья, спасибо!
Администратор
Рады для вас стараться!
Написать сообщение
устройство, принцип действия, достоинства и недостатки
 Своё название щелочные аккумуляторы получили от вида электролита, необходимого для их работы. Основными разновидностями электролита, используемыми в щелочных аккумуляторах, являются едкий калий (КОН) и едкий натрий (NaOH). При сравнении щелочных аккумуляторов с кислотными батареями, очевидно, что аккумуляторы, работающие на электролите, имеют некоторые преимущества. Однако недостатки у них также существуют. Особенности работы щелочных аккумуляторов делают их незаменимыми в некоторых производственных отраслях.
Своё название щелочные аккумуляторы получили от вида электролита, необходимого для их работы. Основными разновидностями электролита, используемыми в щелочных аккумуляторах, являются едкий калий (КОН) и едкий натрий (NaOH). При сравнении щелочных аккумуляторов с кислотными батареями, очевидно, что аккумуляторы, работающие на электролите, имеют некоторые преимущества. Однако недостатки у них также существуют. Особенности работы щелочных аккумуляторов делают их незаменимыми в некоторых производственных отраслях.
Устройство щелочных аккумуляторов
Среди аккумуляторов, работающих при помощи щелочного раствора (электролита), наиболее часто используются два их вида – никель-кадмиевый и никель-металлогидридный. В каждом них положительный электрод состоит из гидроокиси никеля (NiOOH), с добавками графита и окиси бария. Каждая из добавок улучшает качество работы аккумулятора. Графит увеличивает электропроводность электрода, а окись бария увеличивает срок работы аккумулятора. 
Массы отрицательных электродов каждого вида щелочного аккумулятора имеют различный состав. У металлогидридного аккумулятора отрицательный электрод изготовлен из порошкообразного железа и его окислов. В основной состав отрицательного электрода входит также сернистое железо и сернокислый никель. Если батарея никель-кадмиевая, то отрицательный электрод состоит из смеси порошков железа и кадмия.
В качестве электролита преимущественно используют раствор едкого калия (20 %), в который добавлен моногидрат лития, увеличивающий срок эксплуатации щёлочного аккумулятора. Необходимое количество – 20-30 г/литр раствора.
Химические процессы, происходящие при работе щелочного аккумулятора
При использовании щелочного аккумулятора, то есть, при его разряде, гидроокись никеля положительного электрода вступает в реакцию с ионами электролита. Результатом данной реакции становится образование Ni(OH)2 — гидрата закиси никеля
Одновременно подобный процесс происходит на отрицательном электроде, только на нём образуются гидраты окисей кадмия и железа. Разность потенциалов, составляющая около 1,45 вольта, обеспечивается протеканием тока по контурам внешней и внутренней сети. Таков принцип работы щелочного аккумулятора.
При зарядке щелочного аккумулятора происходит обратный химический процесс – при воздействии тока положительные электроды окисляются, превращая гидрат закиси никеля в гидроокись никеля. Отрицательный электрод при этом восстанавливается, в его массе образуется кадмий и железо.
Главная особенность этих процессов в том, что вещества, образующиеся в процессе электрохимических реакций, в реакцию друг с другом не вступают. Они практически не растворяются в электролите. Благодаря такому поведению веществ расход электролита отсутствует, а его плотность не изменяется. 
Особенности эксплуатации щёлочных аккумуляторов
Начиная с момента, когда аккумулятор начинает использоваться по назначению, то есть, к батарее подключается нагрузка, напряжение весьма быстро падает до 1,3 вольта, а затем продолжает снижаться уже медленно. В момент, когда оно уменьшается до 1 вольта, его работу необходимо останавливать.
Далее батарею эксплуатировать не следует, так как её использование при напряжении ниже 1 вольта, приводит к потере ёмкости аккумулятора. Уменьшится и срок его эксплуатации. Повседневный уход за щелочными аккумуляторами ничем не отличается от их кислотных аналогов. Необходима систематическая подзарядка и контроль уровня электролита.
Применение щёлочных аккумуляторов, их достоинства и недостатки.
Щёлочные аккумуляторы находят применение в устройствах систем аварийного электроснабжения, в оборудовании локомотивов и вагонов для пассажиров. Их используют в устройствах электропогрузчиков, электроинструментах и портативных электроинструментах. Телефоны и фотоаппараты также оборудуются щёлочными батареями. Правильно выбрать аккмуляторную батарею можно, протитав статью на нашем сайте.
Основными достоинствами батарей данной конструкции считают:
— Длительный срок службы;
— Небольшой вес;
— Небольшой саморазряд.
Существенным минусом щелочных аккумуляторов является небольшой КПД – всего 55%. Наличие эффекта памяти, приводящего к потере ёмкости.
