Катализатор что это такое в химии: Катализатор — это… Что такое Катализатор? – «Что такое катализатор в химии?» – Яндекс.Знатоки
- 07.12.2020
Катализатор Википедия
 Схема протекания реакции с катализатором
Схема протекания реакции с катализаторомКатализа́тор — химическое вещество, ускоряющее реакцию, но не расходующееся в процессе реакции.
Ингибитор не является противоположным понятием, так как расходуется в ходе реакции[источник не указан 118 дней].
Катализаторы в химии[ | ]
Катализаторы подразделяются на гомогенные и гетерогенные. Гомогенный катализатор находится в одной фазе с реагирующими веществами, гетерогенный — образует самостоятельную фазу, отделённую границей раздела от фазы, в которой находятся реагирующие вещества[1]. Типичными гомогенными катализаторами являются кислоты и основания. В качестве гетерогенных катализаторов применяются металлы, их оксиды и сульфиды.
Реакции одного и того же типа могут протекать как с гомогенными, так и с гетерогенными катализаторами. Так, наряду с растворами кислот применяются имеющие кислотные свойства твёрдые Al
Гетерогенные катализаторы имеют, как правило, сильно развитую поверхность, для чего их распределяют на инертном носителе (силикагель, оксид алюминия, активированный уголь и др.).
Для каждого типа реакций эффективны только определённые катализаторы. Кроме уже упомянутых кислотно-основных, существуют катализаторы окисления-восстановления; для них характерно присутствие переходного металла или его соединения (Со+3, V2O5+MoO3). В этом случае катализ осуществляется путём изменения степени окисления переходного металла.
Много реакций осуществлено при помощи катализаторов, которые действуют через координацию реагентов у атома или иона переходного металла (Ti, Rh, Ni). Такой катализ называется координационным.
Если катализатор обладает хиральными свойствами, то из оптически неактивного субстрата получается оптически активный продукт.
В современной науке и технике часто применяют системы из нескольких катализаторов, каждый из которых ускоряет разные стадии реакции[2][3]. Катализатор также может увеличивать скорость одной из стадий каталитического цикла, осуществляемого другим катализатором. Здесь имеет место «катализ катализа», или
В биохимических реакциях роль катализаторов играют ферменты.
Катализаторы следует отличать от инициаторов. Например, перекиси распадаются на свободные радикалы, которые могут инициировать радикальные цепные реакции. Инициаторы расходуются в процессе реакции, поэтому их нельзя считать катализаторами.
Ингибиторы иногда ошибочно считают отрицательными катализаторами. Но ингибиторы, например, цепных радикальных реакций, реагируют со свободными радикалами и, в отличие от катализаторов, не сохраняются. Другие ингибиторы (каталитические яды) связываются с катализатором и его дезактивируют, здесь имеет место подавление катализа, а не отрицательный катализ. Отрицательный катализ в принципе невозможен: он обеспечивал бы для реакции более медленный путь, но реакция, естественно, пойдёт по более быстрому, в данном случае, не катализированному, пути.
Катализатор Википедия
Схема протекания реакции с катализаторомКатализа́тор — химическое вещество, ускоряющее реакцию, но не расходующееся в процессе реакции.
Ингибитор не является противоположным понятием, так как расходуется в ходе реакции[источник не указан 118 дней].
Катализаторы в химии
Катализаторы подразделяются на гомогенные и гетерогенные. Гомогенный катализатор находится в одной фазе с реагирующими веществами, гетерогенный — образует самостоятельную фазу, отделённую границей раздела от фазы, в которой находятся реагирующие вещества
Реакции одного и того же типа могут протекать как с гомогенными, так и с гетерогенными катализаторами. Так, наряду с растворами кислот применяются имеющие кислотные свойства твёрдые Al2O3, TiO2, ThO2, алюмосиликаты, цеолиты. Гетерогенные катализаторы с основными свойствами: CaO, BaO, MgO[1].
Гетерогенные катализаторы имеют, как правило, сильно развитую поверхность, для чего их распределяют на инертном носителе (силикагель, оксид алюминия, активированный уголь и др.).
Для каждого типа реакций эффективны только определённые катализаторы. Кроме уже упомянутых кислотно-основных, существуют катализаторы окисления-восстановления; для них характерно присутствие переходного металла или его соединения (Со+3, V2O5+MoO3). В этом случае катализ осуществляется путём изменения степени окисления переходного металла.
Много реакций осуществлено при помощи катализаторов, которые действуют через координацию реагентов у атома или иона переходного металла (Ti, Rh, Ni). Такой катализ называется координационным.
Если катализатор обладает хиральными свойствами, то из оптически неактивного субстрата получается оптически активный продукт.
В современной науке и технике часто применяют системы из нескольких катализаторов, каждый из которых ускоряет разные стадии реакции[2][3]. Катализатор также может увеличивать скорость одной из стадий каталитического цикла, осуществляемого другим катализатором. Здесь имеет место «катализ катализа», или катализ второго уровня[2].
В биохимических реакциях роль катализаторов играют ферменты.
Катализаторы следует отличать от инициаторов. Например, перекиси распадаются на свободные радикалы, которые могут инициировать радикальные цепные реакции. Инициаторы расходуются в процессе реакции, поэтому их нельзя считать катализаторами.
Ингибиторы иногда ошибочно считают отрицательными катализаторами. Но ингибиторы, например, цепных радикальных реакций, реагируют со свободными радикалами и, в отличие от катализаторов, не сохраняются. Другие ингибиторы (каталитические яды) связываются с катализатором и его дезактивируют, здесь имеет место подавление катализа, а не отрицательный катализ. Отрицательный катализ в принципе невозможен: он обеспечивал бы для реакции более медленный путь, но реакция, естественно, пойдёт по более быстрому, в данном случае, не катализированному, пути.
Катализаторы в автомобилях
Задачей автомобильного катализатора является снижение количества вредных веществ в выхлопных газах. Среди них:
См. также
Примечания
- ↑ 1 2 Химическая энциклопедия. — М.: Советская энциклопедия, 1990. — Т. 2. — С. 335, 337. — ISBN 5-85270-035-5.
- ↑ 1 2 Имянитов Н. С. Системы из нескольких катализаторов в металлокомплексном катализе. // Координационная химия. 1984. — Т. 10. — № 11 — С. 1443—1454. — ISSN 0132-344X.
- ↑ Temkin O.N., Braylovskiy S. M. / The mechanism of catalysis in homogeneous polyfunctional catalytic systems. // Fundamental Research in Homogeneous Catalysis. — Ed. by A.E. Shilov. — New York etc: Gordon and Breach Science Publishers, 1986. — Vol. Two. — P.621- 633.
- ↑ Автомобильный катализатор и его роль в выхлопной системе (неопр.). AutoRelease.ru. Архивировано 25 августа 2011 года.
Ссылки
27. Катализаторы химических реакций. Представление о механизме катализа. Специфичность катализа. Примеры и роль каталитических процессов при химической переработке древесного сырья.
Катализаторы подразделяются на гомогенные и гетерогенные. Гомогенный катализатор находится в одной фазе с реагирующими веществами, гетерогенный — образует самостоятельную фазу, отделённую границей раздела от фазы, в которой находятся реагирующие вещества [1]. Типичными гомогенными катализаторами являются кислоты и основания. В качестве гетерогенных катализаторов применяются металлы, их оксиды и сульфиды.
Реакции одного и того же типа могут протекать как с гомогенными, так и с гетерогенными катализаторами. Так, наряду с растворами кислот применяются имеющие кислотные свойства твёрдые Al2O3, TiO2, ThO2, алюмосиликаты, цеолиты. Гетерогенные катализаторы с основными свойствами: CaO, BaO, MgO [1].
Гетерогенные катализаторы имеют, как правило, сильно развитую поверхность, для чего их распределяют на инертном носителе (силикагель, оксид алюминия, активированный уголь и др.).
Для каждого типа реакций эффективны только определённые катализаторы. Кроме уже упомянутых
Много реакций осуществлено при помощи катализаторов, которые действуют через координацию реагентов у атома или иона переходного металла (Ti, Rh, Ni). Такой катализ называется координационным.
Если катализатор обладает хиральными свойствами, то из оптически неактивного субстрата получается оптически активный продукт.
В современной науке и технике часто применяют
В биохимических реакциях роль катализаторов играют ферменты.
Катализаторы следует отличать от инициаторов. Например, перекиси распадаются на свободные радикалы, которые могут инициировать радикальные цепные реакции. Инициаторы расходуются в процессе реакции, поэтому их нельзя считать катализаторами.
механизм катализа: 1)мех. стадийный( изменение пути реакции) 2)ассоциактивный 3)ферментативный 4) микрогетерогенный
Спецефичность катализа заключается в том, что в присутствии катализатора изменяется путь, по которому проходит суммарная реакция, образуются другие переходные состояния с иными энергиями активации, а поэтому изменяется и скорость хим. реакции.
переработка древесины требует больших затрат в производстве, поэтому используют катализаторы, которые ускоряют процесс химического превращения, увеличивают выход продукта и уменьшают выброс вредных веществ. приемущество изп. катализаторов в том что они не требуют больших затрат.
28. Растворы. Процессы при образовании растворов. Идеальные и реальные растворы. Гидраты и сольваты.
Растворы — гомогенные (однородные) системы, то есть каждый из компонентов распределён в массе другого в виде молекул, атомов или ионов
Процесс взаимодействия растворителя и растворённого вещества называется сольватацией (если растворителем является вода — гидратацией).
Энергетической характеристикой растворения является теплота образования раствора, рассматриваемая как алгебраическая сумма тепловых эффектов всех эндо- и экзотермических стадий процесса. Наиболее значительными среди них являются: – поглощающие тепло процессы — разрушение кристаллической решётки, разрывы химических связей в молекулах; – выделяющие тепло процессы — образование продуктов взаимодействия растворённого вещества с растворителем (гидраты) и др.
СОЛЬВАТЫ, продукты присоединения растворителя к растворенным веществам. Обычно сольваты образуются в растворе, но нередко (при охлаждении раствора, испарениирастворителя и др.) м. б. получены в виде кристаллич. фаз-кристаллосольватов.
Гидраты — продукты присоединения воды к неорганическим и органическим веществам
6.2. Понятие о катализе и катализаторах

6. ХИМИЧЕСКАЯ КИНЕТИКА И РАВНОВЕСИЕ
6.1. Скорость химической реакции и влияние на нее различных факторов
Р е ш е н и е. По правилу Вант-Гоффа
Vt 2 |
| t 2 −t1 | t | t | |
| ; 8 = 2 10 ; 2 3 | = 2 10 ; ∆t = 30 °C. | |||
= γ | 10 | ||||
V | |||||
|
|
|
| ||
t1 |
|
|
|
| |
Значительное изменение скорости реакции с изменением температуры объясняет теория активации. Согласно этой теории в химическое взаимо-
действие вступают только активные молекулы, обладающие повышенным уровнем энергиии, достаточной для осуществления данной реакции. Неактивные молекулы можно сделать активными, если сообщить им необходимую дополнительную энергию. Этот процесс называется активацией. Один из способов активации – увеличение температуры: при повышении температуры число активных молекул возрастает, благодаря чему резко увеличивается скорость реакции.
Энергия, которую надо сообщить молекулам реагирующих веществ, чтобы превратить их в активные, называется энергией активации. Ее определяют опытным путем, обозначают буквой Еа и обычно выражают в кДж/моль. Например, для соединения водорода и йода
h3 + J2 = 2HJ Еа = 167,4 кДж/моль,
а для реакции распада иодоводорода
2HJ = h3 + J2 Еа = 186,2 кДж/моль.
Энергия активации Еа зависит от природы реагирующих веществ и служит характеристикой каждой реакции. Скорость реакции непосредственно зависит от значения энергии активации: если она мала, то за определенное время протекания реакции энергетический барьер преодолеет большее количество частиц и скорость реакции будет высокой, но если энергия активации велика, то реакция идет медленно.
При взаимодействии ионов энергия активации очень мала и ионные реакции протекают с очень большой скоростью, практически мгновенно.
Увеличить скорость реакции можно с помощью катализаторов. Применять катализаторы выгоднее, чем повышать температуру, тем более, что ее повышение далеко не всегда возможно.
Катализаторами называются вещества, изменяющие скорость химической реакции, но сохраняющие при этом свои свойства и состав. Сам катализатор в реакциях не расходуется и в конечные продукты не входит.
Одни катализаторы ускоряют реакцию – положительный катализ, или просто катализ, другие замедляют – отрицательный катализ. Примером положительного катализа может служить получение серной кислоты из оксида
Химия. Учеб. пособие | -66- |

6.ХИМИЧЕСКАЯ КИНЕТИКА И РАВНОВЕСИЕ
6.2.Понятие о катализе и катализаторах
серы (IV) или окисление аммиака в азотную кислоту с помощью платинового катализатора.
Примером отрицательного катализа является замедление взаимодействия раствора сульфита натрия с кислородом воздуха в присутствии этилового спирта или уменьшение скорости разложения пероксида водорода в присутствии небольших количеств серной кислоты. Отрицательный катализ часто называют ингибированием, а отрицательные катализаторы, снижающие скорость реакции, – ингибиторами (механизм действия последних отличен от действия катализаторов).
Химические реакции, протекающие при участии катализаторов, называются каталитическими. Различают два вида катализа – гомогенный (однородный) и гетерогенный (неоднородный) катализ.
При гомогенном катализе реагирующие вещества и катализатор образуют однофазную систему – газовую или жидкую, между катализатором и реагирующими веществами отсутствует поверхность раздела. Например, каталитическое разложение пероксида водорода в присутствии раствора солей (жидкая фаза). Для гомогенного катализа установлено, что скорость химической реакции пропорциональна концентрации катализатора.
При гетерогенном катализе реагирующие вещества и катализатор образуют систему из разных фаз. В этом случае между катализатором и реагирующими веществами существует поверхность раздела. Обычно катализатор
– твердое вещество, а реагирующие вещества – газы или жидкость. Примером может служить окисление аммиака (газообразная фаза) в присутствии платины (твердая фаза). Все реакции при гетерогенном катализе протекают на поверхности катализатора. Поэтому активность твердого катализатора зависит и от свойств его поверхности (размера, химического состава, строения и состояния). На поверхности катализатора имеются активные центры, реагирующие вещества адсорбируются на них, происходит деформация молекул, ослабевают связи между атомами и молекулы становятся активными.
Механизм действия катализаторов обычно объясняют образованием промежуточных соединений с одним из реагирующих веществ. Рассмотрим схему действия катализатора на следующем примере:
1.Основной химический процесс:
А+ В = АВ; SO2 + ½O2 = SO3
2.Образование промежуточного соединения одного из исходных веществ с катализатором NO:
К+ В = КВ; NO + ½O2 = NO2
3.Взаимодействие промежуточного соединения со вторым исходным веществом и освобождение катализатора:
КВ + А = АВ + К; NO2 + SO2 = SO3 + NO (катализатор)
Химия. Учеб. пособие | -67- |
6.ХИМИЧЕСКАЯ КИНЕТИКА И РАВНОВЕСИЕ
6.2.Понятие о катализе и катализаторах
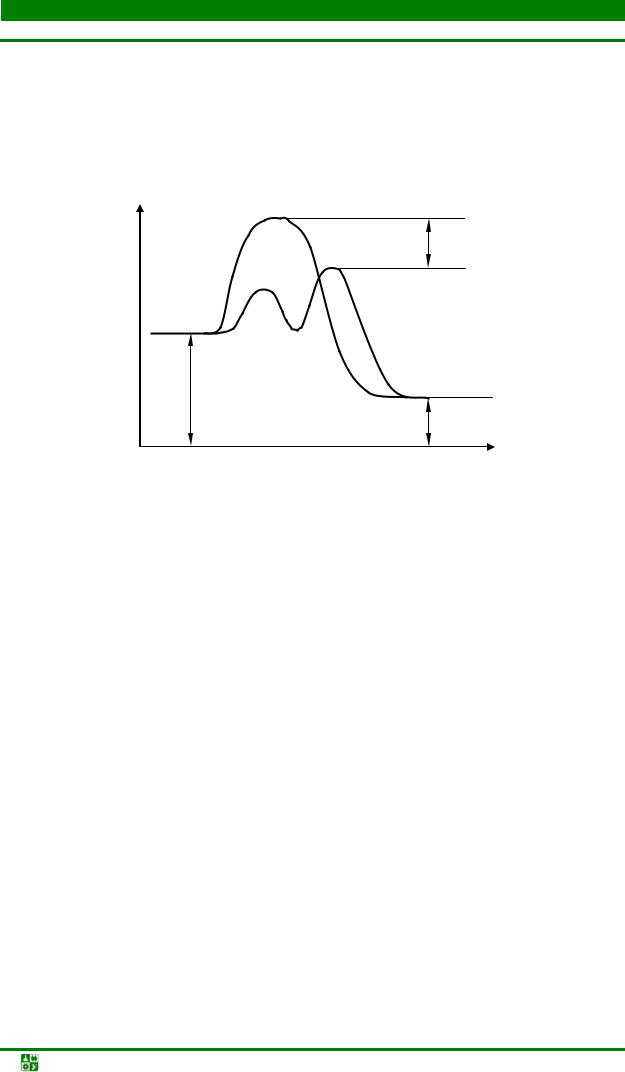
Катализатор разбивает ход химической реакции на несколько стадий. Соответственно, у каждой стадии имеется свой энергетический барьер. В сумме он составляет энергию активации Еа. За счет снижения энергетических барьеров по стадиям реакции протекают с большими скоростями (рис. 6.2).
А +КВ → [А…КВ]# (активированный комплекс) → АВ + К
G | [A…B]# |
| |
| ( G)# |
| [B…AK] # |
| [A…K]# |
A+B
A+B+K AK
AB
Gисходное
Gконечное
Рис. 6.2. Энергетическая схема хода реакции при отсутствии и в присутствии катализатора
Некоторые вещества снижают или полностью уничтожают активность твердого катализатора. Такие вещества называются каталитическими ядами. В качестве примера можно привести соединения мышьяка, ртути, свинца, цианистые соединения, к которым особенно чувствительны платиновые катализаторы.
Однако имеются и такие вещества, которые усиливают действие катализаторов, хотя сами катализаторами не являются. Эти вещества называются промоторами (промотирование платиновых катализаторов добавками железа, алюминия и др.).
Следует особо отметить, что действие катализаторов избирательно, поэтому из одного и того же вещества можно получить разные продукты.
Особую роль играют биологические катализаторы – ферменты. При их участии протекают сложные химические процессы в растительных и животных организмах.
6.3. Колебательные реакции
Существуют химические реакции, при протекании которых происходит периодическое изменение концентраций реагирующих веществ. Наибо-
лее известной колебательной реакцией является реакция Белоусова – Жаботинского, впервые исследованная в 60-х гг. ХХ в. Эта реакция представляет
Химия. Учеб. пособие | -68- |

6.ХИМИЧЕСКАЯ КИНЕТИКА И РАВНОВЕСИЕ
6.3.Колебательные реакции
собой каталитическое окисление малоновой кислоты Ch3(COOH)2 броматионом BrO 3− в присутствии иона германия Ge4+ в кислом водном растворе.
Колебания концентраций заметны по периодическому исчезновению и появлению желтой окраски, вызванной ионами Ge4+. Также периодически изменяются температура и концентрации других продуктов, являющихся интермедиатами (Br–, Br2). Для объяснения колебательных изменений предложен механизм, включающий следующие стадии:
1.BrO3− + Br– + 2H+ → HBrO2 + HBrO
2.HBrO2 + Br– + H+ → 2HBrO
3.BrO3− + HBrO2 + 2Ge3+ + 3H+ → 2HBrO2 + 2Ge4+ + h3O
4.2HBrO2 → BrO3− + HBrO + H+
5.nGe4+ + BrCH(COOH)2 → nGe3+ + продукты окисления.
Броммалоновая кислота образуется в результате реакции
Ch3(COOH)2 + HBrO → BrCH(COOH)2 + h3O
Общее уравнение имеет вид
2 BrO3− + 3Ch3(COOH)2 + 2H+ → 2BrCH(COOH)2 + 3CO2 + 4h3O
Это наиболее упрощенный вариант механизма. Более поздние модели включают 22-стадийные химические процессы в растительных и животных организмах.
6.4. Химическое равновесие и его смещение
Обратимыми называются такие реакции, которые одновременно протекают в двух взаимно противоположных направлениях.
В уравнениях обратимых реакций между левой и правой частями ставят две стрелки, направленные в противоположные стороны. Примером такой реакции может служить синтез аммиака:
3h3 (г) + N2 (г) →← 2Nh4 (г) ∆H = −46,2 кДж/моль.
В технике обратимые реакции, как правило, невыгодны. Поэтому различными методами (изменением температуры, давления и др.) их делают практически необратимыми.
Реакции, которые протекают только в одном направлении и завершаются полным превращением реагирующих веществ в конечные вещества, на-
зываются необратимыми.
Примером такой реакции может служить разложение хлората калия (бертолетовой соли) при нагревании:
Химия. Учеб. пособие | -69- |

6.ХИМИЧЕСКАЯ КИНЕТИКА И РАВНОВЕСИЕ
6.4.Химическое равновесие и его смещение
2KClO3 → 2KCl + 3O2 ↑
Необратимых реакций не так много. Большинство реакций являются обратимыми.
Необратимыми называют такие реакции, при протекании которых:
1. Образующиеся продукты уходят из сферы реакции – выпадают в виде осадков или выделяются в виде газа, например:
BaCl2 + h3SO4 → BaSO4↓ + 2HCl
Na2CO3 + 2HCl→ 2 NaCl + CO2↑ + h3O
2. Образуется малодиссоциирующее соединение, например, вода:
HCl + NaOH → h3O + NaCl
3. Реакция сопровождается большим выделением энергии, например, горение магния:
2Mg + O2↑ → 2MgO, ∆H = − 602,5 кДж.
4.Образуется комплексное соединение.
Вуравнениях необратимых реакций между правой и левой частями ставится знак равенства или одна стрелка.
Под химическим равновесием понимается такое состояние обратимой реакции, когда скорости прямой и обратной реакции равны.
Обратимые реакции не доходят до конца и заканчиваются установлением химического равновесия, например:
h3 (г) + J2 (г) →← 2HJ (г)
В состояния равновесия прямая и обратная реакции не прекращаются. Поэтому такое равновесие называется подвижным или динамическим.
Используя закон действия масс, напишем выражение для скоростей прямой и обратной реакций:
| → | → | ] [J2 |
| ← | ← |
|
|
| ||
| V = k[h3 | ]; V = k[HJ]2 , |
| ||||||||
|
|
| → | ← |
|
|
|
|
|
| |
если в состоянии равновесия V = V , то |
|
|
|
|
| ||||||
|
| ← |
|
|
| ← | [HJ]2 , |
| |||
|
| k =[Н2 ] [J2 | ]= k |
| |||||||
или |
|
|
|
|
|
|
|
|
| ||
| → | [HJ]2 |
|
|
|
| [HJ]2 |
|
| ||
| k | = | , | Kp = | . | ||||||
| ← | [h3 ] [J2 ] | [h3 ] [J2 ] | ||||||||
| k |
|
|
|
| ||||||
Химия. Учеб. пособие | -70- |

6.ХИМИЧЕСКАЯ КИНЕТИКА И РАВНОВЕСИЕ
6.4.Химическое равновесие и его смещение
→ ←
Отношение К/ К называется константой химического равновесия (обозначается Кр), которая постоянна при данной температуре, зависит от температуры и природы реагирующих веществ и не зависит от концентрации.
Химическое равновесие наступает при постоянстве внешних условий (давлении, концентрации, температуре). Изменение этих условий нарушает равновесие и вызывает увеличение скорости прямой или обратной реакции. Через некоторое время снова наступает равновесие. Переход реакционной системы от одного состояния равновесия к другому называется смещением (или сдвигом) химического равновесия.
Направление смещения химического равновесия при изменении концентрации реагирующих веществ, температуры и давления (в случаях газовых реакций) определяется общим положением, известным под названием принципа подвижного равновесия или принципа Ле Шателье: если на сис-
тему, находящуюся в равновесии, оказать какое-либо внешнее воздействие (изменить концентрацию, температуру, давление), то равновесие сместится в том направлении, где оказанное воздействие уменьшится.
Поясним это на примере следующей реакции:
→ | 2Nh4 (г) | ∆H = −92,4 кДж. |
3Н2 (г) + N2 (г) ← | ||
3 объема 1 объем | 2 объема |
|
Влияние концентрации на смещение равновесия. Если внешнее воздей-
ствие выражается в увеличении концентрации азота или водорода (исходных веществ), равновесие смещается к аммиаку, т. е. в сторону прямой реакции, протекающей с получением продуктов реакции. Соответственно, увеличение концентрации аммиака смещает равновесие в сторону исходных веществ.
Влияние температуры на смещение равновесия. При повышении тем-
пературы равновесие смещается в сторону эндотермической реакции, протекающей с поглощением тепла, а при понижении температуры – в сторону экзотермической реакции, идущей с выделением тепла. В данном случае повышение температуры смещает равновесие в сторону обратной реакции, т. к. эта реакция идет с выделением тепла ( Н < 0).
Влияние давления на смещение равновесия. Чтобы определить влияние давления на смещение равновесия, необходимо подсчитать число молей газообразных веществ в правой и левой частях уравнения. В приведенном примере в левой части уравнения содержится четыре моля газов, а в правой – один. Если понижать давление, то равновесие сместится в сторону возрастания числа молей газа (4 объема), т. е. в обратном направлении. Если увеличить давление, то равновесие сместится в сторону меньшего объема (2 моль вещества), т. е. в прямом направлении.
Если же в уравнении обратимой реакции число молей газов в левой части равно числу молей в правой части, например,
N2 (г) + O2 (г) →← 2NO (г)
то изменение давления не вызывает смещения химического равновесия.
Химия. Учеб. пособие | -71- |
Катализаторы биологические — это… Что такое Катализаторы биологические?
- Катализаторы биологические
- биокатализаторы, вещества, образующиеся в живых клетках и ускоряющие (положительный Катализ) или замедляющие (отрицательный катализ) химические процессы, протекающие в организмах. К числу К. о. относятся в первую очередь Катализаторы белковой природы, называемые энзимами, или ферментами (См. Ферменты).
Большая советская энциклопедия. — М.: Советская энциклопедия. 1969—1978.
- Катализаторы
- Каталитические яды
Смотреть что такое «Катализаторы биологические» в других словарях:
КАТАЛИЗАТОРЫ — вещества, ускоряющие химические реакции. Вещества, замедляющие реакции, называются ингибиторами. Биологические катализаторы называются ферментами. Катализаторами служат синтетические алюмосиликаты, металлы платиновой группы, серебро, никель и др … Большой Энциклопедический словарь
Катализаторы — вещества, ускоряющие химические реакции (ср.: ингибиторы замедлители реакций). Биологические К. называются ферментами. Наиболее распространенными К. являются: синтетические алюмосиликаты, металлы платиновой группы, серебро, никель и др … Российская энциклопедия по охране труда
катализаторы — вещества, ускоряющие химические реакции. Вещества, замедляющие реакции, называются ингибиторами. Биологические катализаторы называются ферментами. Катализаторами служат синтетические алюмосиликаты, металлы платиновой группы, серебро, никель и др … Энциклопедический словарь
Катализаторы — (см. Катализ) вещества, как правило, ускоряющие (в противоположность ингибиторам) скорость химических реакций. Катализаторы не смещают равновесие, а изменяют скорости прямой и обратной реакций, способствуют скорейшему достижению равновесия.… … Начала современного естествознания
ПОЛИМЕРЫ БИОЛОГИЧЕСКИЕ — (биополимеры) природные макромолекулы, играющие осн. роль в биол. процессах. К П. б. относятся белки, нуклеиновые кислоты (НК) и полисахариды. П. б. образуют структурную основу всех живых организмов; все процессы в клетке связаны с… … Физическая энциклопедия
Катализатор — (Catalyst) Определение катализатора, механизм действия катализатора Определение катализатора, механизм действия катализатора, применение катализатора Содержание Содержание 1. в химии Виды катализаторов Механизм действия катализаторов Требования,… … Энциклопедия инвестора
КАТАЛИЗ — ускорение химических реакций под действием малых количеств веществ (катализаторов), которые сами в ходе реакции не изменяются. Каталитические процессы играют огромную роль в нашей жизни. Биологические катализаторы, называемые ферментами,… … Энциклопедия Кольера
Катализ — (от греч. katálysis разрушение) изменение скорости химических реакций в присутствии веществ (катализаторов (См. Катализаторы)), вступающих в промежуточное химическое взаимодействие с реагирующими веществами, но восстанавливающих после… … Большая советская энциклопедия
фермент — Термин фермент Термин на английском enzyme Синонимы Аббревиатуры Связанные термины активный центр катализатора, белки, биологические моторы, биологические нанообъекты, биосенсор, генная инженерия, иммобилизация, кинезин, клетка, лаборатория на… … Энциклопедический словарь нанотехнологий
Биотехнологии — Биотехнология интеграция естественных и инженерных наук, позволяющая наиболее полно реализовать возможности живых организмов или их производные для создания и модификации продуктов или процессов различного назначения. Чаще всего применяется в… … Википедия
Алкилирование — Википедия
Материал из Википедии — свободной энциклопедии
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 13 марта 2013; проверки требуют 13 правок. Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 13 марта 2013; проверки требуют 13 правок.Алкилирование — введение алкильного заместителя в молекулу органического соединения. Типичными алкилирующими агентами являются алкилгалогениды, алкены, эпоксисоединения, спирты, реже альдегиды, кетоны, эфиры, сульфиды, диазоалканы. Катализаторами алкилирования являются минеральные кислоты, кислоты Льюиса а также цеолиты.
Алкилирование широко применяется в химической и нефтехимической промышленности.
Процесс алкилирования направлен на получение высокооктановых компонентов автомобильного бензина из непредельных углеводородных газов. В основе процесса лежит реакция соединения алкена и алкана с получением алкана с числом атомов углерода, равным сумме атомов углерода в исходном алкене и алкане. Поскольку наибольшим октановым числом обладают молекулы алканов с изо-строением, то молекулы исходного сырья тоже должны иметь изо-строение. В нефтепереработке наибольшее распространение получило сырье алкилирования бутан-бутиленовая фракция (ББФ), которая получается в процессе каталитического крекинга.
Типовой состав ББФ с установки FCC.
| Компонент | Содержание, % масс. |
|---|---|
| пропилен | 0,5 |
| пропан | 1,5 |
| n-бутан | 10 |
| i-бутан | 35 |
| i-бутилен | 16 |
| n-бутен | 12 |
| t-бутен | 14 |
| z-бутен | 10 |
| пентен | 0,3 |
| i-пентан | 0,6 |
| n-пентан | 0,1 |
Основные реакции:
- изо-бутан + 1-бутилен = изо-октан (2,2,4-триметилпентан) (Октановое число — 100 ед.)
- изо-бутан + бутилен-2 = изо-октан (2,3,3-триметилпентан) (ОЧМ < 100)
- изо-бутан + изо-бутилен = изо-октан (2,3,4-триметилпентан) (ОЧМ<100)
Побочные реакции из-за примесей пропилена и нормального бутилена
- изо-бутан + пропилен = изо-гептан (2,2-диметилпентан) (ОЧМ<<100)
Режим работы реактора
| Параметр | Значение |
|---|---|
| Температура, °C | 38 |
| Давление, МПа | 0,6 — 1,0 |
| Мольное соотношение изобутан:бутилены | 6 — 12 |
| Катализатор | Плавиковая кислота (HF) |
| Объемное соотношение между у/в и фторводородной кислотой | 0,7 — 1,5 |
| Время контакта сырья с катализатором, мин. | 20 −30 |
Октановое число смеси продуктов реакции (алкилат) около 95, следует отметить важную особенность равенства октановых чисел по моторному методу и исследовательскому. Так, например, продукт каталитического риформинга (риформат) имеет исследовательское октановое число 95 и моторное 85, в то время как алкилат 95 и 92 соответственно. Это обстоятельство делает его наиболее ценным компонентом товарных бензинов. Однако его себестоимость так же очень велика. К тому же есть конкурирующий процесс использования ББФ — производство МТБЭ.
Сырье алкилирования — бутан-бутиленовую фракцию (ББФ) необходимо очищать от сернистых соединений, которые в основном представлены меркаптанами. Метод очистки ББФ от меркаптанов заключается в щелочной экстракции меркаптанов из углеводородной фракции и последующей регенерации щелочи в присутствии гомогенных или гетерогенных катализаторов кислородом воздуха с выделением дисульфидного масла. Данный процесс называется Merox.
КАТАЛИТИЧЕСКИЕ РЕАКЦИИ — это… Что такое КАТАЛИТИЧЕСКИЕ РЕАКЦИИ?
- КАТАЛИТИЧЕСКИЕ РЕАКЦИИ
- КАТАЛИТИЧЕСКИЕ РЕАКЦИИ КАТАЛИТИ́ЧЕСКИЕ РЕА́КЦИИ (от греч. «katalysis» — разрушение), гомогенные (см. ГОМОГЕННЫЕ РЕАКЦИИ) и гетерогенные (см. ГЕТЕРОГЕННЫЕ РЕАКЦИИ) химические реакции, протекающие с участием катализатора (см. КАТАЛИЗАТОРЫ). В зависимости от положительного или отрицательного каталитического действия скорость основной реакции может увеличиваться и уменьшаться. В каталитических реакциях катализатор вводится в небольших количествах и не расходуется: 2SO2 + O2 ® 2SO3 (катализатор V2O5 ). Если катализатором является один из продуктов реакции, то процесс называется автокаталитическим:MgO + 2HF ® MgF2 + H2O (катализатор H2O).
Энциклопедический словарь. 2009.
- КАТАЛИЗА ИНСТИТУТ Сибирского отделения РАН
- КАТАНА
Смотреть что такое «КАТАЛИТИЧЕСКИЕ РЕАКЦИИ» в других словарях:
Каталитические реакции — (циклические) К. реакциями называются многочисленные химические превращения, вызываемые в различных химических системах веществами, которые, не подвергаясь сами каким либо постоянным изменениям, одним своим присутствием обусловливают… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Реакции химические — Химическая реакция превращение одного или нескольких исходных веществ (реагентов) в отличающиеся от них по химическому составу или строению вещества (продукты реакции). В отличие от ядерных реакций, при химических реакциях ядра атомов не меняются … Википедия
Каталитические яды — контактные яды, вещества, вызывающие «отравление» катализаторов (См. Катализаторы) (обычно гетерогенных), т. е. снижающие их каталитическую активность или полностью прекращающие каталитическое действие. Отравление гетерогенных… … Большая советская энциклопедия
Химические реакции — Химическая реакция превращение одного или нескольких исходных веществ (реагентов) в отличающиеся от них по химическому составу или строению вещества (продукты реакции). В отличие от ядерных реакций, при химических реакциях ядра атомов не… … Википедия
Сложные реакции — такие Реакции химические, элементарные акты которых различны. В противоположность С. р. элементарные акты простых реакций не отличаются один от другого природой участвующих в них веществ, а лишь, возможно, направлением превращения, если… … Большая советская энциклопедия
ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ — (р ции окисления восстановления) происходят с изменением степени окисления атомов, входящих в состав реагирующих в в. При окислении в в степень окисления элементов возрастает, при восстановлении понижается. Первоначально окислением называли… … Химическая энциклопедия
СЛОЖНЫЕ РЕАКЦИИ — Хим. р ция реализуется как совокупность множества дискретных актов хим. превращения, в каждом из к рых участвует лишь одна или небольшое число частиц (молекул, атомов, ионов). Если среди актов р ции имеются химически различающиеся, то р ция наз.… … Химическая энциклопедия
ГАЗОФАЗНЫЕ РЕАКЦИИ — (от газ и греч. «phasis» появление), химические реакции между газообразными веществами, происходящие в результате столкновения частиц. Скорость газофазных реакций зависит от температуры и давления. Часто реализуются как гетерогенно каталитические … Энциклопедический словарь
КАТАЛИЗ — ускорение химических реакций под действием малых количеств веществ (катализаторов), которые сами в ходе реакции не изменяются. Каталитические процессы играют огромную роль в нашей жизни. Биологические катализаторы, называемые ферментами,… … Энциклопедия Кольера
Катализ — (от греч. katálysis разрушение) изменение скорости химических реакций в присутствии веществ (катализаторов (См. Катализаторы)), вступающих в промежуточное химическое взаимодействие с реагирующими веществами, но восстанавливающих после… … Большая советская энциклопедия
